| Disponibilidade: | |
|---|---|
| Quantidade: | |











Amplo portfólio de modelos – modelos de haptenos, citocinas, alérgenos e análogos de vitamina D que abrangem endótipos de DA aguda, crônica e dominante Th2/Th17/Th22.
Múltiplas espécies/cepas – BALB/c (com tendência a Th2), C57BL/6 (com tendência a Th1/Th17) e ratos SD disponíveis.
Endpoints abrangentes – Peso corporal, espessura da orelha, pontuação da pele, eventos de coceira, IgE sérica, perfil de citocinas (IL‑4, IL‑13, IL‑17, IL‑36), histopatologia (HE, azul de toluidina), espessura epidérmica.
Valor translacional – Ideal para testar inibidores de JAK, produtos biológicos (anti‑IL‑4Rα, anti‑IL‑13), inibidores de PDE4 e agentes tópicos.
Pacotes de dados prontos para IND – Os estudos podem ser conduzidos de acordo com os princípios das BPL.
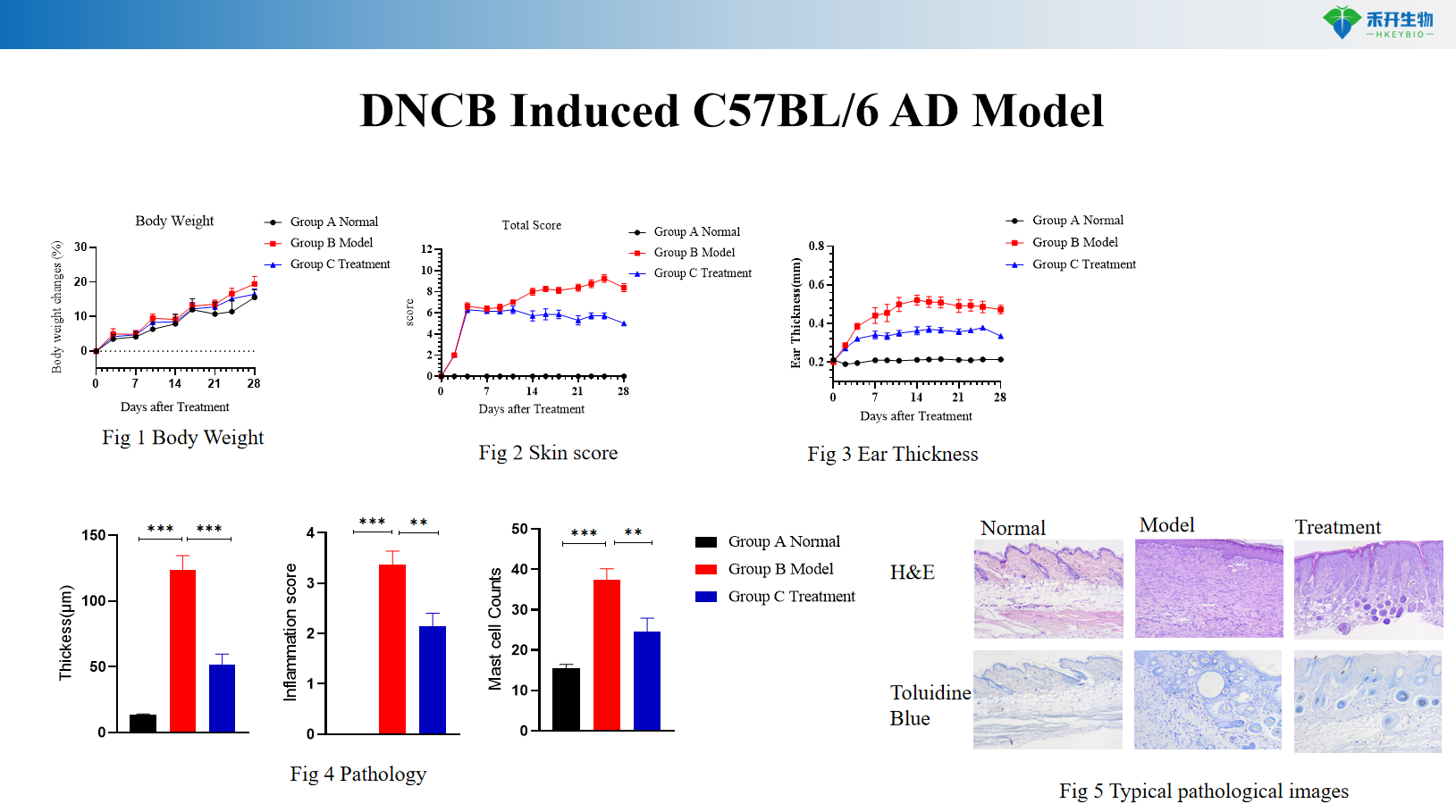
Modelo C57BL/6 AD induzido por DNCB
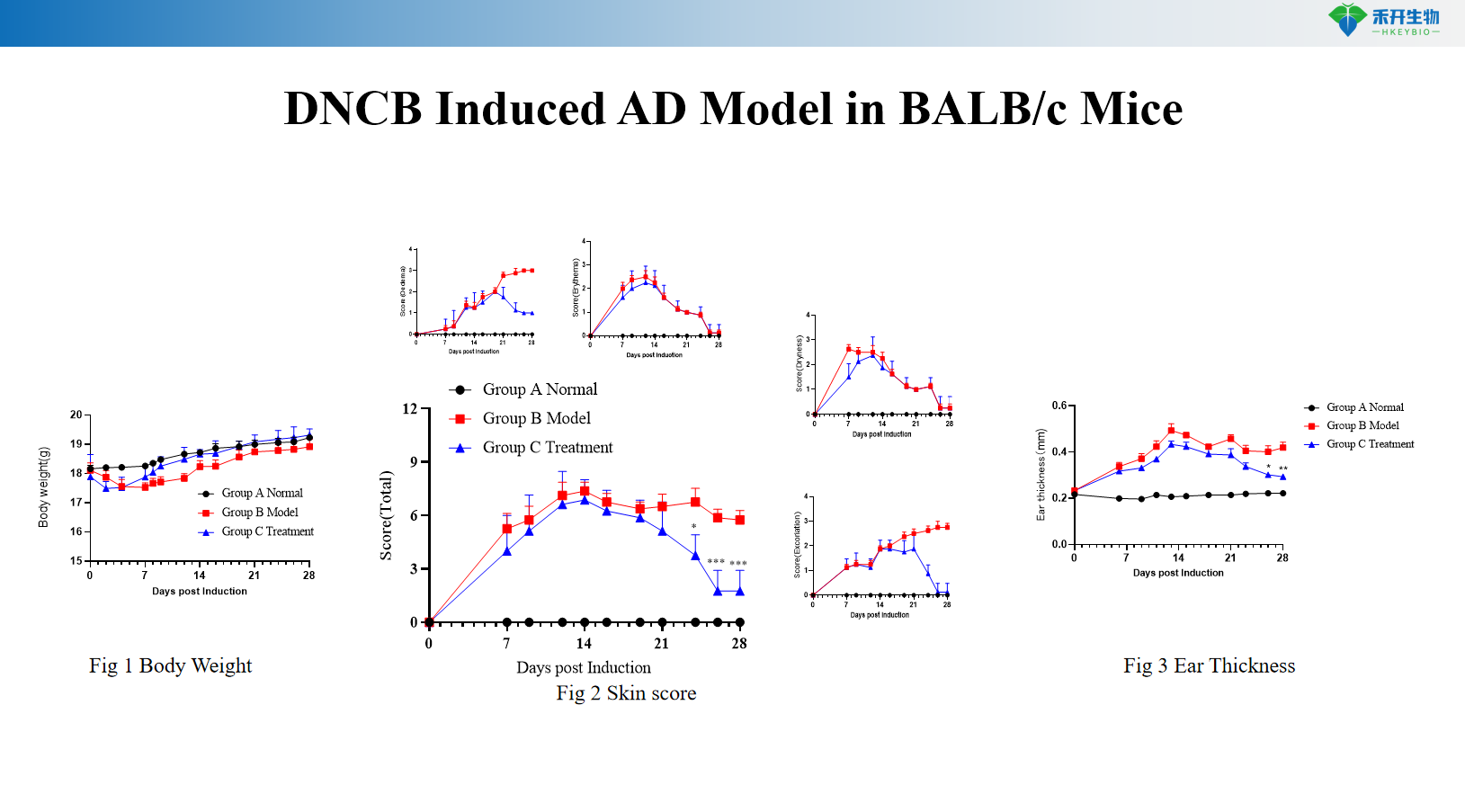
Modelo de AD induzido por DNCB em camundongos BALB/c
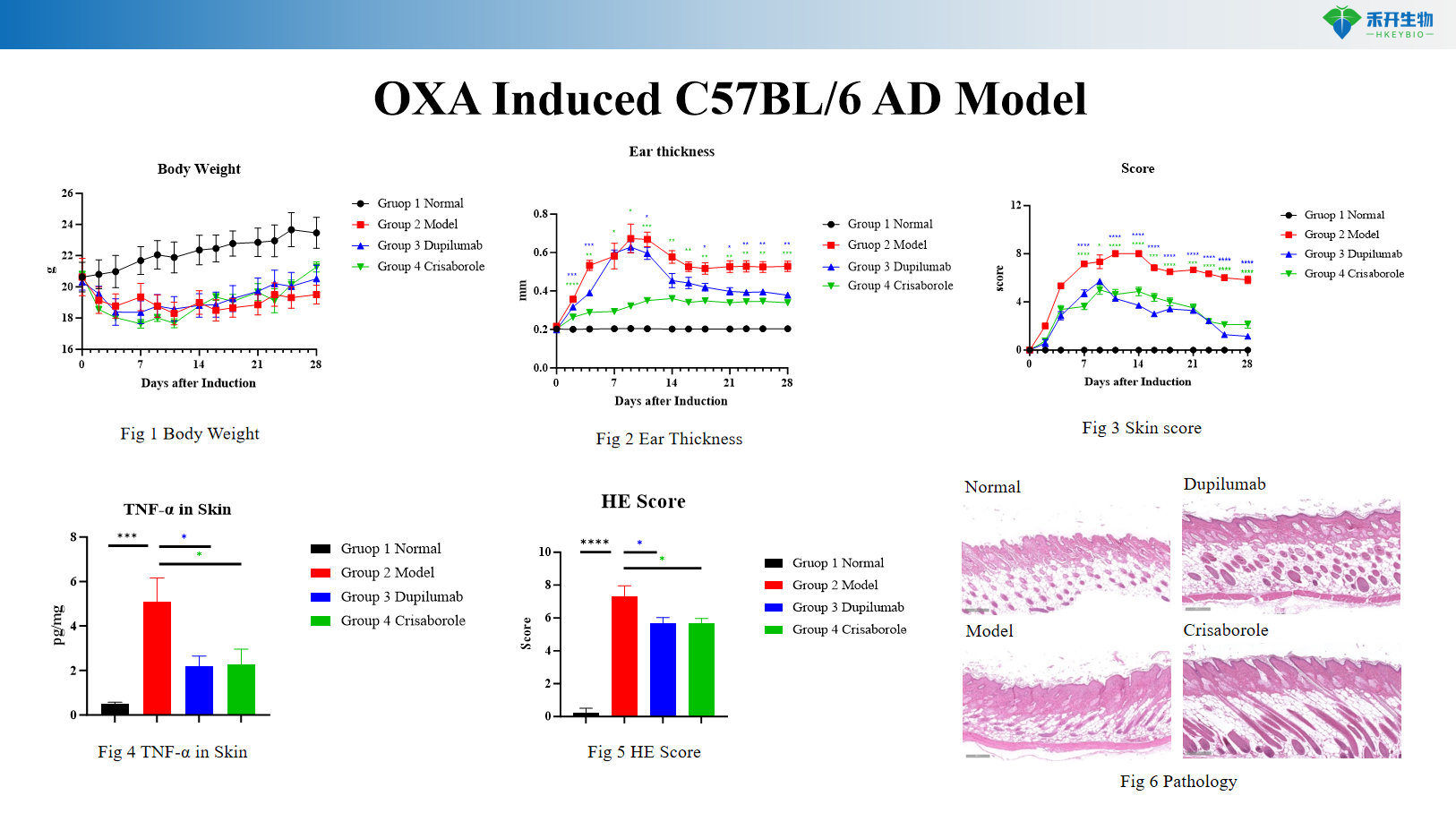
Modelo C57BL/6 AD induzido por OXA
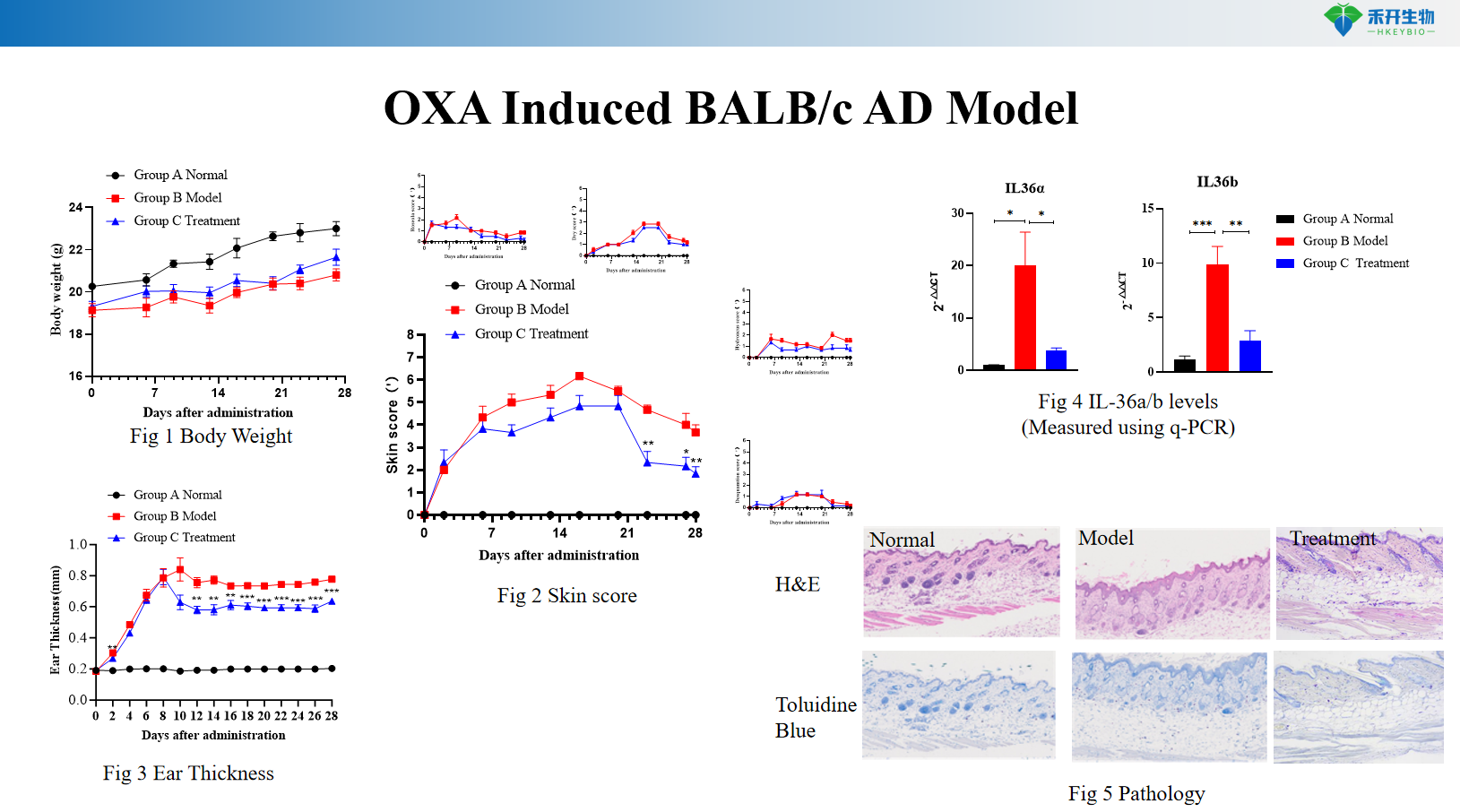
Modelo BALB/c AD induzido por OXA
Modelo C57BL/6 AD induzido por MC903

Modelo AD BALB/c induzido por MC903


Modelo de DA induzida por MC903 e OXA em BALB/c

Modelo BALB/c AD induzido por FITC
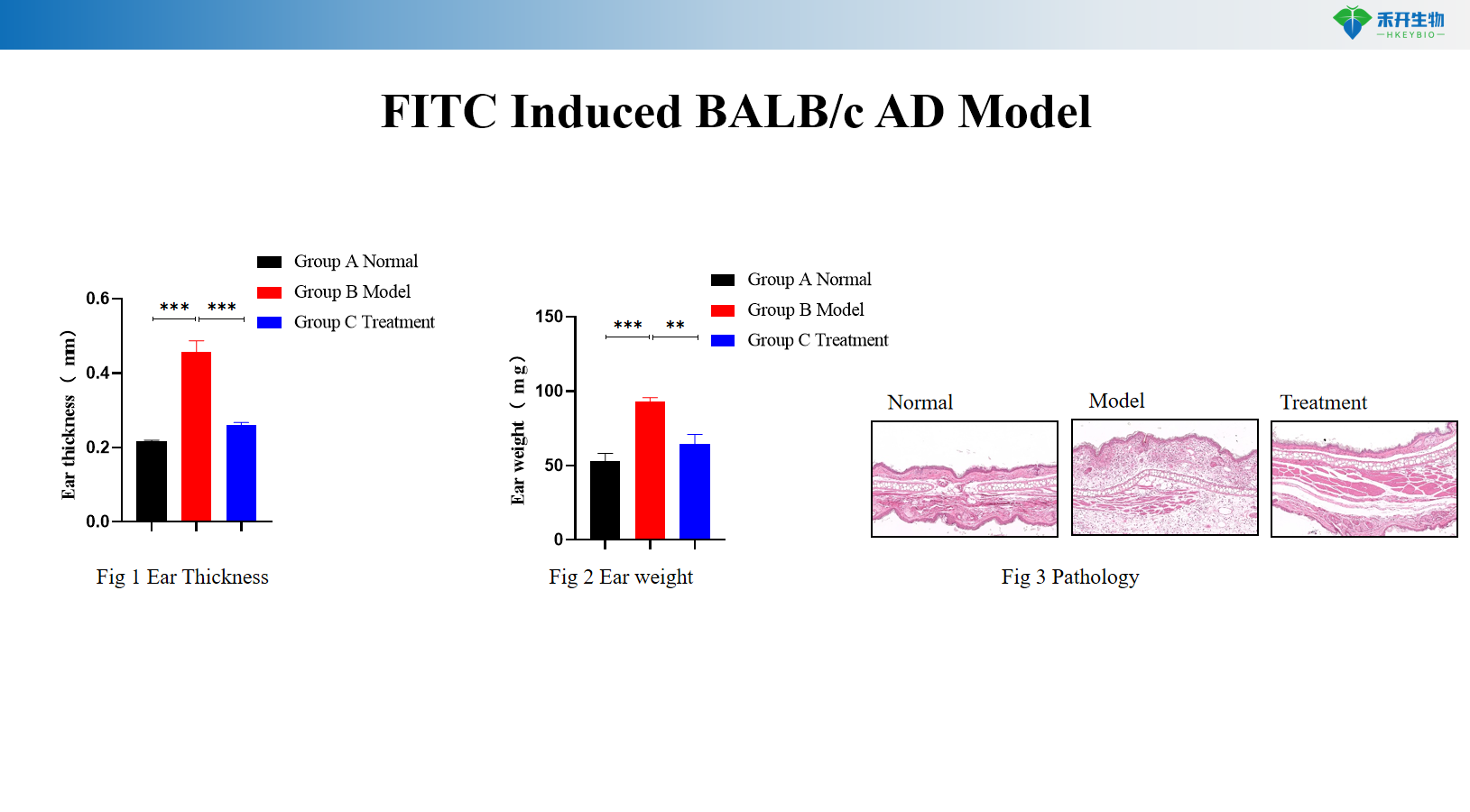
Modelo BALB/c AD induzido por DNFB + OVA
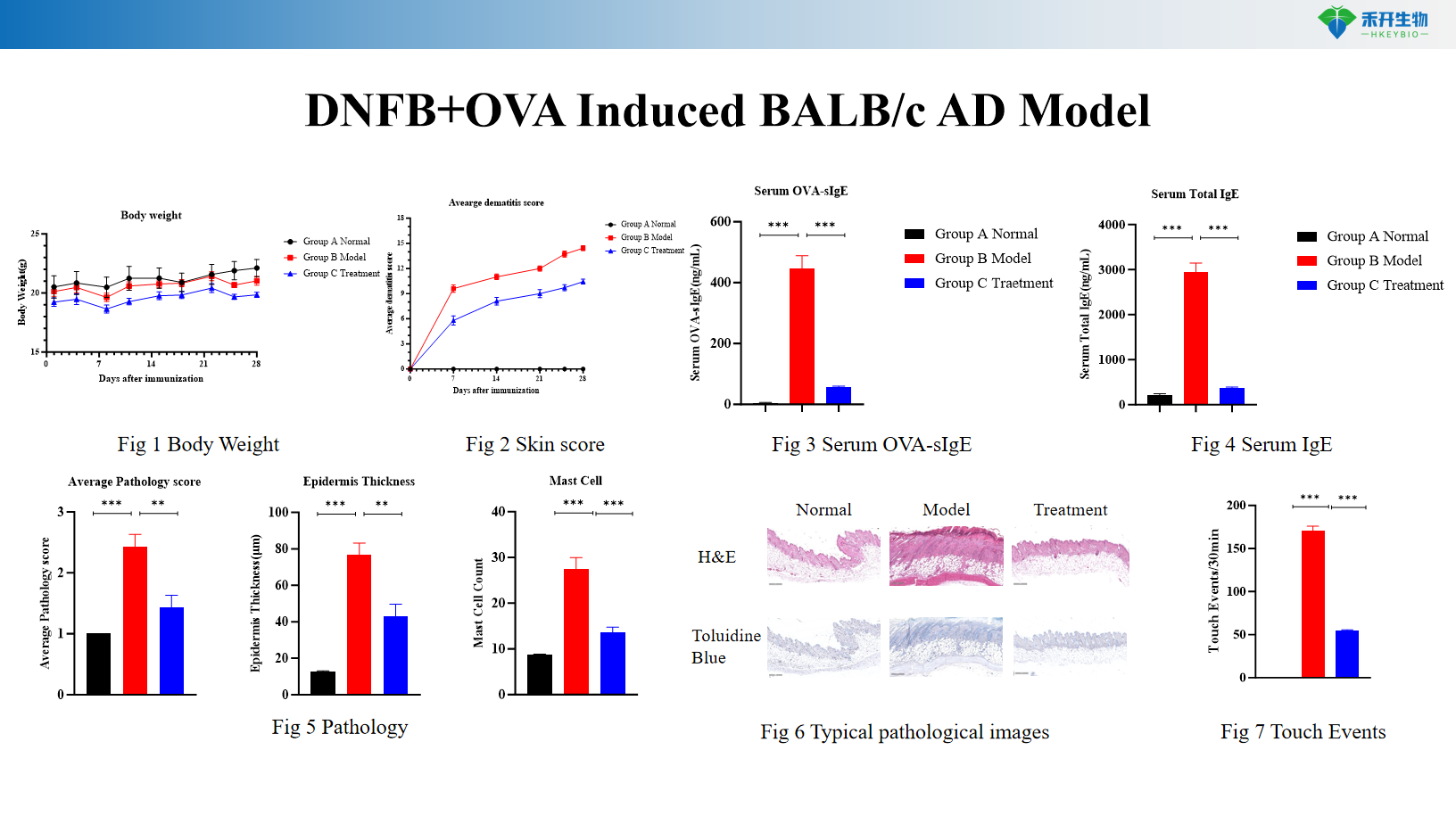
Modelo BALB/c AD induzido por IL-33
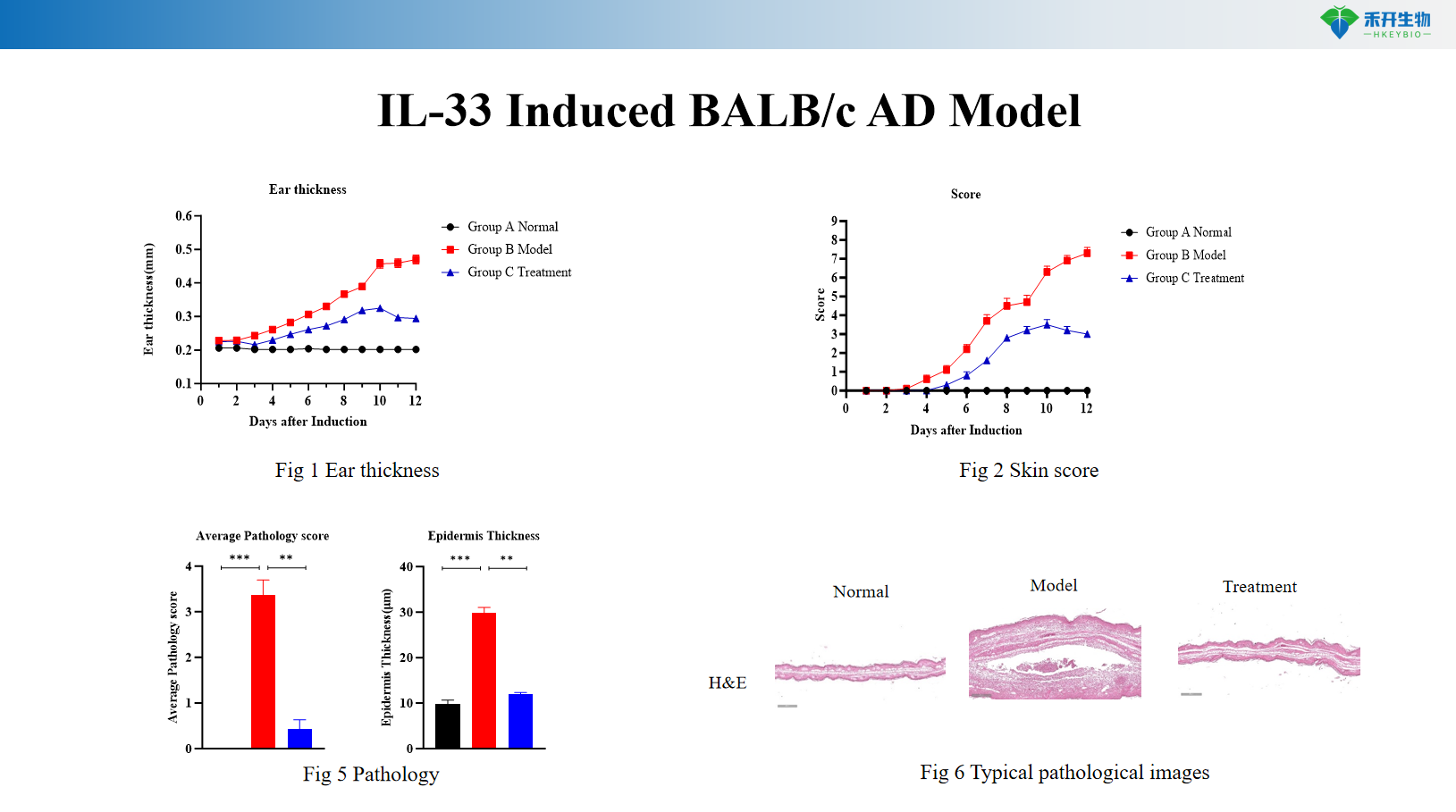
Modelo de AD induzido por IL-36 em camundongos C57BL/6
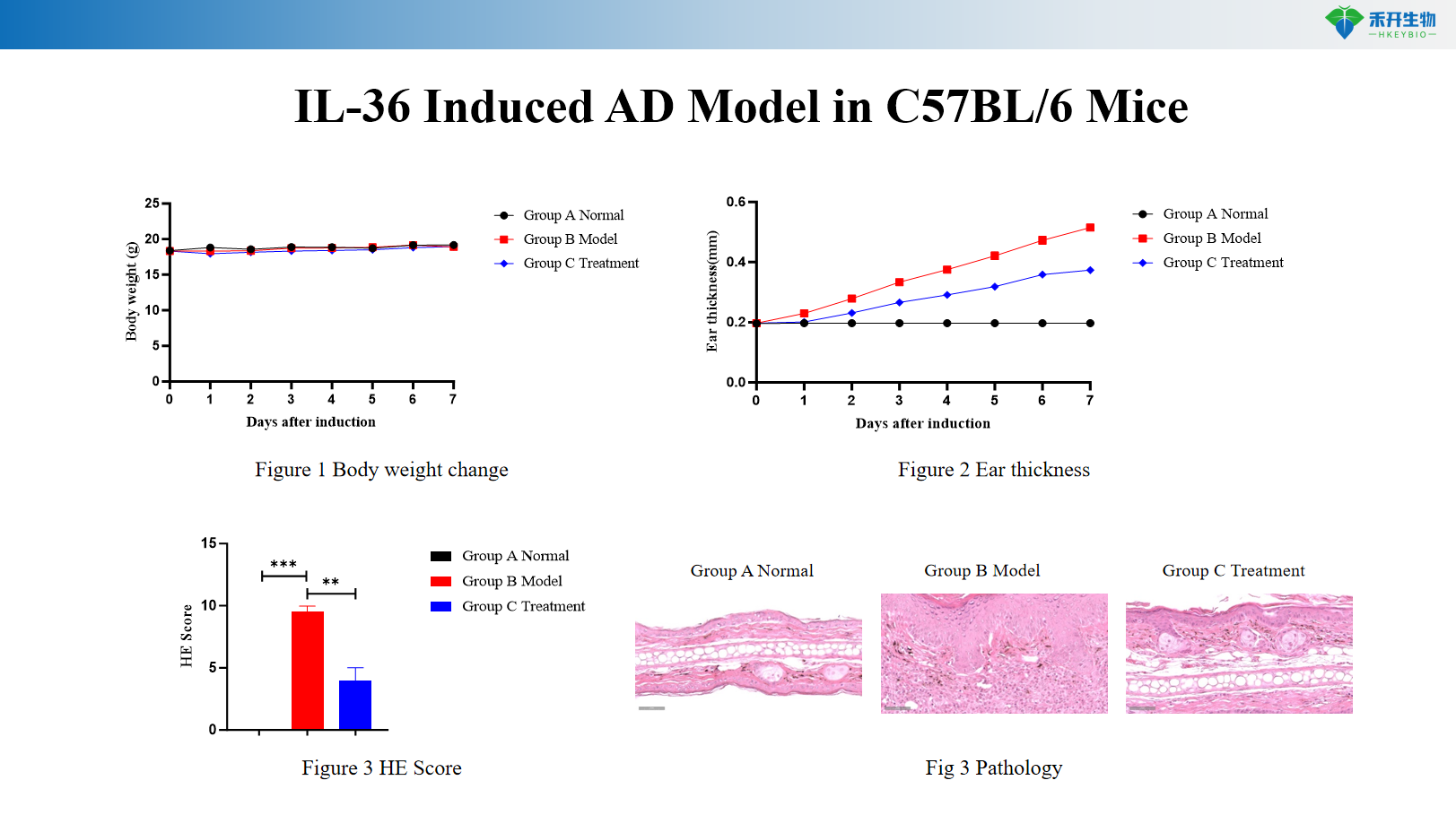
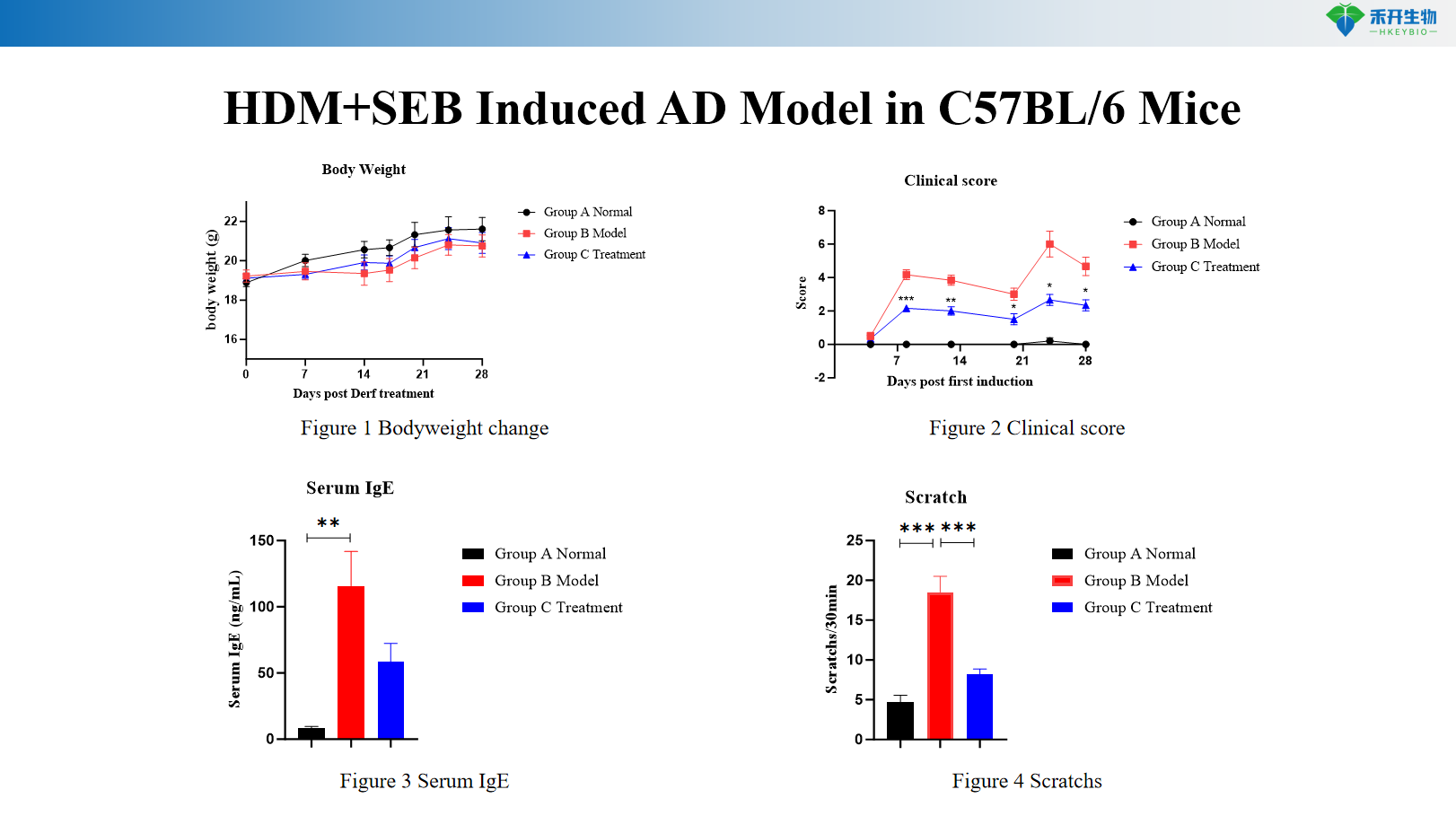
Modelo de AD induzido por HDM + SEB em camundongos C57BL/6
• Testes de eficácia de terapias tópicas e sistêmicas para DA (inibidores de JAK, inibidores de PDE4, produtos biológicos direcionados a IL-4/13, IL-31, IL-33, TSLP)
• Validação de alvo para Th2, Th17, Th22 e vias de coceira
• Descoberta de biomarcadores (IgE, assinaturas de citocinas, proteínas de barreira cutânea)
• Estudos de mecanismo de ação (MOA)
• Estudos de farmacologia e toxicologia que permitem o IND
Parâmetro |
Especificação |
Espécie/Estirpe |
Ratinho (BALB/c, C57BL/6); Rato (SD) |
Método de indução |
Haptenos (DNCB, OXA, DNFB+OVA, FITC), análogo da vitamina D (MC903), citocinas (IL‑33, IL‑36), alérgenos (HDM+SEB), combinações (MC903+OXA) |
Duração do estudo |
7–28 dias (dependendo do modelo) |
Principais pontos de extremidade |
Peso corporal, espessura da orelha, pontuação clínica da pele, eventos de coceira (coçar), IgE total sérica e IgE específica para antígeno, níveis de citocinas (IL-4, IL-13, IL-17, IL-36, TNF-α), histopatologia (H&E, azul de toluidina), espessura epidérmica, infiltração de células imunes (FACS/IHC) |
Pacote de dados |
Dados brutos, relatórios de análise, fotografias clínicas, lâminas histológicas, arquivos de citometria de fluxo, bioinformática (opcional) |
P: Como escolho o modelo de AD certo para o meu medicamento candidato?
R: Considere o mecanismo do seu medicamento: produtos biológicos direcionados a Th2 (por exemplo, anti-IL-4Rα) são melhor avaliados em modelos de hapteno ou MC903; Os compostos relacionados ao Th17 podem ser adequados para os modelos IL-36 ou HDM+SEB. Camundongos BALB/c exibem respostas Th2 mais fortes, enquanto C57BL/6 apresentam perfis Th1/Th17 mais equilibrados. Nossa equipe científica pode orientar a seleção do modelo com base no seu alvo específico.
P: Esses modelos podem ser usados para estudos de viabilização do IND?
R: Sim. Os estudos podem ser conduzidos de acordo com os princípios das BPL para submissões regulatórias (FDA, EMA).
P: Vocês oferecem protocolos de estudo personalizados (por exemplo, diferentes esquemas de dosagem, terapias combinadas)?
R: Absolutamente. Nossa equipe científica adapta protocolos de indução, cronogramas de tratamento e análises de desfechos para seu medicamento candidato específico.
P: Qual é o cronograma típico para um estudo piloto de eficácia?
R: A maioria dos modelos de DA são concluídos em 2–4 semanas, incluindo as fases de sensibilização/desafio e tratamento. Os prazos específicos dependem da escolha do modelo e dos pontos finais.
