| Ketersediaan: | |
|---|---|
| Kuantitas: | |











Relevansi klinis – Tinjauan patofisiologi asma manusia: hiperresponsif saluran napas, peradangan eosinofilik, peningkatan sitokin Th2.
Berbagai pilihan alergen – tersedia model induksi protein A.Suum dan HDM.
Titik akhir komposit – mencakup fungsi paru-paru (resistensi saluran napas), jumlah sel BALF, kadar IgE/IgG1, analisis histopatologi dan sitokin.
Paket Siap IND – Penelitian dapat dilakukan sesuai dengan prinsip GLP.
Protokol yang dapat disesuaikan – Menyesuaikan protokol sensitisasi, rencana tantangan, dan analisis titik akhir untuk kandidat obat Anda.
Data representatif dari model asma NHP kami:
A. Model asma NHP yang diinduksi Suum
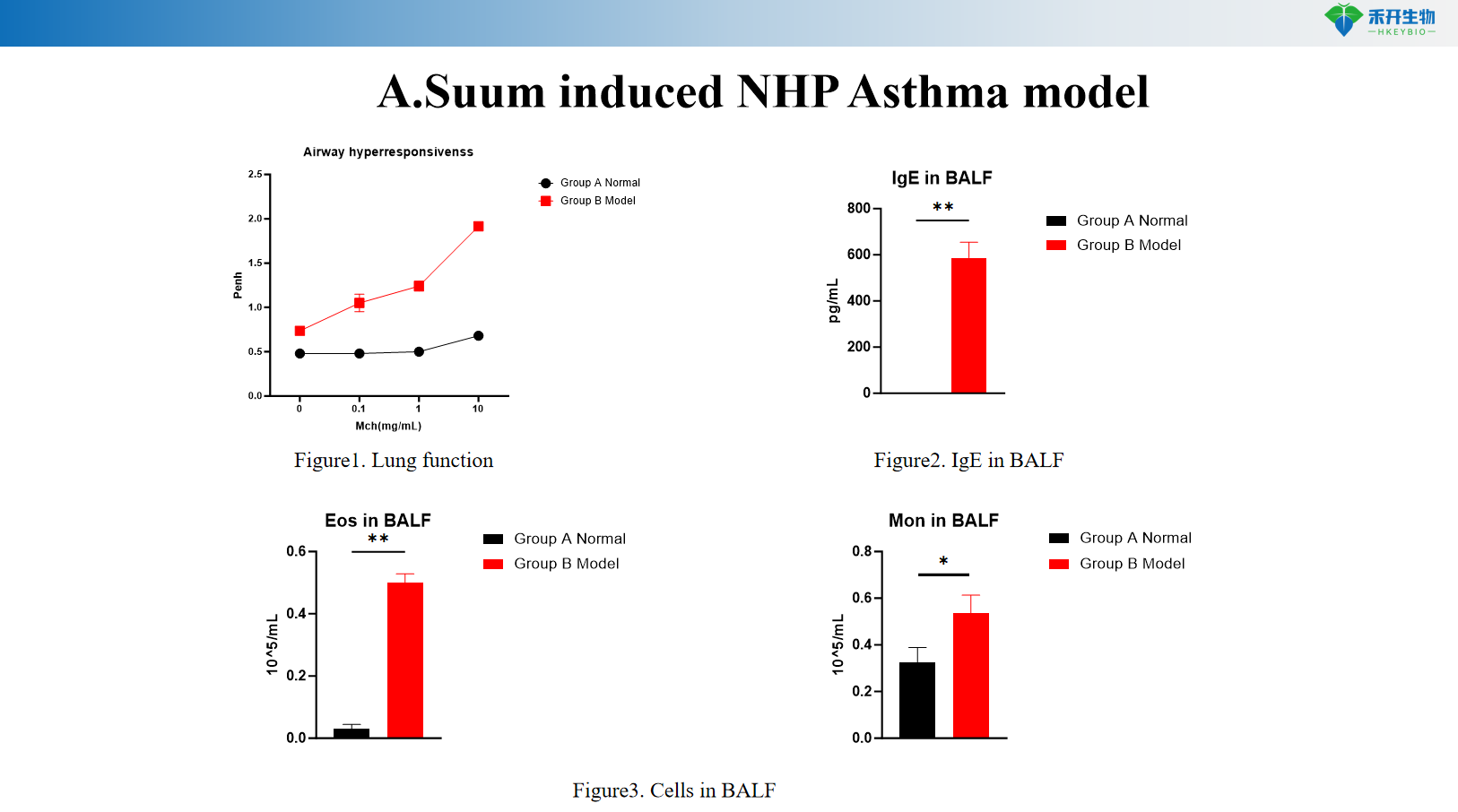
•
Model asma NHP yang diinduksi HDM
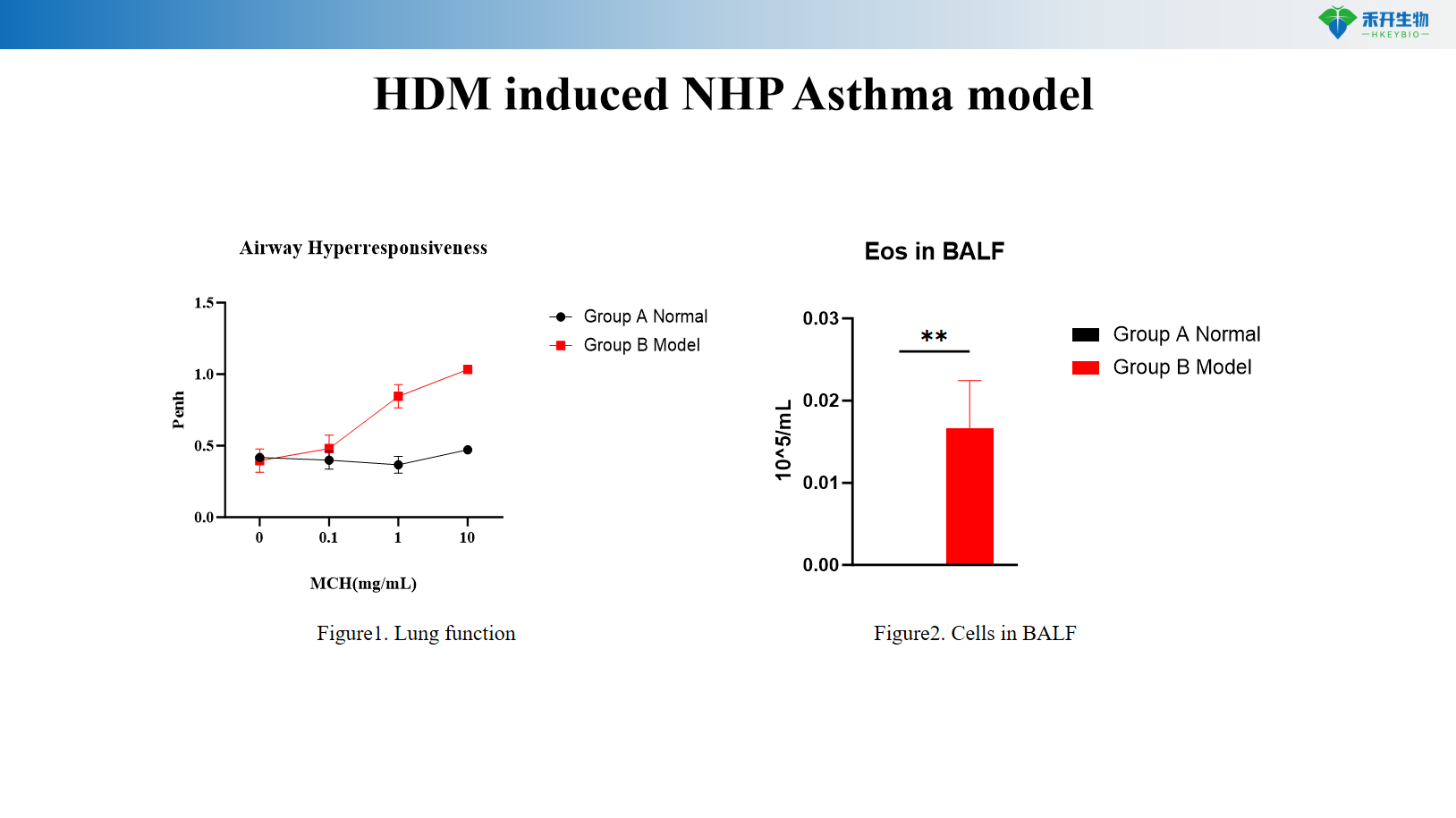
• Uji kemanjuran pengobatan asma (biologis, molekul kecil, obat inhalasi)
• Validasi target peradangan yang dipicu oleh Th2
• Penemuan dan validasi biomarker (eosinofil, IgE, sitokin)
• Studi toksikologi dan keamanan farmakologi untuk mendukung IND
• Investigasi Mekanisme Aksi (MOA).
cakupan |
A. Model induksi Suum |
Model yang diinduksi HDM |
Jenis |
Macaca fascicularis |
Macaca fascicularis |
metode induksi |
A.Suum protein + bahan pembantu tawas (sensitisasi sistemik) + A.Suum tantangan aerosol |
Ekstrak tungau debu rumah (HDM), sensitisasi dan tantangan intratrakeal atau aerosol |
waktu belajar |
8–12 minggu |
6–10 minggu |
titik akhir kritis |
Hiperresponsif saluran napas, eosinofil BALF, IgE, IL-4/5/13, histopatologi paru |
Hiperresponsif saluran napas, eosinofil BALF, IgE total dan IgE spesifik HDM, sitokin Th2, histopatologi paru |
paket |
Data mentah, laporan analisis, slide histologi, bioinformatika (opsional) |
T: Bagaimana model asma NHP diinduksi?
J: Ada dua model yang tersedia: protein A.Suum dengan bahan pembantu tawas (sensitisasi sistemik diikuti dengan tantangan aerosol) dan HDM (sensitisasi/tantangan intratrakeal atau aerosol). Keduanya menyebabkan peradangan saluran napas eosinofilik dan hiperresponsif.
T: Apakah model ini dapat digunakan untuk studi dukungan IND?
Jawaban: Ya. Kami dapat melakukan studi sesuai dengan prinsip GLP; paket data dirancang untuk mendukung pengajuan peraturan (FDA, EMA).
T: Apakah Anda menawarkan rencana penelitian yang disesuaikan?
Jawaban: Tentu saja. Tim ilmiah kami menyesuaikan protokol sensitisasi, rejimen pemberian dosis, dan analisis titik akhir untuk kandidat obat dan MOA Anda.
T: Apa jadwal umum untuk studi kemanjuran percontohan?
A: Studi percontohan (n=4-6/kelompok) dapat diselesaikan dalam 10-12 minggu dan mencakup sensitisasi, tantangan, pengobatan, dan analisis titik akhir.
