| Disponibilidad: | |
|---|---|
| Cantidad: | |











Clínicamente relevante : recapitula la TAO humana con hipertiroidismo, producción de TSAb, fibrosis orbitaria y patología ocular.
Impulsado por mecanismos : la expresión de hTSHR induce autoanticuerpos TSHR, imitando la patogénesis autoinmune de la TAO humana.
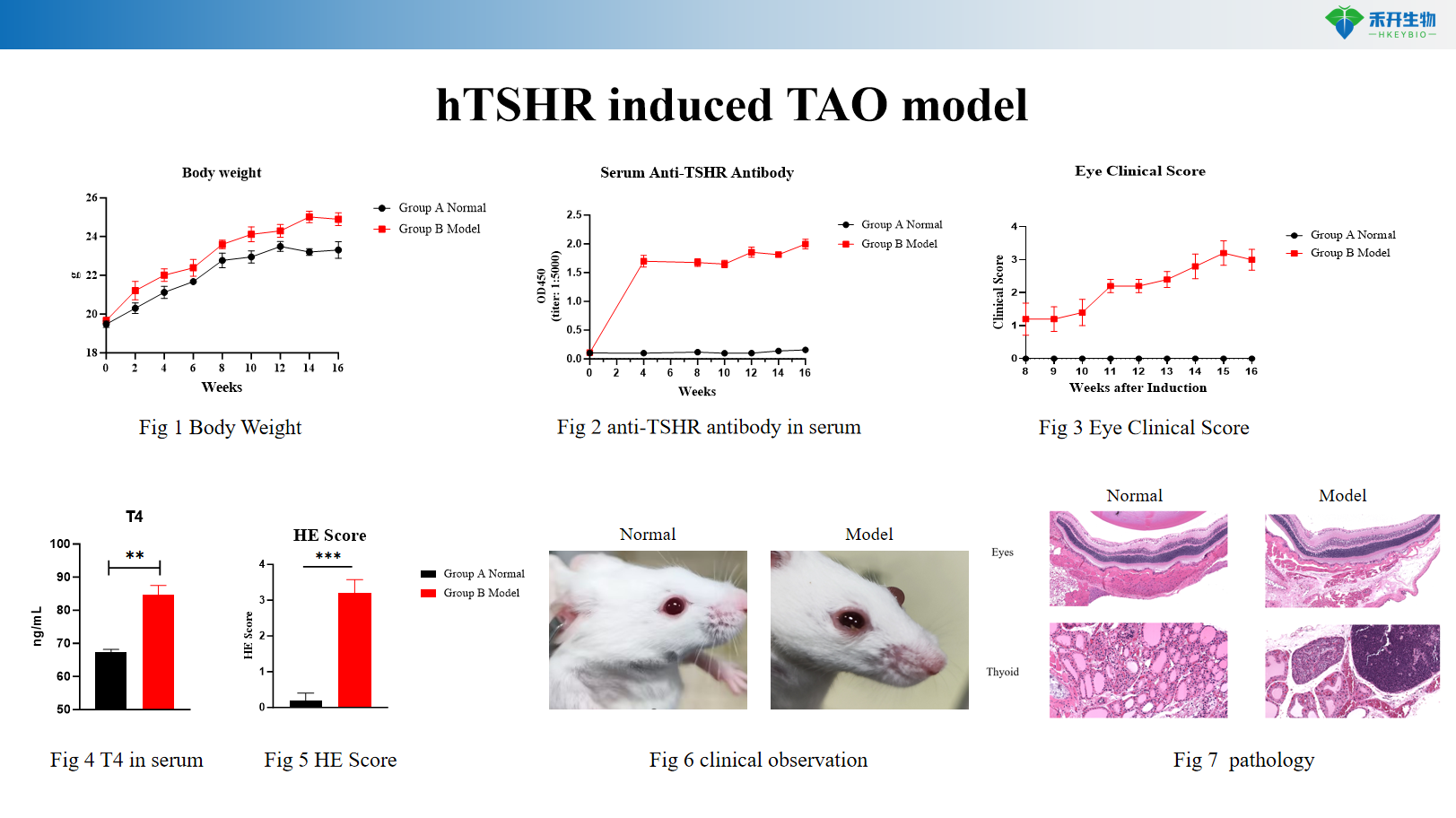
Criterios de valoración integrales : peso corporal, niveles séricos de T4 y TSAb, anticuerpos anti-TSHR, puntuación clínica ocular, histopatología orbitaria (HE), observación clínica.
Valor traslacional : ideal para probar antagonistas de TSHR, inmunomoduladores y terapias antiinflamatorias para TAO.
Paquetes de datos preparados para IND : los estudios se pueden realizar de acuerdo con los principios GLP.
Modelo TAO inducido por hTSHR
• Pruebas de eficacia de antagonistas de TSHR e inhibidores de moléculas pequeñas dirigidos a la señalización de TSHR
• Evaluación de inmunomoduladores (corticosteroides, rituximab, tocilizumab) para TAO
• Validación de objetivos para las vías de autoinmunidad TSHR y fibrosis orbitaria
• Descubrimiento de biomarcadores (TSAb, anticuerpos anti-TSHR, niveles de T4)
• Estudios de farmacología y toxicología que permitan el IND
Parámetro |
Especificación |
Especie/Cepa |
Ratón BALB/c |
Método de inducción |
Electroporación repetida (EP) de ADNc de TSHR humano en el músculo esquelético, normalmente de 4 a 6 inmunizaciones durante 8 a 12 semanas |
Duración del estudio |
8-16 semanas (fase de inducción + tratamiento) |
Puntos finales clave |
Peso corporal, niveles séricos de T4 (ELISA), TSAb sérico (anticuerpo estimulante de la tiroides), anticuerpos anti-TSHR, puntuación clínica ocular (escala de 0 a 4), histopatología del tejido orbitario (HE con puntuación de fibrosis), imágenes de observación clínica |
| control positivo | Corticosteroides (p. ej., prednisolona) o antagonistas de TSHR disponibles como compuestos de referencia |
Paquete de datos |
Datos brutos, informes de análisis, resultados de ELISA, portaobjetos de histología, fotografías clínicas, bioinformática (opcional) |
P: ¿Cómo induce la electroporación hTSHR la TAO en ratones?
R: La electroporación repetida del ADNc de TSHR humano en el tejido muscular impulsa la expresión persistente de la proteína TSHR, rompiendo la tolerancia inmune y generando autoanticuerpos TSHR (TSAb). Estos autoanticuerpos reaccionan de forma cruzada con el TSHR orbital, lo que induce inflamación, fibrosis y signos clínicos de TAO.
P: ¿Cuáles son las similitudes clave con la TAO humana?
R: El modelo exhibe hipertiroidismo (T4 elevado), producción de TSAb, anticuerpos anti-TSHR, fibrosis orbitaria y patología ocular (retracción del párpado, proptosis), lo que refleja fielmente la oftalmopatía de Graves humana.
P: ¿Se puede utilizar este modelo para estudios que permitan IND?
R: Sí. Los estudios se pueden realizar de acuerdo con los principios GLP para presentaciones regulatorias (FDA, EMA).
P: ¿Ofrecen protocolos de estudio personalizados (p. ej., diferentes regímenes de electroporación, tiempos de tratamiento)?
R: Absolutamente. Nuestro equipo científico adapta los protocolos de electroporación, los programas de tratamiento y los análisis de criterios de valoración a su fármaco candidato específico.
P: ¿Cuál es el cronograma típico para un estudio piloto de eficacia?
R: Los estudios suelen durar entre 12 y 16 semanas, incluidas entre 8 y 12 semanas de inducción y 4 semanas de tratamiento con análisis de criterios de valoración.
