| Tillgänglighet: | |
|---|---|
| Kvantitet: | |











Kliniskt relevant – Rekapitulerar mänsklig KOA: broskdegeneration, ledsvullnad och smärtrelaterade beteenden.
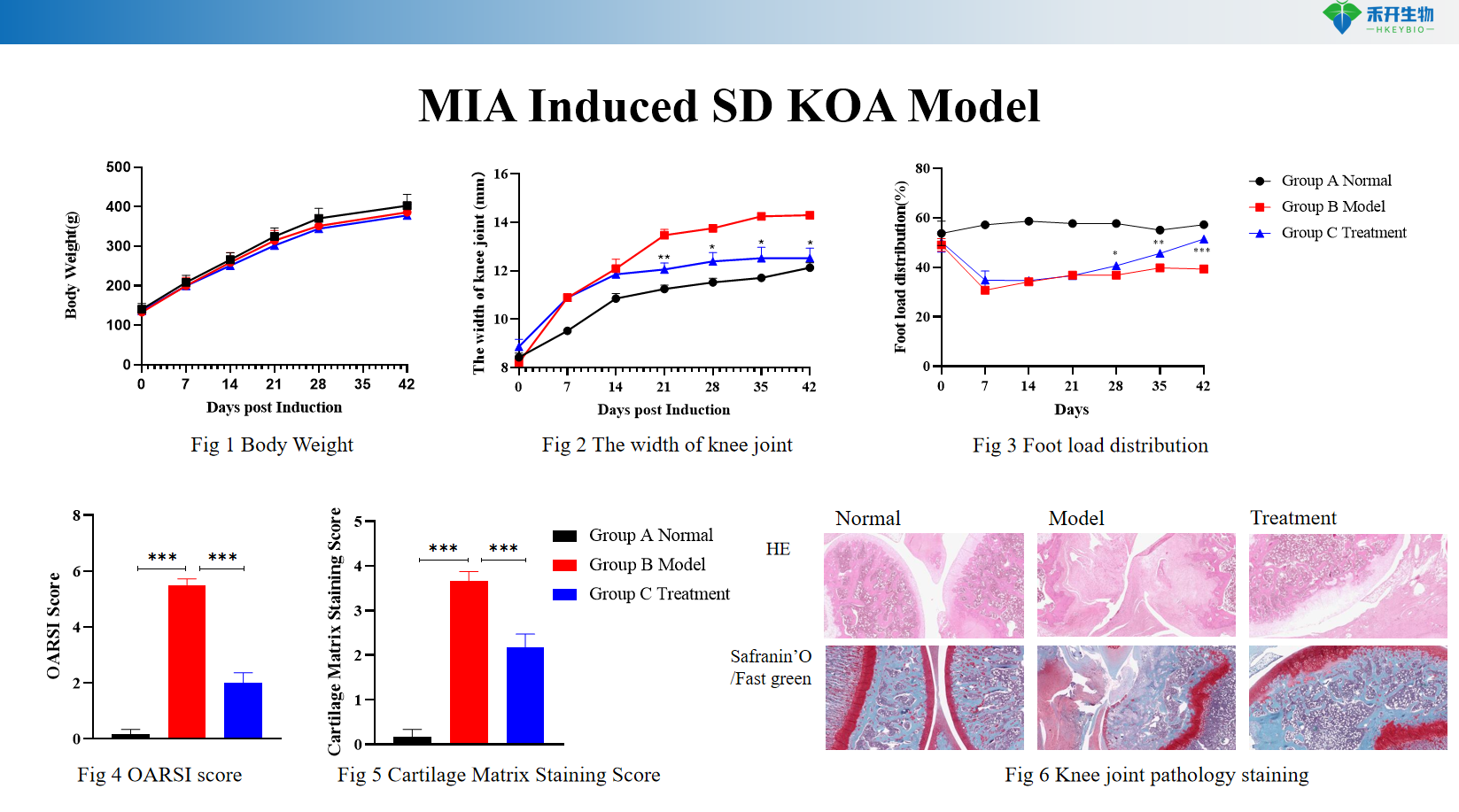
Kvantifierbara endpoints – Kroppsvikt, knäledsbredd (okmått), fotbelastningsfördelning (viktbärande asymmetri), broskmatrisfärgningspoäng (Safranin O/Snabbgrön), histopatologi (HE, toluidinblått).
Mekanismdriven – MIA hämmar kondrocytglykolys, inducerar apoptos och progressiv brosknedbrytning, efterliknar de metabola och strukturella förändringarna i artros.
Translationellt värde – Idealiskt för att testa sjukdomsmodifierande artrosläkemedel (DMOAD), smärtstillande medel (NSAID, opioider) och antiinflammatoriska medel.
IND-färdiga datapaket – Studier kan utföras i enlighet med GLP-principer.
MIA-inducerad SD KOA-modell
• Effekttester av sjukdomsmodifierande artrosläkemedel (DMOADs) inklusive cathepsin K-hämmare, Wnt pathway-modulatorer och anabola medel
• Utvärdering av analgetika (NSAID, COX-2-hämmare, opioider, cannabinoider) för artrossmärta
• Målvalidering för brosknedbrytning och smärtvägar
• Upptäckt av biomarkörer (markörer för nedbrytning av brosk, inflammatoriska mediatorer)
• IND-möjliggörande farmakologi och toxikologistudier
Parameter |
Specifikation |
Art/Stam |
Sprague-Dawley (SD) råtta |
Induktionsmetod |
Intraartikulär injektion av monojodacetat (MIA, 1–3 mg i 50 μL koksaltlösning) i knäleden |
Studietid |
1–8 veckor (akuta till kroniska faser) |
Viktiga slutpunkter |
Kroppsvikt, knäledsbredd (ok), fotbelastningsfördelning (viktbärande asymmetri), broskmatrisfärgningspoäng (Safranin O/Fast green), histopatologi (HE, toluidinblått, OARSI-poäng), valfritt: mekanisk allodyni (von Frey), gånganalys, serumbiomarkörer (IIP), |
| Positiv kontroll | NSAID (t.ex. indometacin) eller DMOAD tillgängliga som referensföreningar |
Datapaket |
Rådata, analysrapporter, histologibilder, beteendedata, bioinformatik (valfritt) |
F: Hur inducerar MIA artros?
S: Monojodoacetat (MIA) hämmar glyceraldehyd-3-fosfatdehydrogenas, ett nyckelenzym i glykolys, vilket leder till metabolisk störning av kondrocyter och apoptos. Detta utlöser progressiv brosknedbrytning, subkondrala benförändringar och smärtbeteenden som nära efterliknar mänsklig artros.
F: Vilka är de viktigaste likheterna med mänsklig knäartros?
S: Modellen uppvisar broskmatrisförlust, ledsvullnad, förändrad viktbärande och histopatologiska förändringar (flimmer, kondrocytförlust, subkondral benskleros), som nära återspeglar mänsklig KOA-patologi och smärtrelaterade funktionella brister.
F: Kan den här modellen användas för IND-aktiverande studier?
A: Ja. Studier kan utföras i enlighet med GLP-principer för regulatoriska inlämningar (FDA, EMA).
F: Erbjuder du skräddarsydda studieprotokoll (t.ex. olika MIA-doser, profylaktisk kontra terapeutisk dosering)?
A: Absolut. Vårt forskarteam skräddarsyr MIA-doser, behandlingsscheman och slutpunktsanalyser för din specifika läkemedelskandidat.
F: Vilken är den typiska tidslinjen för en pilotstudie om effektivitet?
S: Studier av akut smärta kan slutföras på 1–2 veckor; kroniska strukturella studier kräver vanligtvis 4–8 veckor efter MIA-injektion.
