| Dostępność: | |
|---|---|
| Ilość: | |











Klinicznie istotne – podsumowuje ludzkie KOA: zwyrodnienie chrząstki, obrzęk stawów i zachowania związane z bólem.
Wymierne punkty końcowe – masa ciała, szerokość stawu kolanowego (pomiar suwmiarką), rozkład obciążenia stopy (asymetria obciążenia), wynik barwienia macierzy chrząstki (Safranin O/Fast green), histopatologia (HE, błękit toluidynowy).
Oparta na mechanizmach – MIA hamuje glikolizę chondrocytów, indukując apoptozę i postępującą degradację chrząstki, naśladując zmiany metaboliczne i strukturalne w chorobie zwyrodnieniowej stawów.
Wartość translacyjna – Idealny do testowania leków modyfikujących przebieg choroby zwyrodnieniowej stawów (DMOAD), leków przeciwbólowych (NLPZ, opioidy) i środków przeciwzapalnych.
Pakiety danych gotowe do IND – Badania mogą być prowadzone zgodnie z zasadami GLP.
Model SD KOA indukowany MIA
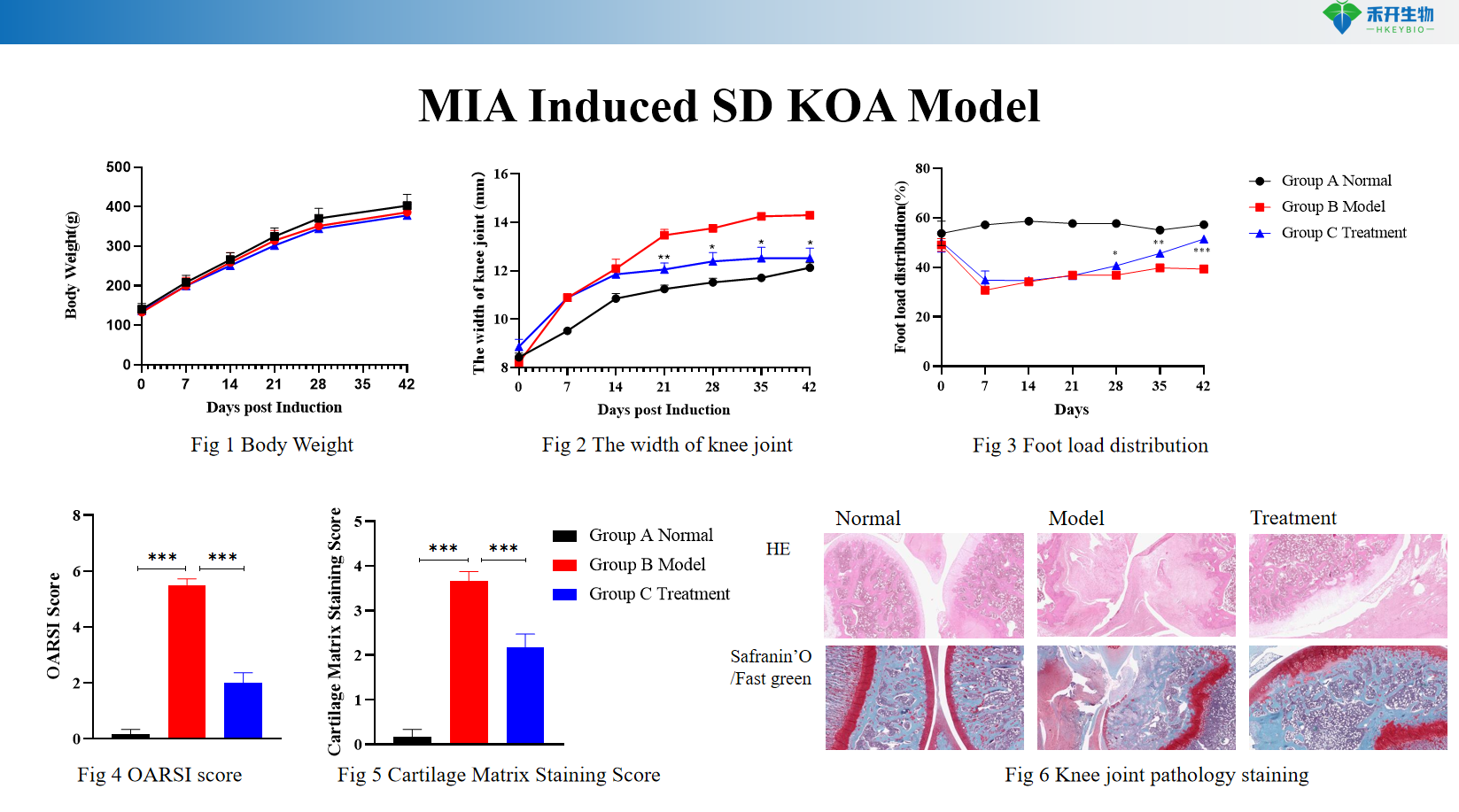
• Testowanie skuteczności leków modyfikujących przebieg choroby zwyrodnieniowej stawów (DMOAD), w tym inhibitorów katepsyny K, modulatorów szlaku Wnt i środków anabolicznych
• Ocena leków przeciwbólowych (NLPZ, inhibitory COX-2, opioidy, kannabinoidy) w leczeniu bólu związanego z chorobą zwyrodnieniową stawów
• Docelowa walidacja degradacji chrząstki i ścieżek bólowych
• Odkrycie biomarkerów (markery degradacji chrząstki, mediatory stanu zapalnego)
• Badania farmakologiczne i toksykologiczne umożliwiające IND
Parametr |
Specyfikacja |
Gatunek/szczep |
Szczur Sprague-Dawley (SD). |
Metoda indukcyjna |
Śródstawowe wstrzyknięcie monojodooctanu (MIA, 1–3 mg w 50 µl soli fizjologicznej) do stawu kolanowego |
Czas trwania nauki |
1–8 tygodni (faza ostra do przewlekłej) |
Kluczowe punkty końcowe |
Masa ciała, szerokość stawu kolanowego (suwmiarka), rozkład obciążenia stopy (asymetria obciążenia), wynik barwienia macierzy chrząstki (Safranin O/Fast green), histopatologia (HE, błękit toluidynowy, punktacja OARSI), opcjonalnie: allodynia mechaniczna (von Freya), analiza chodu, biomarkery surowicy (COMP, CTX-II) |
| Pozytywna kontrola | NLPZ (np. indometacyna) lub DMOAD dostępne jako związki referencyjne |
Pakiet danych |
Surowe dane, raporty z analiz, slajdy histologiczne, dane behawioralne, bioinformatyka (opcjonalnie) |
P: W jaki sposób MIA wywołuje chorobę zwyrodnieniową stawów?
Odp.: Monojodooctan (MIA) hamuje dehydrogenazę gliceraldehydo-3-fosforanu, kluczowy enzym w glikolizie, prowadzący do zaburzeń metabolicznych chondrocytów i apoptozy. Powoduje to postępującą degradację chrząstki, zmiany w kościach podchrzęstnych i zachowania bólowe, które bardzo naśladują ludzką chorobę zwyrodnieniową stawów.
P: Jakie są kluczowe podobieństwa z chorobą zwyrodnieniową stawu kolanowego u człowieka?
Odp.: Model wykazuje utratę macierzy chrząstki, obrzęk stawów, zmienione obciążenie i zmiany histopatologiczne (migotanie, utrata chondrocytów, stwardnienie podchrzęstne kości), ściśle odzwierciedlające patologię ludzkiego KOA i deficyty funkcjonalne związane z bólem.
P: Czy ten model można wykorzystać do badań umożliwiających IND?
O: Tak. Badania można przeprowadzić zgodnie z zasadami GLP dotyczącymi zgłoszeń regulacyjnych (FDA, EMA).
P: Czy oferujecie niestandardowe protokoły badań (np. różne dawki MIA, dawkowanie profilaktyczne i terapeutyczne)?
O: Absolutnie. Nasz zespół naukowy dostosowuje dawki MIA, harmonogramy leczenia i analizy punktów końcowych do konkretnego kandydata na lek.
P: Jaki jest typowy harmonogram pilotażowego badania skuteczności?
Odp.: Badania dotyczące bólu ostrego można zakończyć w ciągu 1–2 tygodni; przewlekłe badania strukturalne zazwyczaj wymagają 4–8 tygodni po wstrzyknięciu MIA.
