| Beschikbaarheid: | |
|---|---|
| Aantal: | |











Klinisch relevant – Recapituleert menselijke KOA: kraakbeendegeneratie, gewrichtszwelling en pijngerelateerd gedrag.
Kwantificeerbare eindpunten – Lichaamsgewicht, breedte van het kniegewricht (meting van de remklauw), verdeling van de voetbelasting (gewichtsdragende asymmetrie), score voor kleuring van de kraakbeenmatrix (Safranin O/Fast groen), histopathologie (HE, toluïdineblauw).
Mechanismegestuurd – MIA remt de glycolyse van chondrocyten, waardoor apoptose en progressieve afbraak van kraakbeen worden geïnduceerd, waardoor de metabolische en structurele veranderingen bij artrose worden nagebootst.
Translationele waarde – Ideaal voor het testen van ziektemodificerende geneesmiddelen tegen artrose (DMOAD’s), analgetica (NSAID’s, opioïden) en ontstekingsremmende middelen.
IND-ready datapakketten – Onderzoeken kunnen worden uitgevoerd volgens GLP-principes.
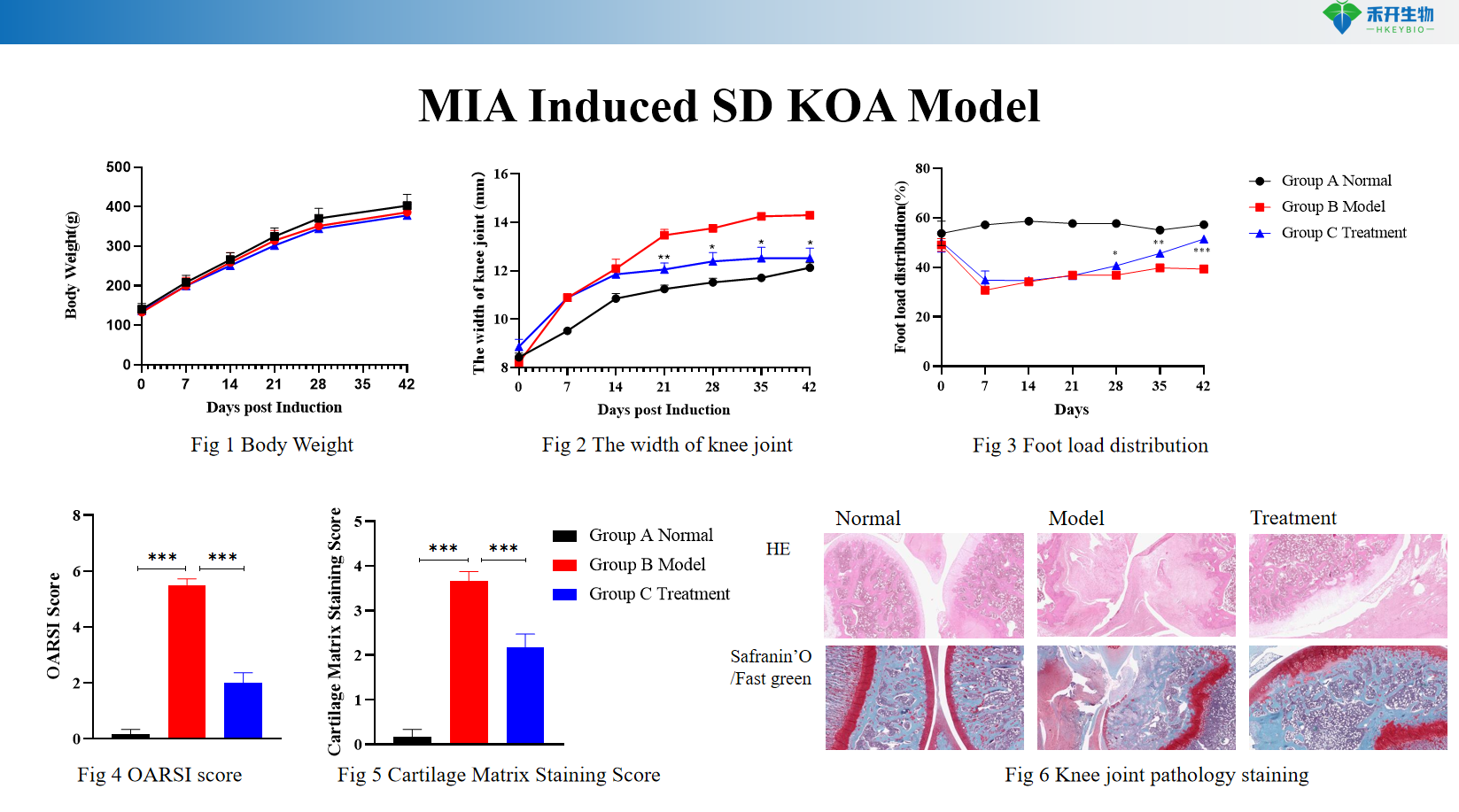
MIA-geïnduceerd SD KOA-model
• Werkzaamheidstesten van ziektemodificerende geneesmiddelen tegen artrose (DMOADs), waaronder cathepsine K-remmers, Wnt-routemodulatoren en anabole middelen
• Evaluatie van analgetica (NSAID's, COX-2-remmers, opioïden, cannabinoïden) voor pijn bij artrose
• Doelvalidatie voor kraakbeenafbraak en pijnpaden
• Ontdekking van biomarkers (markers voor afbraak van kraakbeen, ontstekingsmediatoren)
• Farmacologische en toxicologische onderzoeken die IND mogelijk maken
Parameter |
Specificatie |
Soort/stam |
Sprague-Dawley (SD) rat |
Inductiemethode |
Intra-articulaire injectie van monojoodacetaat (MIA, 1-3 mg in 50 μl zoutoplossing) in het kniegewricht |
Studieduur |
1–8 weken (acute tot chronische fasen) |
Belangrijkste eindpunten |
Lichaamsgewicht, breedte van het kniegewricht (remklauw), verdeling van de voetbelasting (gewichtdragende asymmetrie), kraakbeenmatrixkleuringscore (Safranin O/Fast green), histopathologie (HE, toluidineblauw, OARSI-score), optioneel: mechanische allodynie (von Frey), loopanalyse, serumbiomarkers (COMP, CTX-II) |
| Positieve controle | NSAID's (bijv. indomethacine) of DMOAD's beschikbaar als referentieverbindingen |
Datapakket |
Ruwe gegevens, analyserapporten, histologiedia's, gedragsgegevens, bio-informatica (optioneel) |
Vraag: Hoe veroorzaakt MIA artrose?
A: Monojoodacetaat (MIA) remt glyceraldehyde-3-fosfaatdehydrogenase, een sleutelenzym bij de glycolyse, wat leidt tot verstoring van de metabolische chondrocyten en apoptose. Dit veroorzaakt een progressieve afbraak van het kraakbeen, veranderingen in het subchondrale bot en pijngedrag dat sterk lijkt op menselijke artrose.
Vraag: Wat zijn de belangrijkste overeenkomsten met artrose van de menselijke knie?
A: Het model vertoont verlies van kraakbeenmatrix, zwelling van de gewrichten, veranderde gewichtsbelasting en histopathologische veranderingen (fibrillatie, verlies van chondrocyten, subchondrale botsclerose), wat nauw aansluit bij de menselijke KOA-pathologie en pijngerelateerde functionele tekorten.
Vraag: Kan dit model worden gebruikt voor onderzoeken die de IND mogelijk maken?
EEN: Ja. Studies kunnen worden uitgevoerd in overeenstemming met de GLP-principes voor indieningen bij de regelgevende instanties (FDA, EMA).
Vraag: Biedt u op maat gemaakte onderzoeksprotocollen aan (bijvoorbeeld verschillende MIA-doses, profylactische versus therapeutische dosering)?
EEN: Absoluut. Ons wetenschappelijk team stemt MIA-doses, behandelschema's en eindpuntanalyses af op uw specifieke kandidaat-geneesmiddel.
Vraag: Wat is de typische tijdlijn voor een pilotstudie naar de werkzaamheid?
A: Onderzoek naar acute pijn kan binnen 1 à 2 weken worden afgerond; Bij chronische structurele onderzoeken is doorgaans 4 tot 8 weken na de MIA-injectie nodig.
