| Tilgjengelighet: | |
|---|---|
| Antall: | |











Klinisk relevant – Rekapitulerer menneskelig KOA: bruskdegenerasjon, leddhevelse og smerterelatert atferd.
Kvantifiserbare endepunkter – Kroppsvekt, kneleddsbredde (calipermåling), fotbelastningsfordeling (vektbærende asymmetri), bruskmatrisefargingsscore (Safranin O/Fast green), histopatologi (HE, toluidinblått).
Mekanismedrevet – MIA hemmer kondrocyttglykolyse, induserer apoptose og progressiv brusknedbrytning, og etterligner metabolske og strukturelle endringer i slitasjegikt.
Translasjonsverdi – Ideell for testing av sykdomsmodifiserende artrosemedisiner (DMOADs), smertestillende (NSAIDs, opioider) og antiinflammatoriske midler.
IND-klare datapakker – Studier kan utføres i henhold til GLP-prinsipper.
MIA-indusert SD KOA-modell
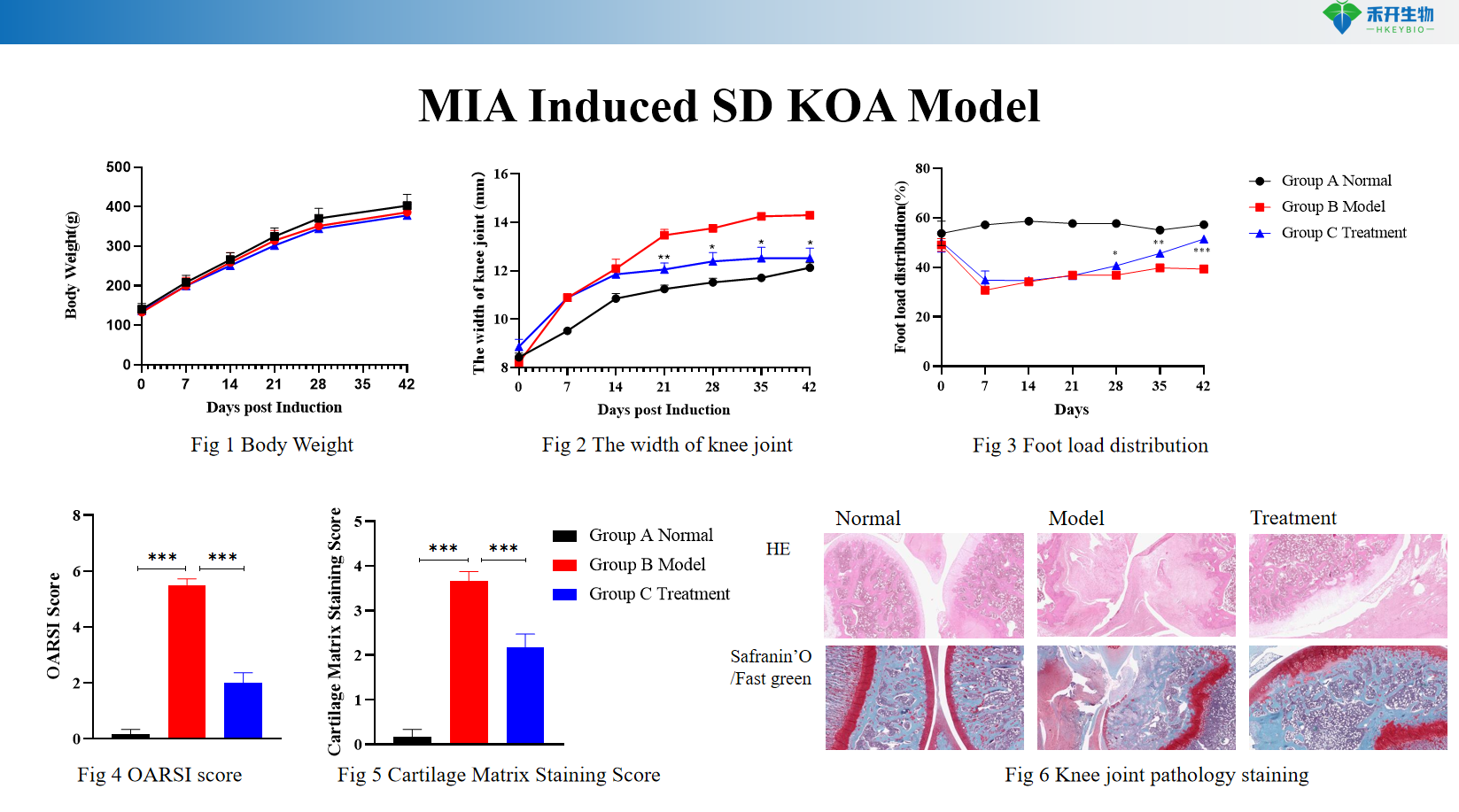
• Effekttesting av sykdomsmodifiserende osteoartrittmedisiner (DMOADs) inkludert cathepsin K-hemmere, Wnt-banemodulatorer og anabole midler
• Evaluering av analgetika (NSAIDs, COX-2-hemmere, opioider, cannabinoider) for slitasjegiktsmerter
• Målvalidering for bruskdegradering og smerteveier
• Biomarkørfunn (markører for brusknedbrytning, inflammatoriske mediatorer)
• IND-aktiverende farmakologi og toksikologistudier
Parameter |
Spesifikasjon |
Arter/Stamme |
Sprague-Dawley (SD) rotte |
Induksjonsmetode |
Intraartikulær injeksjon av monojodacetat (MIA, 1–3 mg i 50 μL saltvann) i kneleddet |
Studievarighet |
1–8 uker (akutte til kroniske faser) |
Viktige endepunkter |
Kroppsvekt, kneleddsbredde (caliper), fotbelastningsfordeling (vektbærende asymmetri), bruskmatrisefargingsscore (Safranin O/Fast green), histopatologi (HE, toluidinblått, OARSI-score), valgfritt: mekanisk allodyni (von Frey), ganganalyse, serumbiomarkører (COMP), |
| Positiv kontroll | NSAIDs (f.eks. indometacin) eller DMOADs tilgjengelig som referanseforbindelser |
Datapakke |
Rådata, analyserapporter, histologiske lysbilder, atferdsdata, bioinformatikk (valgfritt) |
Spørsmål: Hvordan induserer MIA slitasjegikt?
A: Monoiodoacetate (MIA) hemmer glyceraldehyd-3-fosfatdehydrogenase, et nøkkelenzym i glykolyse, som fører til kondrocyttmetabolsk forstyrrelse og apoptose. Dette utløser progressiv brusknedbrytning, subkondrale beinforandringer og smerteatferd som tett etterligner menneskelig slitasjegikt.
Spørsmål: Hva er de viktigste likhetene med menneskelig kneartrose?
A: Modellen viser bruskmatrisetap, leddhevelse, endret vektbærende og histopatologiske endringer (flimmer, kondrocyttap, subkondral bensklerose), som tett gjenspeiler menneskelig KOA-patologi og smerterelaterte funksjonsdefekter.
Spørsmål: Kan denne modellen brukes til IND-aktiverende studier?
A: Ja. Studier kan utføres i samsvar med GLP-prinsipper for regulatoriske innleveringer (FDA, EMA).
Spørsmål: Tilbyr du tilpassede studieprotokoller (f.eks. forskjellige MIA-doser, profylaktisk vs. terapeutisk dosering)?
A: Absolutt. Vårt vitenskapelige team skreddersyr MIA-doser, behandlingsplaner og endepunktsanalyser til din spesifikke legemiddelkandidat.
Spørsmål: Hva er den typiske tidslinjen for en piloteffektstudie?
A: Akutt smertestudier kan fullføres på 1–2 uker; kroniske strukturelle studier krever vanligvis 4–8 uker etter MIA-injeksjon.
