| Beschikbaarheid: | |
|---|---|
| Aantal: | |











Brede ziektedekking – Xenogene (menselijke PBMC), allogene MHC-niet-overeenkomende acute en chronische lupusachtige GVHD-modellen beschikbaar.
Kwantificeerbare eindpunten – Lichaamsgewicht, overlevingspercentage, klinische GVHD-score (schaal 0-10 met houding, activiteit, vacht, huid), auto-antilichamen in serum (anti-dsDNA, IgG), proteïnurie, histopathologie.
Mechanismegestuurd – Menselijk PBMC-model voor mensspecifieke therapieën; allogene modellen voor T-cel-gemedieerde GVHD; chronisch model voor auto-antilichaam-gemedieerde pathologie.
Translationele waarde – Ideaal voor het testen van immunosuppressiva (calcineurineremmers, mTOR-remmers), biologische geneesmiddelen (anti-TNF, anti-IL-6R) en celgebaseerde therapieën.
IND-ready datapakketten – Onderzoeken kunnen worden uitgevoerd volgens GLP-principes.
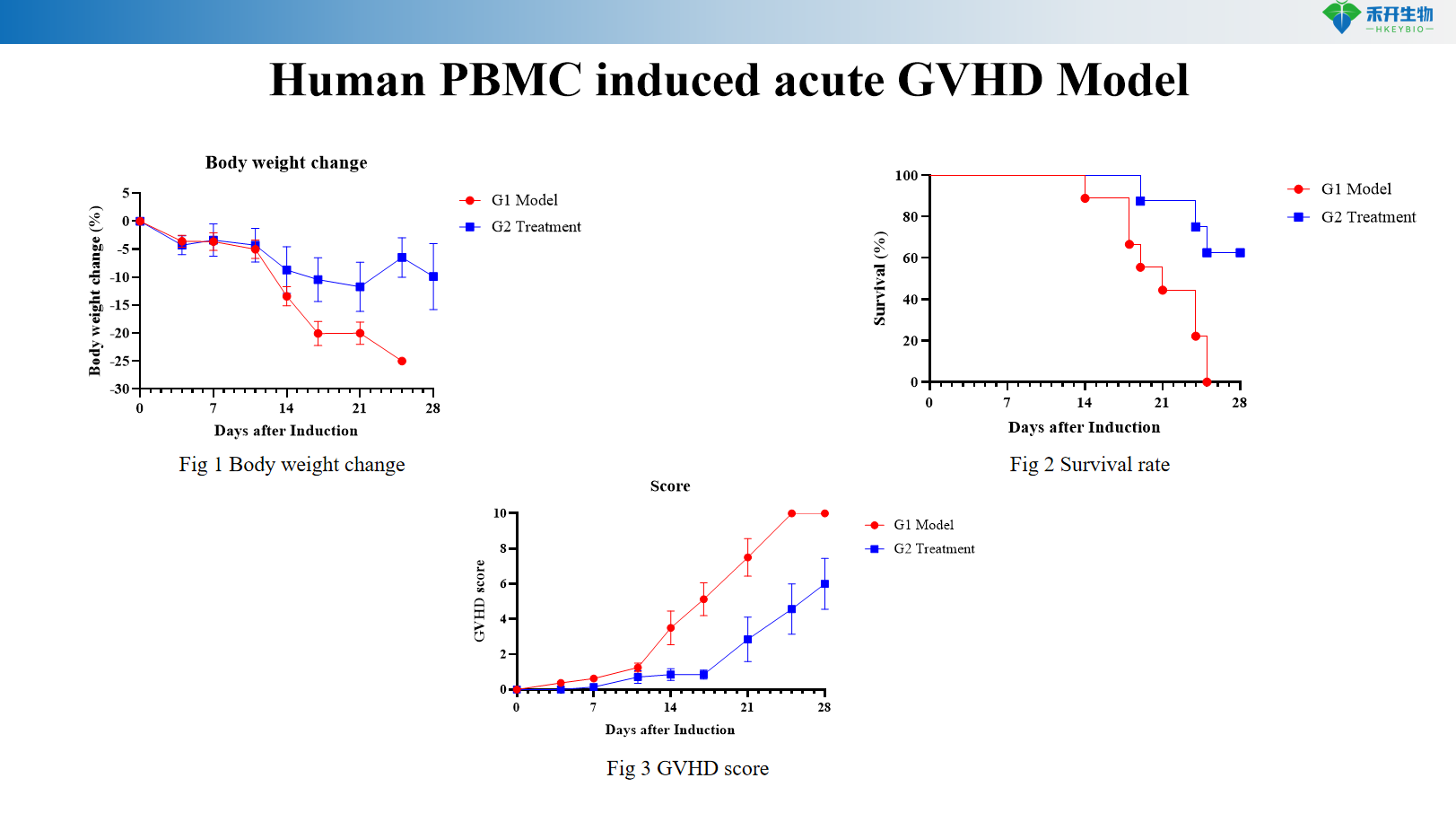
Menselijk PBMC induceerde acuut GVHD-model
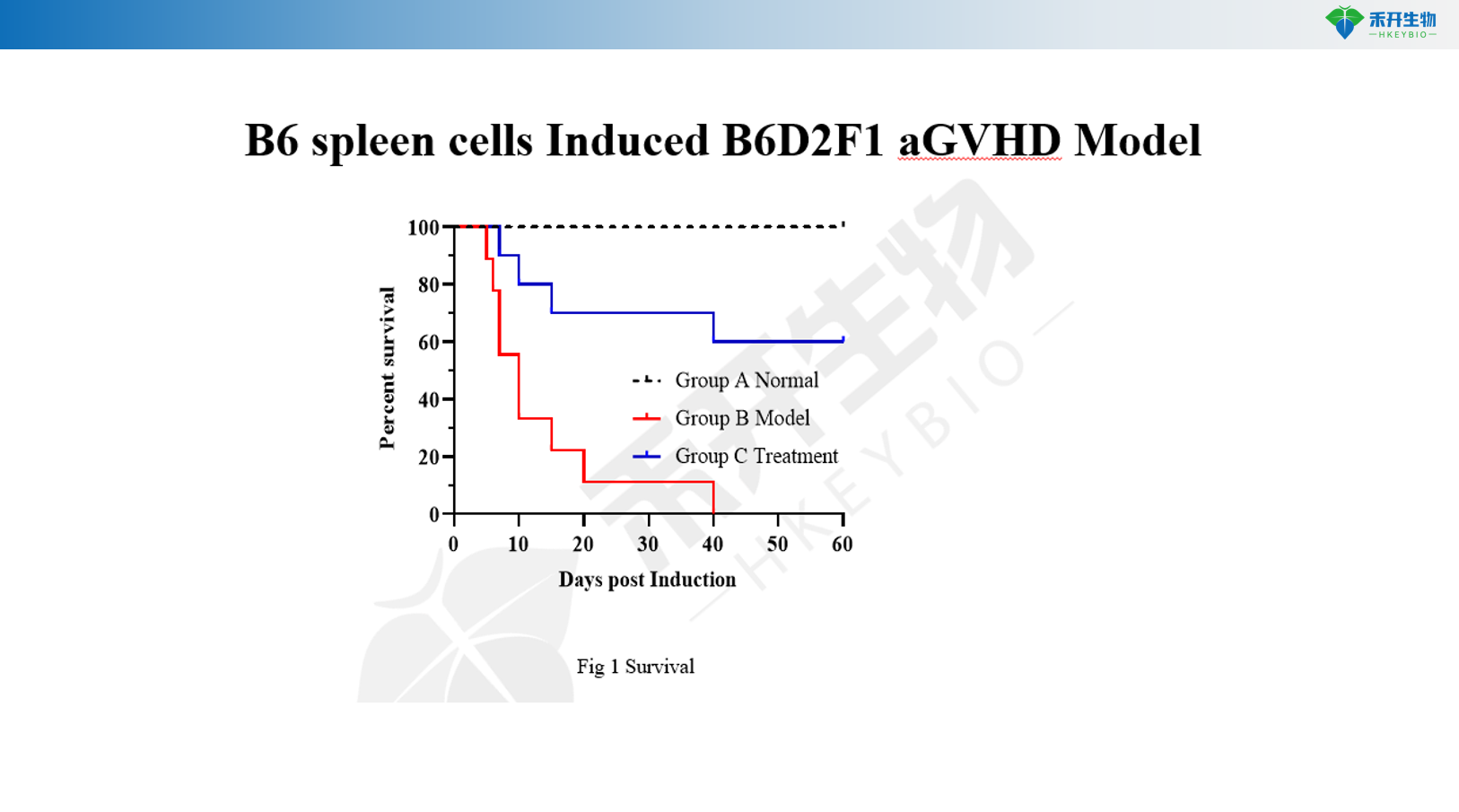
B6 miltcellen Geïnduceerd B6D2F1 aGVHD-model
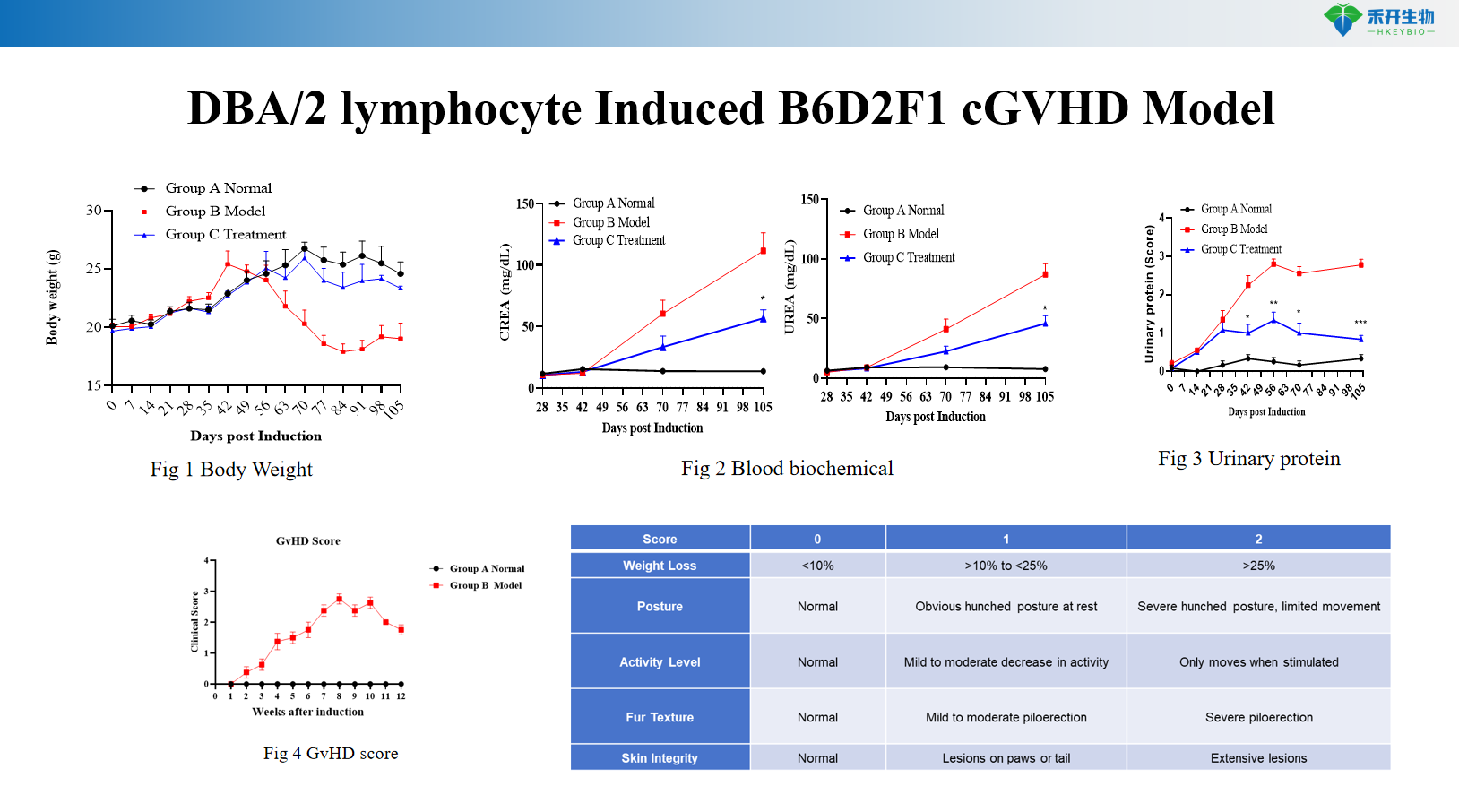
DBA/2 lymfocyt-geïnduceerd B6D2F1 cGVHD-model
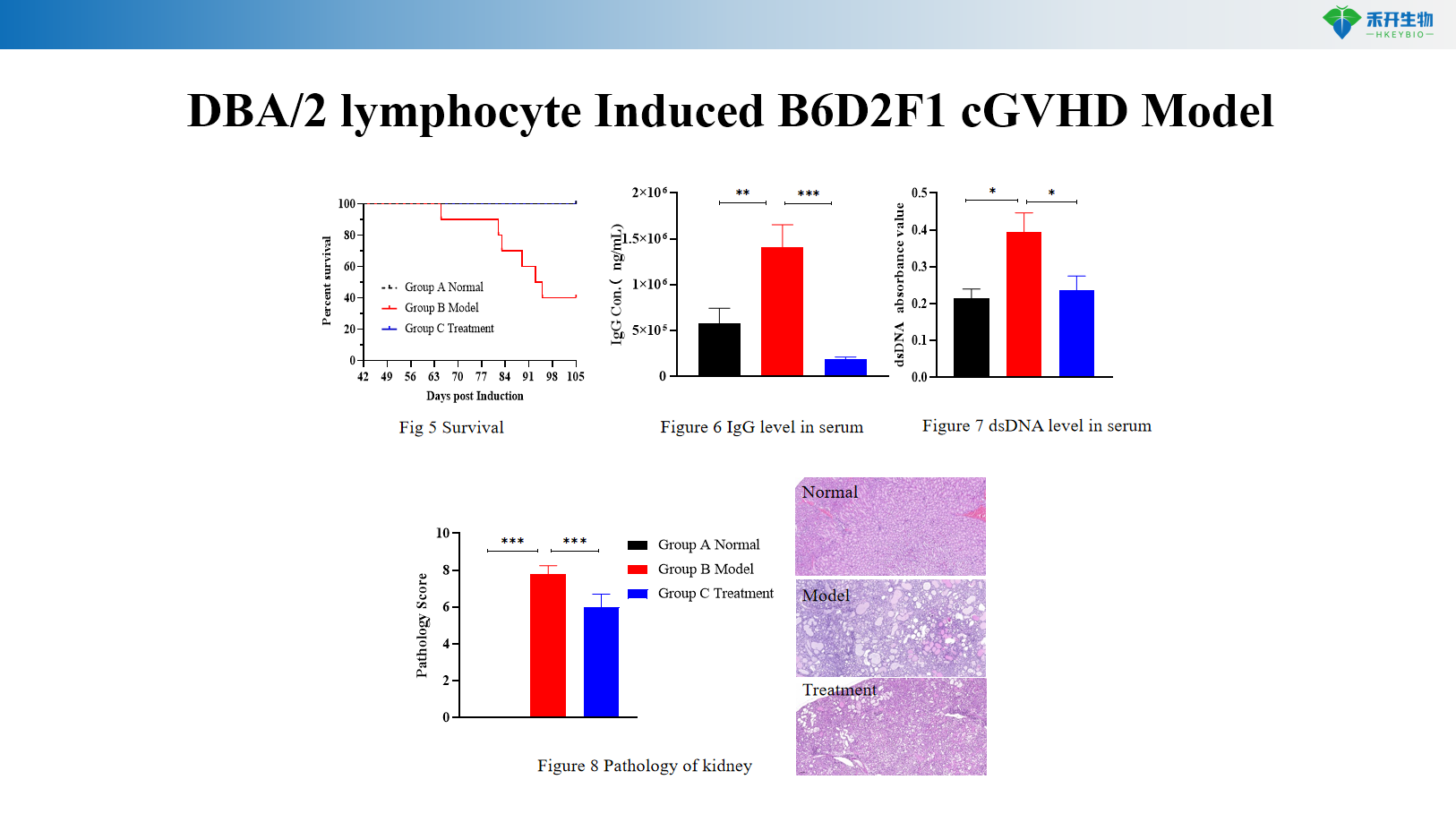
• Werkzaamheidstesten van immunosuppressiva (tacrolimus, cyclosporine, mycofenolaatmofetil, mTOR-remmers) voor preventie en behandeling van GVHD
• Evaluatie van biologische geneesmiddelen die zich richten op T-cellen (anti-CD3, anti-CD4), cytokines (anti-IL-6R, anti-TNF) en co-stimulatieroutes (CTLA-4-Ig)
• Testen van celgebaseerde therapieën (Tregs, MSC's) en antilichaamdepletiestrategieën
• Doelvalidatie voor T-celactivatie, productie van auto-antilichamen en pathologie van meerdere organen
• Farmacologische en toxicologische onderzoeken die IND mogelijk maken
Parameter |
Menselijk PBMC aGVHD-model |
B6 → B6D2F1 aGVHD-model | DBA/2 → B6D2F1 cGVHD-model |
Soort/stam |
NSG-muis (ontvanger) |
B6 → B6D2F1 | DBA/2 → B6D2F1 |
Soort ziekte |
Acuut (xenogeen) | Acuut (allogeen) | Chronisch (lupus-achtig) |
Belangrijkste eindpunten |
Lichaamsgewicht, overleving, GVHD-score | Overleving, GVHD-score | Lichaamsgewicht, overleving, GVHD-score, serum IgG, anti-dsDNA, proteïnurie, bloedbiochemie, nierpathologie |
Vraag: Wat zijn de verschillen tussen de drie GVHD-modellen?
A: Het menselijke PBMC-model is xenogeen, ideaal voor het testen van mensspecifieke therapieën. Het B6 → B6D2F1-model is een MHC-mismatched allogene acute GVHD. Het DBA/2 → B6D2F1-model is een chronische, lupusachtige GVHD met auto-antilichaamproductie, nefritis en fibrose in meerdere organen.
Vraag: Welk model is het meest geschikt voor het testen van anti-menselijke biologische geneesmiddelen?
A: Het door menselijke PBMC geïnduceerde aGVHD-model in NSG-muizen heeft de voorkeur voor het evalueren van mensspecifieke antilichamen (bijvoorbeeld anti-CD3, anti-CD4, anti-IL-6R), aangezien de donor-T-cellen menselijk zijn.
Vraag: Kunnen deze modellen worden gebruikt voor onderzoeken die de IND mogelijk maken?
EEN: Ja. Studies kunnen worden uitgevoerd in overeenstemming met de GLP-principes voor indieningen bij de regelgevende instanties (FDA, EMA).
Vraag: Biedt u op maat gemaakte onderzoeksprotocollen aan (bijvoorbeeld verschillende donorcelaantallen, timing van de behandeling)?
EEN: Absoluut. Ons wetenschappelijk team stemt inductieprotocollen, behandelschema's en eindpuntanalyses af op uw specifieke kandidaat-geneesmiddel.
Vraag: Wat is de typische tijdlijn voor een pilotstudie naar de werkzaamheid?
A: Onderzoek naar acute GVHD loopt doorgaans 4 tot 6 weken na de transplantatie; chronische GVHD-onderzoeken kunnen zich uitstrekken tot 8-12 weken voor de volledige ontwikkeling van auto-antilichamen en orgaanpathologie.
