| Διαθεσιμότητα: | |
|---|---|
| Ποσότητα: | |











Ευρεία κάλυψη ασθενειών – Ξενογενετικά (ανθρώπινα PBMC), αλλογενή μοντέλα οξείας και χρόνιου λύκου GVHD που δεν ταιριάζουν με τον άνθρωπο.
Ποσοτικοποιήσιμα τελικά σημεία – Σωματικό βάρος, ποσοστό επιβίωσης, κλινική βαθμολογία GVHD (κλίμακα 0-10 με στάση, δραστηριότητα, γούνα, δέρμα), αυτοαντισώματα ορού (anti-dsDNA, IgG), πρωτεϊνουρία, ιστοπαθολογία.
Με γνώμονα τον μηχανισμό – Ανθρώπινο μοντέλο PBMC για θεραπείες ειδικά για τον άνθρωπο. αλλογενή μοντέλα για GVHD που προκαλείται από Τ κύτταρα. χρόνιο μοντέλο για παθολογία που προκαλείται από αυτοαντίσωμα.
Μεταφραστική αξία – Ιδανικό για τη δοκιμή ανοσοκατασταλτικών (αναστολέων καλσινευρίνης, αναστολείς mTOR), βιολογικών (anti-TNF, anti-IL-6R) και θεραπειών με βάση τα κύτταρα.
Πακέτα δεδομένων έτοιμα για IND – Οι μελέτες μπορούν να διεξαχθούν σύμφωνα με τις αρχές της ΟΕΠ.
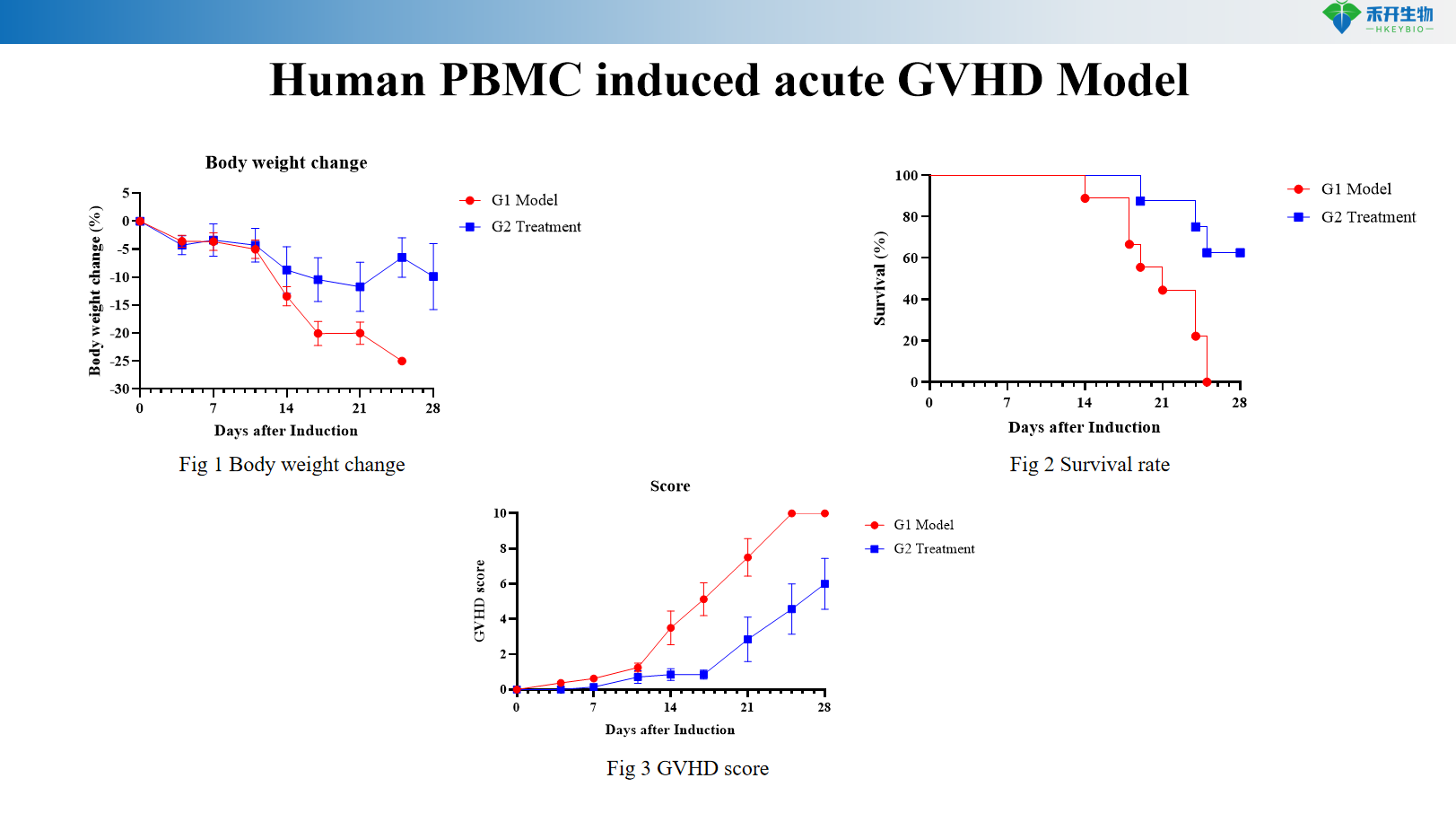
Ανθρώπινο μοντέλο οξείας GVHD που προκαλείται από PBMC
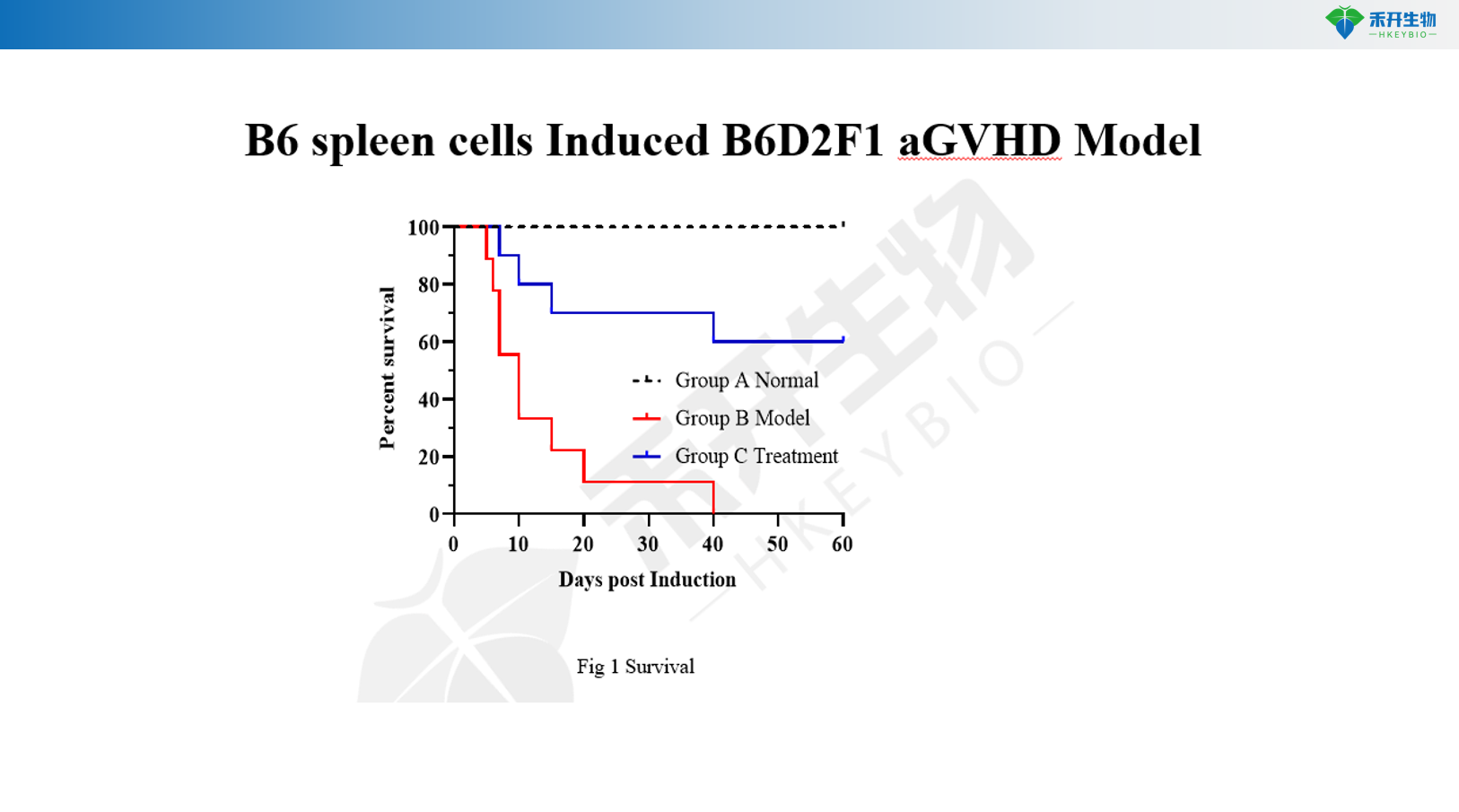
Μοντέλο B6D2F1 aGVHD που προκαλούνται από B6 σπληνικά κύτταρα
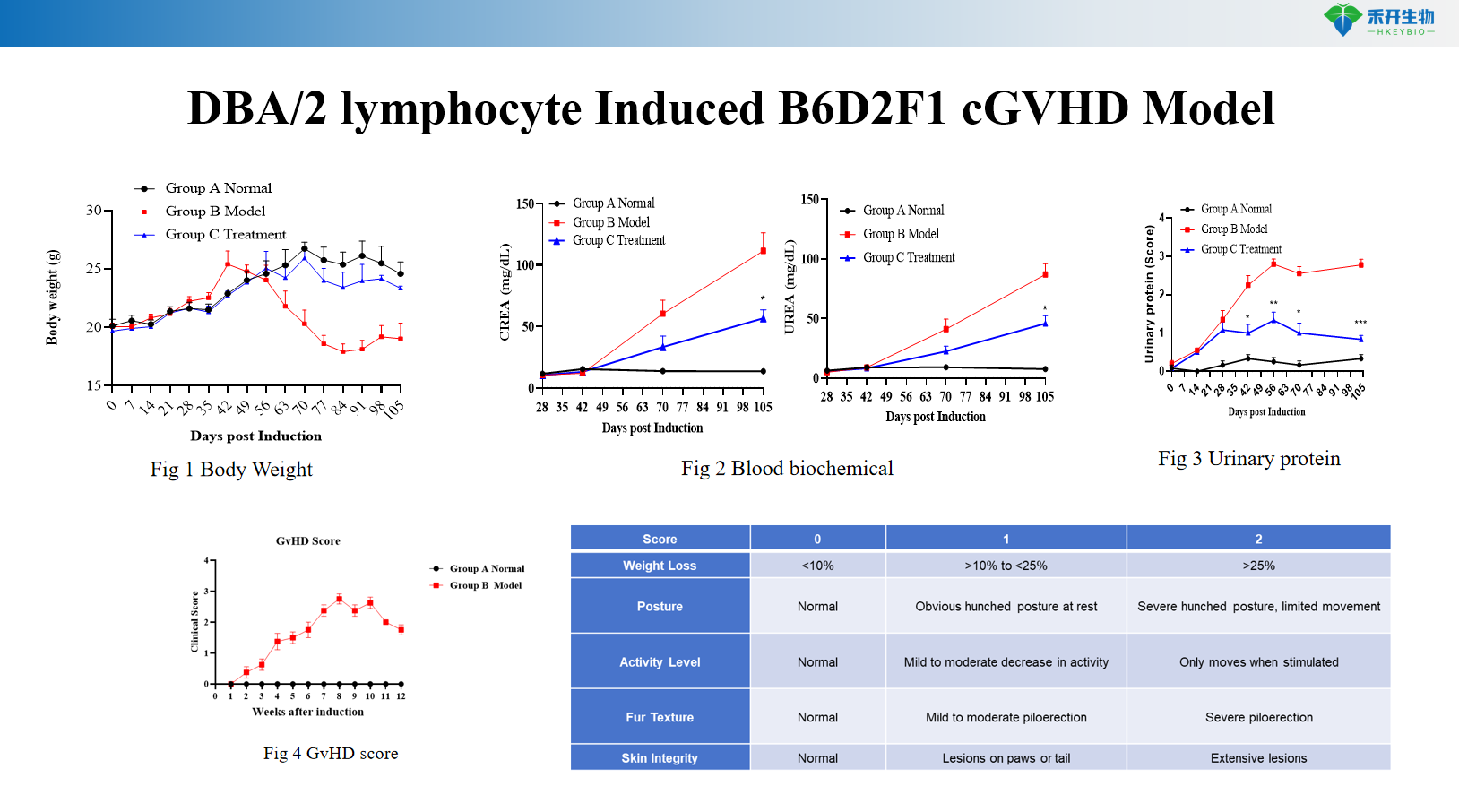
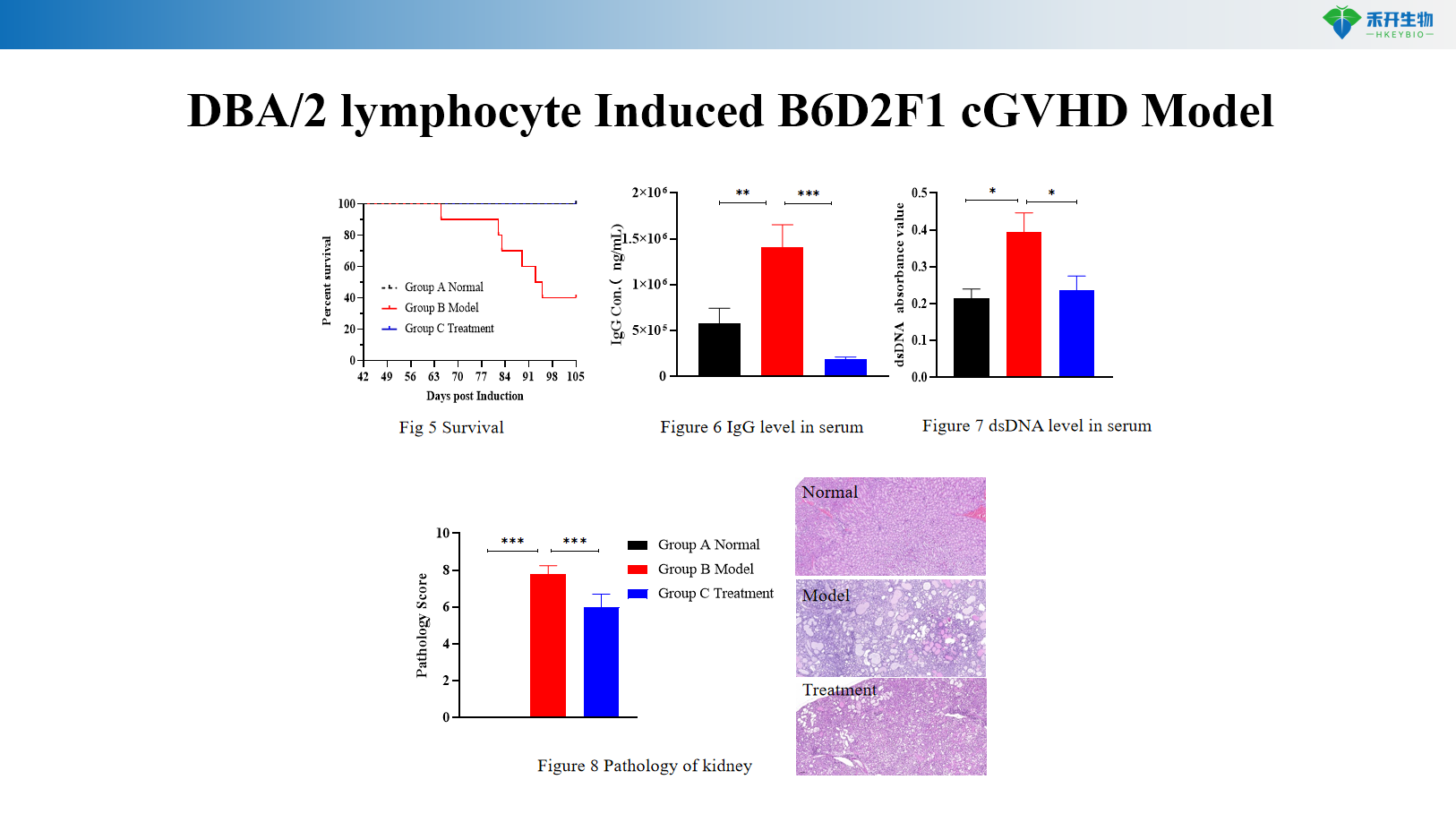
Μοντέλο B6D2F1 cGVHD που προκαλείται από DBA/2 λεμφοκύτταρα
• Δοκιμή αποτελεσματικότητας ανοσοκατασταλτικών (τακρόλιμους, κυκλοσπορίνη, μυκοφαινολάτη μοφετίλ, αναστολείς mTOR) για την πρόληψη και τη θεραπεία της GVHD
• Αξιολόγηση βιολογικών φαρμάκων που στοχεύουν Τ κύτταρα (anti-CD3, anti-CD4), κυτοκινών (anti-IL-6R, anti-TNF) και μονοπατιών συνδιέγερσης (CTLA-4-Ig)
• Δοκιμές θεραπειών με βάση τα κύτταρα (Tregs, MSCs) και στρατηγικών εξάντλησης αντισωμάτων
• Επικύρωση στόχου για την ενεργοποίηση των Τ κυττάρων, την παραγωγή αυτοαντισωμάτων και την παθολογία πολλαπλών οργάνων
• Φαρμακολογικές και τοξικολογικές μελέτες που επιτρέπουν το IND
Παράμετρος |
Ανθρώπινο μοντέλο PBMC aGVHD |
B6 → B6D2F1 aGVHD Μοντέλο | DBA/2 → B6D2F1 cGVHD Μοντέλο |
Είδος / Στέλεχος |
Ποντίκι NSG (παραλήπτης) |
B6 → B6D2F1 | DBA/2 → B6D2F1 |
Τύπος ασθένειας |
Οξεία (ξενογενής) | Οξεία (αλλογενική) | Χρόνια (όπως λύκος) |
Βασικά τελικά σημεία |
Σωματικό βάρος, επιβίωση, βαθμολογία GVHD | Επιβίωση, βαθμολογία GVHD | Σωματικό βάρος, επιβίωση, βαθμολογία GVHD, IgG ορού, anti-dsDNA, πρωτεϊνουρία, βιοχημεία αίματος, παθολογία νεφρών |
Ε: Ποιες είναι οι διαφορές μεταξύ των τριών μοντέλων GVHD;
Α: Το ανθρώπινο μοντέλο PBMC είναι ξενογενές, ιδανικό για τη δοκιμή θεραπειών ειδικών για τον άνθρωπο. Το μοντέλο B6 → B6D2F1 είναι μια αταίριαστη με MHC αλλογενή οξεία GVHD. Το μοντέλο DBA/2 → B6D2F1 είναι ένα χρόνιο GVHD που μοιάζει με λύκο με παραγωγή αυτοαντισωμάτων, νεφρίτιδα και ίνωση πολλαπλών οργάνων.
Ε: Ποιο μοντέλο είναι πιο κατάλληλο για τη δοκιμή αντιανθρώπινων βιολογικών ουσιών;
Α: Το ανθρώπινο μοντέλο aGVHD που προκαλείται από PBMC σε ποντίκια NSG είναι η προτιμώμενη επιλογή για την αξιολόγηση των ανθρώπινων ειδικών αντισωμάτων (π.χ., αντι-CD3, αντι-CD4, αντι-IL-6R) καθώς τα Τ κύτταρα δότη είναι ανθρώπινα.
Ε: Μπορούν αυτά τα μοντέλα να χρησιμοποιηθούν για μελέτες που ενεργοποιούν το IND;
Α: Ναι. Οι μελέτες μπορούν να διεξαχθούν σύμφωνα με τις αρχές της ΟΕΠ για ρυθμιστικές υποβολές (FDA, EMA).
Ε: Προσφέρετε προσαρμοσμένα πρωτόκολλα μελέτης (π.χ. διαφορετικοί αριθμοί κυττάρων δότη, χρόνος θεραπείας);
Α: Απολύτως. Η επιστημονική μας ομάδα προσαρμόζει πρωτόκολλα εισαγωγής, χρονοδιαγράμματα θεραπείας και αναλύσεις τελικών σημείων στο συγκεκριμένο υποψήφιο φάρμακο.
Ε: Ποιο είναι το τυπικό χρονοδιάγραμμα για μια πιλοτική μελέτη αποτελεσματικότητας;
A: Οι μελέτες οξείας GVHD συνήθως διεξάγονται 4-6 εβδομάδες μετά τη μεταμόσχευση. Οι χρόνιες μελέτες GVHD μπορεί να επεκταθούν σε 8-12 εβδομάδες για πλήρη ανάπτυξη αυτοαντισωμάτων και παθολογίας οργάνων.
