| Elérhetőség: | |
|---|---|
| Mennyiség: | |











Klinikailag releváns – az LPS-indukált ALI szorosan utánozza a humán ALI/ARDS-t akut gyulladással, leukocita infiltrációval és tüdőödémával.
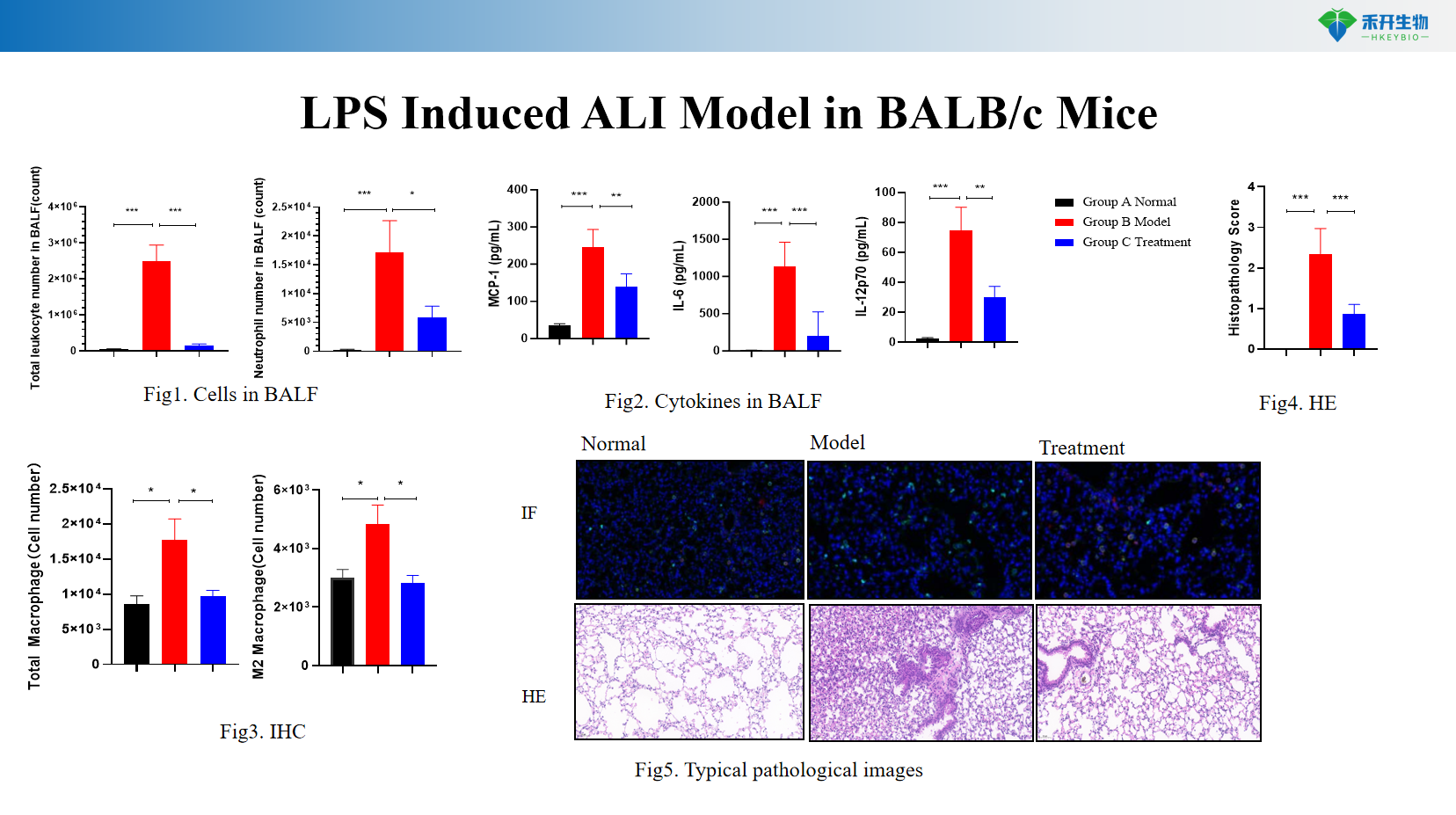
Átfogó végpontok – BALF sejtszám (limfociták, neutrofilek, makrofágok), citokin profilalkotás (MCP-1, IL-6, IL-10), tüdőszövettani vizsgálat (HE, IHC), tüdőödéma felmérése (nedves/száraz arány).
Mechanizmus által vezérelt – Az LPS aktiválja a TLR4 jelátvitelt, kiváltva az NF-κB útvonalat és erőteljes gyulladásos választ, tükrözve a Gram-negatív szepszis által kiváltott tüdőkárosodást.
Transzlációs érték – Ideális gyulladáscsökkentő gyógyszerek, citokin-gátlók, neutrofil elasztáz inhibitorok és sejtalapú terápiák tesztelésére.
IND-ready adatcsomagok – A vizsgálatok a GLP elveinek megfelelően végezhetők.
LPS-indukált ALI modell BALB/c egerekben
• Gyulladáscsökkentő gyógyszerek (kortikoszteroidok, NSAID-ok), citokin-gátlók (anti-IL-6, anti-TNF-α) és neutrofil elasztáz inhibitorok hatékonyságának vizsgálata
• A mesenchymális őssejt (MSC) terápia és az extracelluláris vezikula alapú kezelések értékelése
• Célérvényesítés a TLR4 jelátvitelhez, az NF-κB útvonalhoz és a gyulladásos kaszkádokhoz
• Biomarkerek felfedezése (BALF sejtprofilok, citokin aláírások, tüdősérülési markerek)
• IND-t lehetővé tevő farmakológiai és toxikológiai vizsgálatok
Paraméter |
Specifikáció |
Faj/törzs |
BALB/c egér |
Indukciós módszer |
Lipopoliszacharid (LPS, 5-10 mg/kg) intratracheális, intranazális vagy intraperitoneális beadása |
A tanulmány időtartama |
Akut: 6-48 órával az LPS beadása után |
Kulcsfontosságú végpontok |
BALF sejtszám (összes és differenciális: neutrofilek, makrofágok, limfociták), BALF citokinszintek (MCP-1, IL-6, IL-10 ELISA-val), tüdőszövettan (HE festés tüdősérülési pontszámmal), immunhisztokémia (IHC) a gyulladásos markerek számára (opcionális lúg-populációs markerek, lúg-populáris súlyarány). aktivitás, oxidatív stressz markerek |
Adatcsomag |
Nyers adatok, elemzési jelentések, BALF sejtszámok, ELISA eredmények, szövettani tárgylemezek (HE, IHC), bioinformatika (opcionális) |
K: Hogyan idéz elő az LPS akut tüdőkárosodást egerekben?
V: Az LPS az immunsejteken kötődik a TLR4-hez, aktiválja az NF-κB és MAPK útvonalakat, ami erős gyulladásos válaszhoz vezet citokin felszabadulás mellett (IL-6, TNF-α, MCP-1), neutrofilek toborzásához a tüdőben, megnövekedett vaszkuláris permeabilitással és alveoláris károsodással, ami szorosan utánozza a Grammalis-negduced Sepsim-et.
K: Mik a legfontosabb hasonlóságok az emberi ALI/ARDS-szel?
V: A modell neutrofil infiltrációt, emelkedett pro-inflammatorikus citokinek, tüdőödémát és kórszövettani jellemzőket (alveoláris megvastagodás, hialin membrán képződés) mutat, amelyek megegyeznek a humán ALI/ARDS-szel.
K: Használható ez a modell IND-t lehetővé tevő vizsgálatokhoz?
V: Igen. A vizsgálatok a hatósági beadványok (FDA, EMA) GLP-elvei szerint végezhetők.
K: Kínál személyre szabott vizsgálati protokollokat (pl. különböző LPS-dózisok, beadási módok, időpontok)?
V: Abszolút. Tudományos csapatunk az LPS adagolási rendjét, beadási módjait és végpontelemzéseit az Ön konkrét gyógyszerjelöltjeihez szabja.
