| Disponibilidade: | |
|---|---|
| Quantidade: | |











Clinicamente relevante – a LPA induzida por LPS imita de perto a LPA/SDRA humana com inflamação aguda, infiltração de leucócitos e edema pulmonar.
Endpoints abrangentes – contagens de células LBA (linfócitos, neutrófilos, macrófagos), perfil de citocinas (MCP-1, IL-6, IL-10), histopatologia pulmonar (HE, IHC), avaliação de edema pulmonar (relação úmido/seco).
Impulsionado pelo mecanismo – o LPS ativa a sinalização do TLR4, desencadeando a via do NF-κB e uma resposta inflamatória robusta, refletindo a lesão pulmonar induzida pela sepse Gram-negativa.
Valor translacional – Ideal para testar medicamentos antiinflamatórios, inibidores de citocinas, inibidores de elastase de neutrófilos e terapias baseadas em células.
Pacotes de dados prontos para IND – Os estudos podem ser conduzidos de acordo com os princípios das BPL.
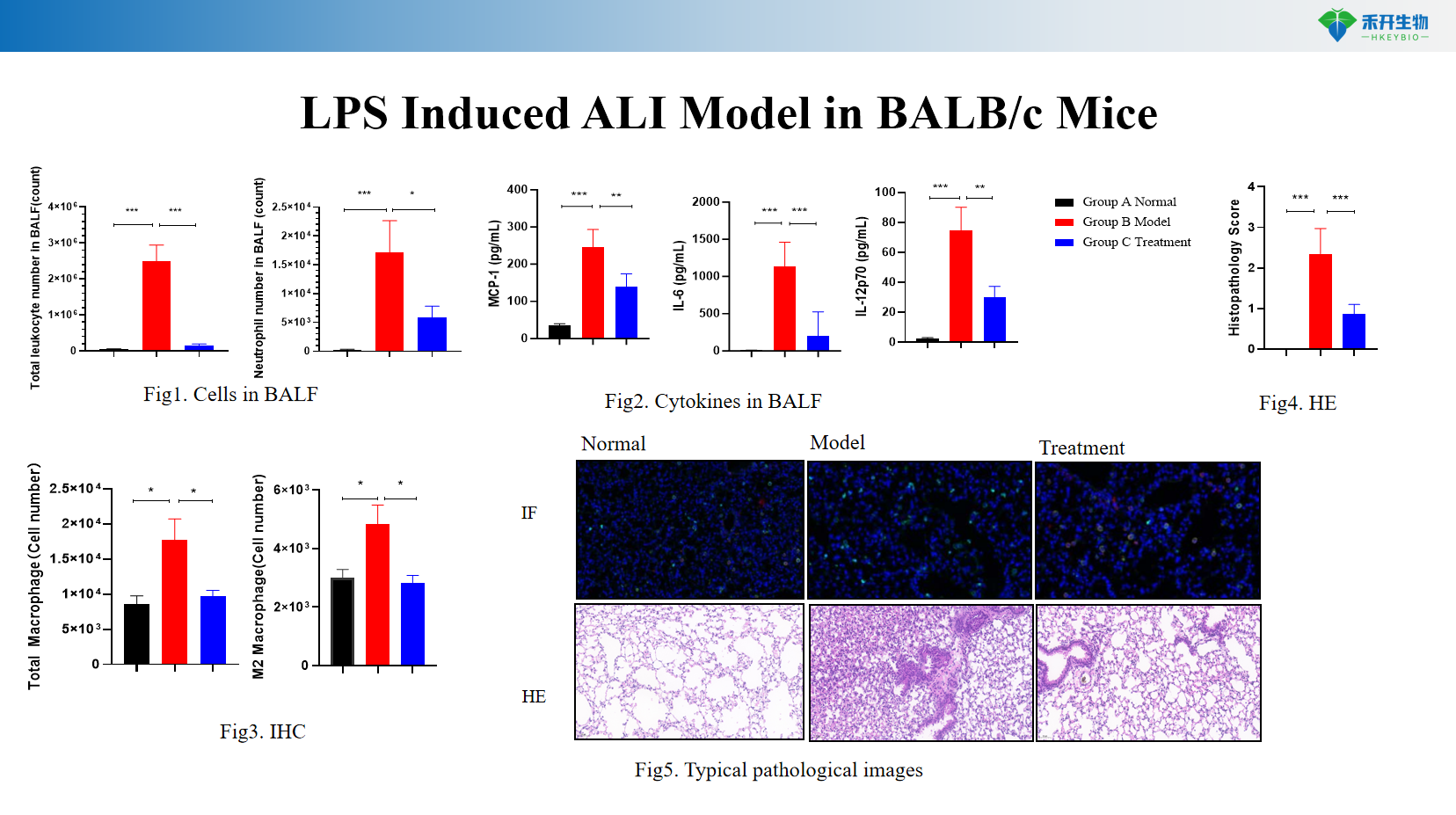
Modelo ALI induzido por LPS em camundongos BALB/c
• Teste de eficácia de medicamentos anti-inflamatórios (corticosteróides, AINEs), inibidores de citocinas (anti-IL-6, anti-TNF-α) e inibidores de elastase de neutrófilos
• Avaliação da terapia com células-tronco mesenquimais (MSC) e tratamentos baseados em vesículas extracelulares
• Validação de alvo para sinalização TLR4, via NF-κB e cascatas inflamatórias
• Descoberta de biomarcadores (perfis de células BALF, assinaturas de citocinas, marcadores de lesão pulmonar)
• Estudos de farmacologia e toxicologia que permitem IND
Parâmetro |
Especificação |
Espécie/Estirpe |
Rato BALB/c |
Método de indução |
Administração intratraqueal, intranasal ou intraperitoneal de lipopolissacarídeo (LPS, 5–10 mg/kg) |
Duração do estudo |
Agudo: 6–48 horas após a administração de LPS |
Principais pontos de extremidade |
Contagens de células LBA (total e diferencial: neutrófilos, macrófagos, linfócitos), níveis de citocinas LBA (MCP-1, IL-6, IL-10 por ELISA), histopatologia pulmonar (coloração HE com pontuação de lesão pulmonar), imuno-histoquímica (IHQ) para marcadores inflamatórios, relação peso úmido/seco do pulmão (edema pulmonar), opcional: atividade de MPO, marcadores de estresse oxidativo |
Pacote de dados |
Dados brutos, relatórios de análise, contagens de células BALF, resultados de ELISA, lâminas histológicas (HE, IHC), bioinformática (opcional) |
P: Como o LPS induz lesão pulmonar aguda em camundongos?
A: O LPS se liga ao TLR4 nas células do sistema imunológico, ativando as vias NF-κB e MAPK, levando a uma resposta inflamatória robusta com liberação de citocinas (IL-6, TNF-α, MCP-1), recrutamento de neutrófilos para os pulmões, aumento da permeabilidade vascular e dano alveolar, imitando de perto a LPA induzida por sepse Gram-negativa.
P: Quais são as principais semelhanças com LPA/SDRA humana?
A: O modelo exibe infiltração de neutrófilos, citocinas pró-inflamatórias elevadas, edema pulmonar e características histopatológicas (espessamento alveolar, formação de membrana hialina) idênticas à LPA/SDRA humana.
P: Este modelo pode ser usado para estudos que habilitam o IND?
R: Sim. Os estudos podem ser conduzidos de acordo com os princípios das BPL para submissões regulatórias (FDA, EMA).
P: Vocês oferecem protocolos de estudo personalizados (por exemplo, diferentes doses de LPS, vias de administração, momentos)?
R: Absolutamente. Nossa equipe científica adapta regimes de dosagem de LPS, vias de administração e análises de desfechos para seu medicamento candidato específico.
