| Dostępność: | |
|---|---|
| Ilość: | |











Klinicznie istotne – ALI wywołany LPS bardzo naśladuje ludzki ALI/ARDS z ostrym stanem zapalnym, naciekiem leukocytów i obrzękiem płuc.
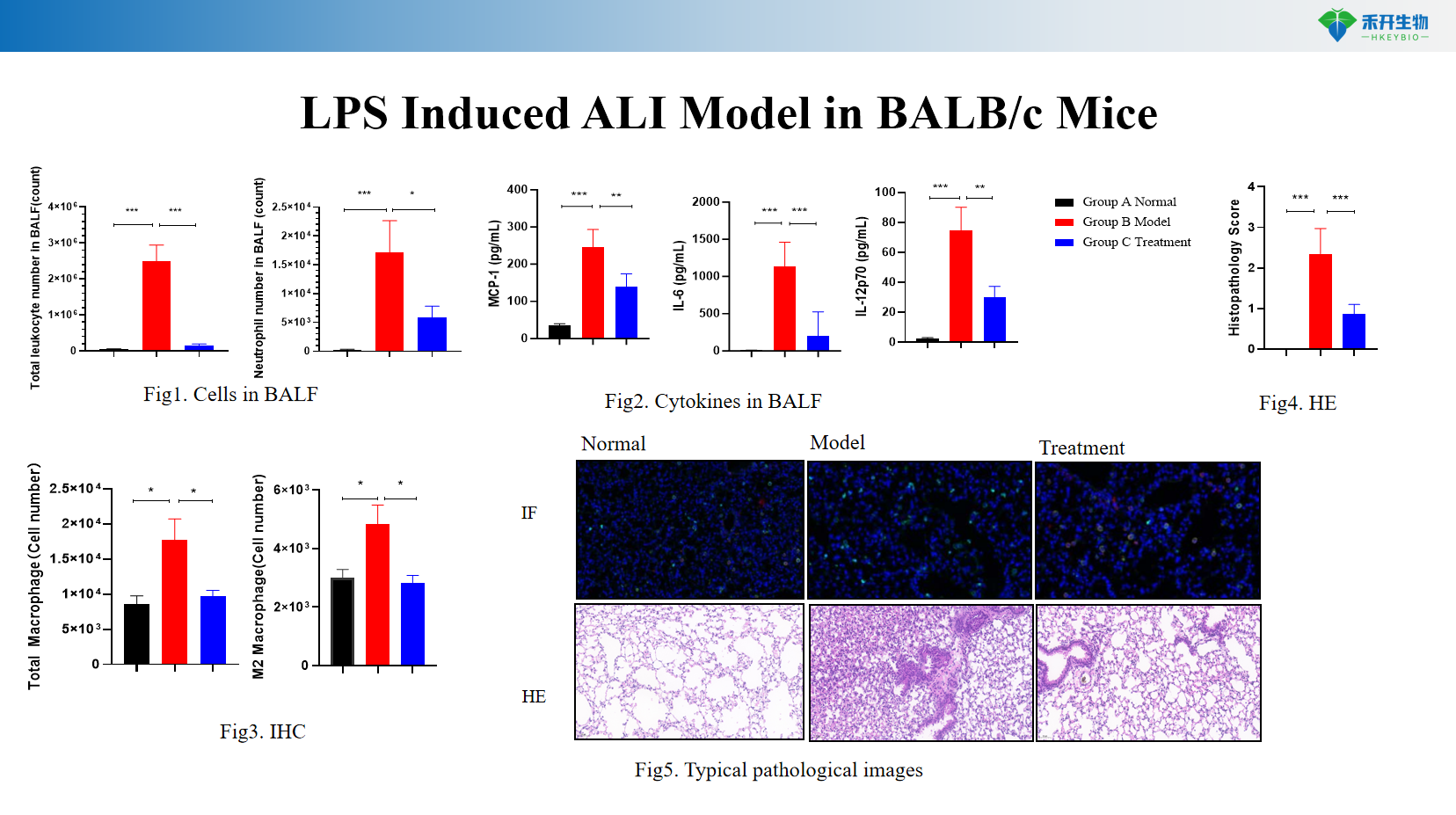
Kompleksowe punkty końcowe – liczba komórek BALF (limfocyty, neutrofile, makrofagi), profilowanie cytokin (MCP-1, IL-6, IL-10), histopatologia płuc (HE, IHC), ocena obrzęku płuc (stosunek mokry/suchy).
Oparta na mechanizmach – LPS aktywuje sygnalizację TLR4, wyzwalając szlak NF-κB i silną odpowiedź zapalną, odzwierciedlając uszkodzenie płuc wywołane sepsą Gram-ujemną.
Wartość translacyjna – Idealny do testowania leków przeciwzapalnych, inhibitorów cytokin, inhibitorów elastazy neutrofilowej i terapii komórkowych.
Pakiety danych gotowe do IND – Badania mogą być prowadzone zgodnie z zasadami GLP.
Model ALI indukowany LPS u myszy BALB/c
• Testowanie skuteczności leków przeciwzapalnych (kortykosteroidy, NLPZ), inhibitorów cytokin (anty-IL-6, anty-TNF-α) i inhibitorów elastazy neutrofilowej
• Ocena terapii mezenchymalnymi komórkami macierzystymi (MSC) i terapii opartych na pęcherzykach zewnątrzkomórkowych
• Walidacja celu dla sygnalizacji TLR4, szlaku NF-κB i kaskad zapalnych
• Odkrycie biomarkerów (profile komórek BALF, sygnatury cytokin, markery uszkodzenia płuc)
• Badania farmakologiczne i toksykologiczne umożliwiające IND
Parametr |
Specyfikacja |
Gatunek/szczep |
Mysz BALB/c |
Metoda indukcyjna |
Dotchawicze, donosowe lub dootrzewnowe podanie lipopolisacharydu (LPS, 5–10 mg/kg) |
Czas trwania nauki |
Ostre: 6–48 godzin po podaniu LPS |
Kluczowe punkty końcowe |
Liczba komórek BALF (całkowita i różnicowa: neutrofile, makrofagi, limfocyty), poziom cytokin BALF (MCP-1, IL-6, IL-10 metodą ELISA), histopatologia płuc (barwienie HE z oceną uszkodzenia płuc), immunohistochemia (IHC) dla markerów stanu zapalnego, stosunek masy mokrej do suchej płuc (obrzęk płuc), opcjonalnie: aktywność MPO, markery stresu oksydacyjnego |
Pakiet danych |
Surowe dane, raporty analityczne, liczba komórek BALF, wyniki ELISA, preparaty histologiczne (HE, IHC), bioinformatyka (opcjonalnie) |
P: W jaki sposób LPS wywołuje ostre uszkodzenie płuc u myszy?
Odp.: LPS wiąże się z TLR4 na komórkach odpornościowych, aktywując szlaki NF-κB i MAPK, co prowadzi do silnej odpowiedzi zapalnej z uwolnieniem cytokin (IL-6, TNF-α, MCP-1), rekrutacją neutrofili do płuc, zwiększoną przepuszczalnością naczyń i uszkodzeniem pęcherzyków płucnych, bardzo naśladując ALI indukowany sepsą Gram-ujemną.
P: Jakie są kluczowe podobieństwa z ludzkim ALI/ARDS?
Odp.: Model wykazuje naciek neutrofilów, podwyższony poziom cytokin prozapalnych, obrzęk płuc i cechy histopatologiczne (pogrubienie pęcherzyków, tworzenie błony szklistej) identyczne z ludzkim ALI/ARDS.
P: Czy ten model można wykorzystać do badań umożliwiających IND?
O: Tak. Badania można przeprowadzić zgodnie z zasadami GLP dotyczącymi zgłoszeń regulacyjnych (FDA, EMA).
P: Czy oferujecie niestandardowe protokoły badań (np. różne dawki LPS, drogi podawania, punkty czasowe)?
O: Absolutnie. Nasz zespół naukowy dostosowuje schematy dawkowania LPS, drogi podawania i analizy punktów końcowych do konkretnego kandydata na lek.
