| Disponibilité : | |
|---|---|
| Quantité : | |











Cliniquement pertinent – L’ALI induite par le LPS imite étroitement l’ALI/ARDS humain avec une inflammation aiguë, une infiltration de leucocytes et un œdème pulmonaire.
Critères d'évaluation complets : numération des cellules BALF (lymphocytes, neutrophiles, macrophages), profilage des cytokines (MCP-1, IL-6, IL-10), histopathologie pulmonaire (HE, IHC), évaluation de l'œdème pulmonaire (rapport humide/sec).
Axé sur un mécanisme – Le LPS active la signalisation TLR4, déclenchant la voie NF-κB et une réponse inflammatoire robuste, reflétant les lésions pulmonaires induites par la septicémie à Gram négatif.
Valeur translationnelle – Idéal pour tester des médicaments anti-inflammatoires, des inhibiteurs de cytokines, des inhibiteurs de l’élastase des neutrophiles et des thérapies cellulaires.
Ensembles de données prêts pour l'IND – Les études peuvent être menées conformément aux principes BPL.
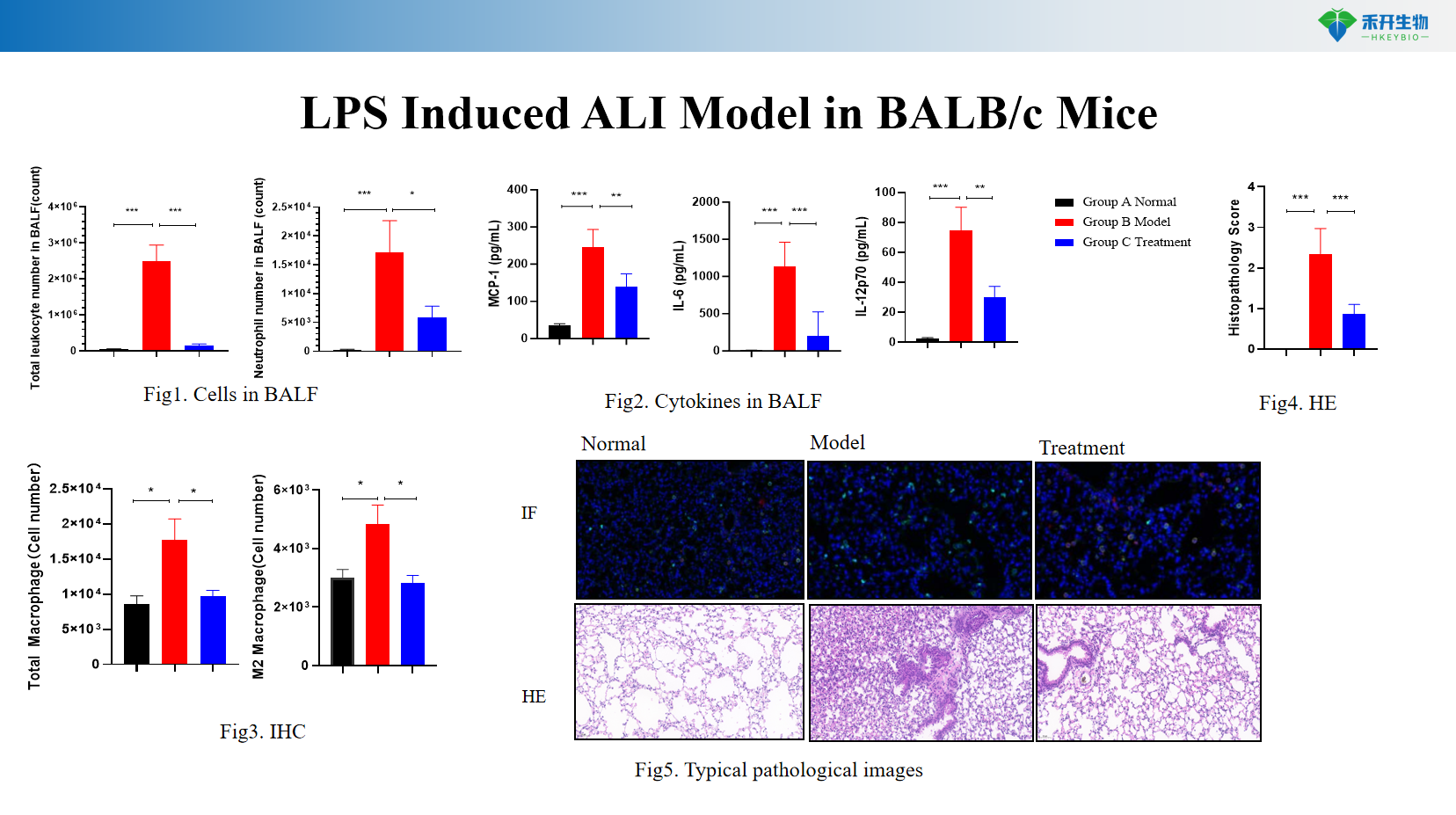
Modèle ALI induit par LPS chez les souris BALB/c
• Tests d'efficacité des médicaments anti-inflammatoires (corticostéroïdes, AINS), des inhibiteurs de cytokines (anti-IL-6, anti-TNF-α) et des inhibiteurs de l'élastase des neutrophiles.
• Évaluation de la thérapie par cellules souches mésenchymateuses (CSM) et des traitements à base de vésicules extracellulaires
• Validation des cibles pour la signalisation TLR4, la voie NF-κB et les cascades inflammatoires
• Découverte de biomarqueurs (profils cellulaires BALF, signatures de cytokines, marqueurs de lésions pulmonaires)
• Études pharmacologiques et toxicologiques permettant l'IND
Paramètre |
Spécification |
Espèce/souche |
Souris BALB/c |
Méthode d'induction |
Administration intratrachéale, intranasale ou intrapéritonéale de lipopolysaccharide (LPS, 5 à 10 mg/kg) |
Durée des études |
Aigu : 6 à 48 heures après l'administration du LPS |
Points de terminaison clés |
Numération cellulaire BALF (totale et différentielle : neutrophiles, macrophages, lymphocytes), taux de cytokines BALF (MCP-1, IL-6, IL-10 par ELISA), histopathologie pulmonaire (coloration HE avec score de lésion pulmonaire), immunohistochimie (IHC) pour les marqueurs inflammatoires, rapport poids humide/sec des poumons (œdème pulmonaire), facultatif : activité MPO, marqueurs de stress oxydatif |
Paquet de données |
Données brutes, rapports d'analyse, numération cellulaire BALF, résultats ELISA, lames histologiques (HE, IHC), bioinformatique (facultatif) |
Q : Comment le LPS induit-il des lésions pulmonaires aiguës chez la souris ?
R : Le LPS se lie au TLR4 sur les cellules immunitaires, activant les voies NF-κB et MAPK, conduisant à une réponse inflammatoire robuste avec libération de cytokines (IL-6, TNF-α, MCP-1), recrutement de neutrophiles dans les poumons, augmentation de la perméabilité vasculaire et lésions alvéolaires, imitant fidèlement l'ALI induite par la septicémie à Gram négatif.
Q : Quelles sont les principales similitudes avec l’ALI/ARDS humain ?
R : Le modèle présente une infiltration de neutrophiles, des cytokines pro-inflammatoires élevées, un œdème pulmonaire et des caractéristiques histopathologiques (épaississement alvéolaire, formation de membrane hyaline) identiques à l'ALI/ARDS humain.
Q : Ce modèle peut-il être utilisé pour des études permettant l’IND ?
R : Oui. Les études peuvent être menées conformément aux principes BPL pour les soumissions réglementaires (FDA, EMA).
Q : Proposez-vous des protocoles d'étude personnalisés (par exemple, différentes doses de LPS, voies d'administration, moments) ?
R : Absolument. Notre équipe scientifique adapte les schémas posologiques, les voies d'administration et les analyses des paramètres de LPS à votre candidat-médicament spécifique.
