| Dostupnost: | |
|---|---|
| Množství: | |











Klinicky relevantní – Rekapituluje lidskou přecitlivělost I. typu: degranulaci žírných buněk zprostředkovanou IgE a reakci wheal-and-flare.
Kvantifikovatelné koncové body – Hodnocení klinických příznaků (velikost pupínků, erytém, edém), měření lokalizované kožní reakce.
Mechanismem řízené – Přímé hodnocení dráhy IgE/FcεRI a funkce žírných buněk in vivo.
Translační hodnota – Ideální pro testování anti-IgE biologických látek (omalizumab, ligelizumab), stabilizátorů žírných buněk (kromolyn, ketotifen), H1-antihistaminik a dalších antialergických látek.
Datové balíčky připravené pro IND – Studie lze provádět v souladu se zásadami SLP.
Model NHP PCA indukovaný DNP-IgE a DNFB
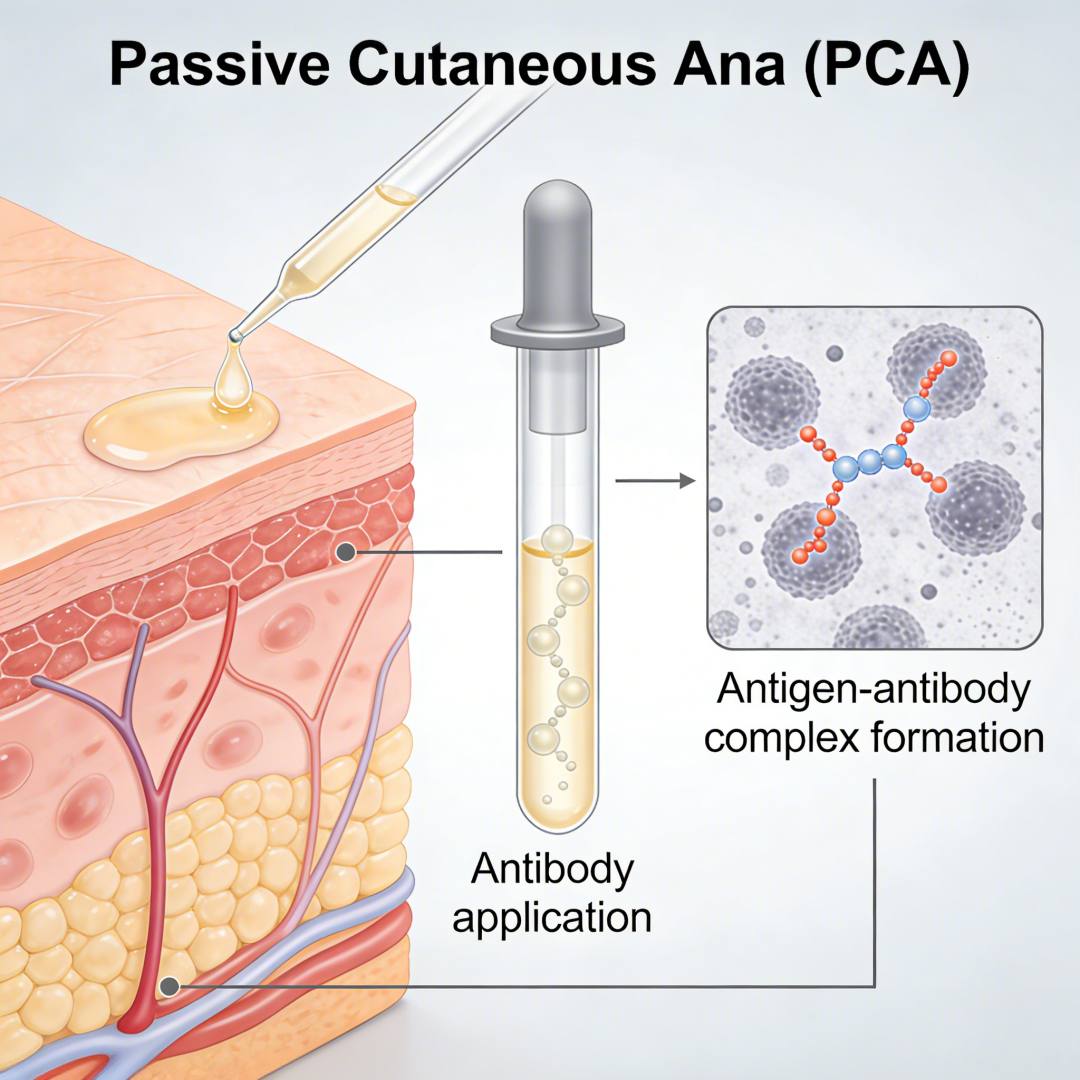
• Testování účinnosti anti-IgE biologických látek (omalizumab, ligelizumab, jiné anti-IgE protilátky)
• Vyhodnocení stabilizátorů žírných buněk (kromolyn, ketotifen, nedocromil) a H1-antihistaminik
• Cílová validace pro IgE/FcεRI dráhu a biologii žírných buněk
• Objev biomarkerů (IgE, mediátory žírných buněk)
• Farmakologické a toxikologické studie umožňující IND
Parametr |
Specifikace |
Druh/kmen |
Makak Cynomolgus ( Macaca fascicularis ) |
Indukční metoda |
Intradermální injekce DNP-specifického IgE (den 1) následovaná topickou aplikací DNFB na stejné místo (den 2) |
Délka studia |
2–3 dny (senzibilizace + provokace) |
Klíčové koncové body |
Bodování klinických příznaků (velikost pupínků, erytém, edém), měření lokalizované kožní reakce (průměr, tloušťka), volitelné: histopatologie kůže (degranulace žírných buněk), hladiny IgE v séru |
Datový balíček |
Nezpracovaná data, analytické zprávy, klinické fotografie, histologická sklíčka (volitelně), bioinformatika (volitelně) Nezpracovaná data, analytické zprávy, klinická chemie, analýza moči, histologická sklíčka, bioinformatika (volitelně) |
Otázka: Jak funguje model PCA indukovaný DNP-IgE a DNFB?
Odpověď: DNP-specifický IgE je pasivně přenášen intradermální injekcí a váže se na FcεRI receptory na žírných buňkách. Následná topická expozice DNFB na stejném místě zesíťuje navázaný IgE, spouští degranulaci žírných buněk, uvolňování histaminu a lokalizovanou reakci puchýře a vzplanutí.
Otázka: Jaké jsou klíčové podobnosti s lidskou přecitlivělostí I. typu?
Odpověď: Model vykazuje aktivaci žírných buněk zprostředkovanou IgE, uvolňování histaminu, vazodilataci a lokalizovaný edém, přímo odrážející lidské alergické reakce, jako je kopřivka a anafylaxe.
Otázka: Lze tento model použít pro studie umožňující IND?
A: Ano. Studie mohou být prováděny v souladu se zásadami SLP pro regulační podání (FDA, EMA).
Otázka: Nabízíte přizpůsobené protokoly studií (např. různé dávky IgE, provokační koncentrace)?
A: Rozhodně. Náš vědecký tým přizpůsobuje koncentrace IgE, testovací protokoly a analýzy koncových bodů vašemu konkrétnímu kandidátovi na lék.
Otázka: Jaká je typická časová osa pro pilotní studii účinnosti?
Odpověď: Model je dokončen během 2–3 dnů, což umožňuje rychlý screening antialergických sloučenin.
