| Ketersediaan: | |
|---|---|
| Kuantitas: | |











Relevan secara klinis – Kombinasi asap rokok dan paparan LPS mirip dengan etiologi PPOK pada manusia dan peradangan kronis.
Berbagai spesies – Model tikus dan tikus tersedia untuk memenuhi kebutuhan eksperimen yang berbeda (alat genetik vs. ukuran yang lebih besar).
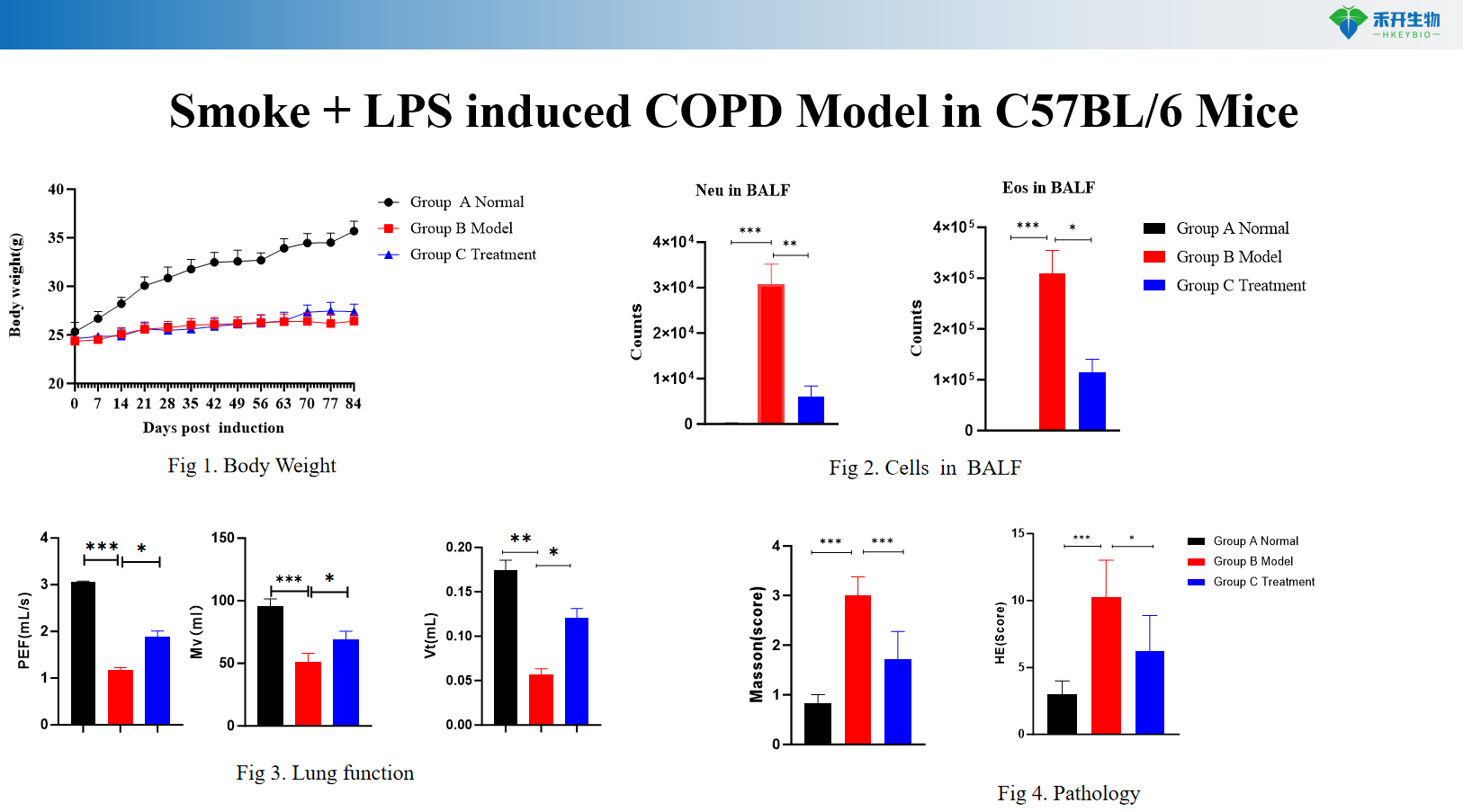
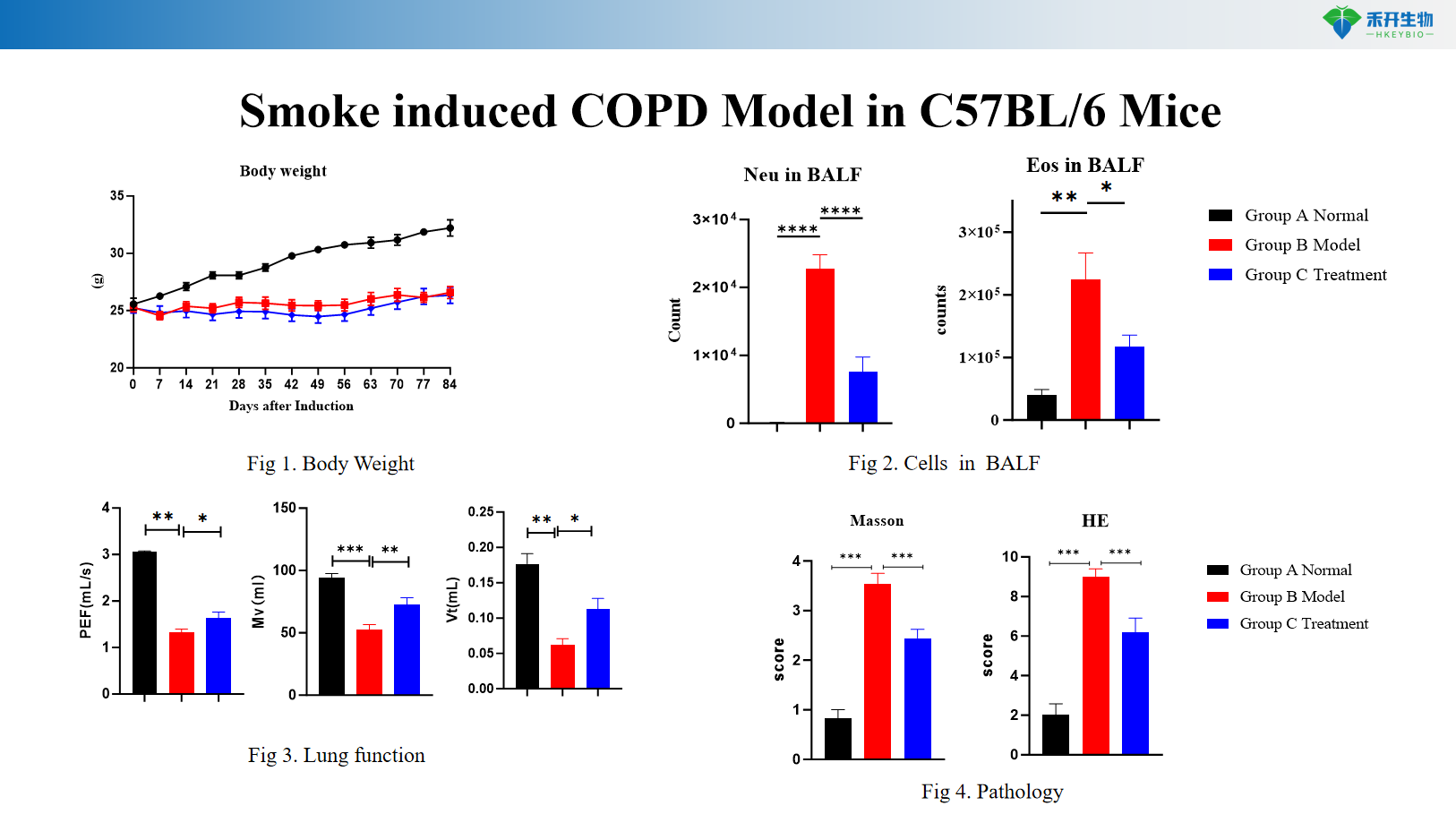
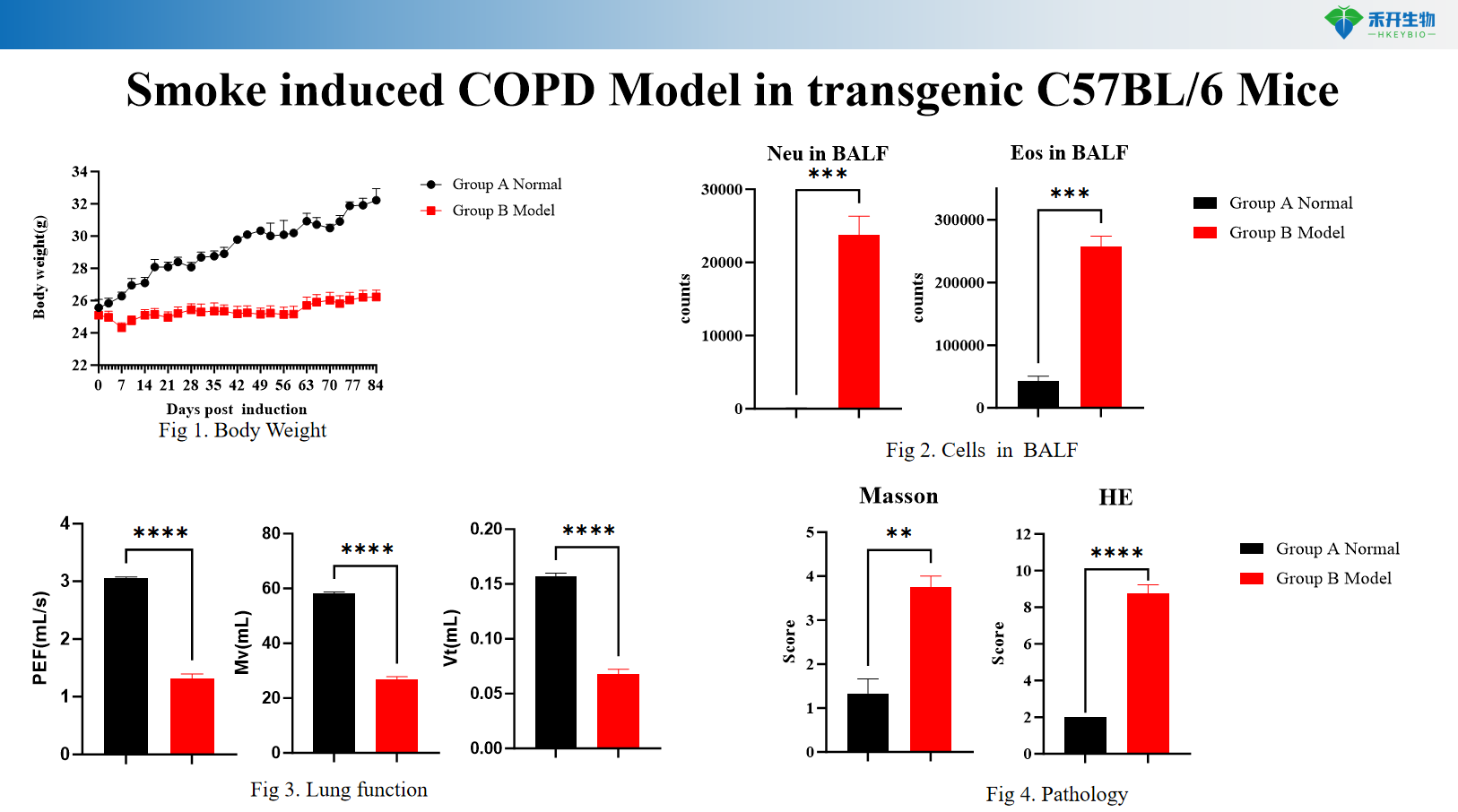
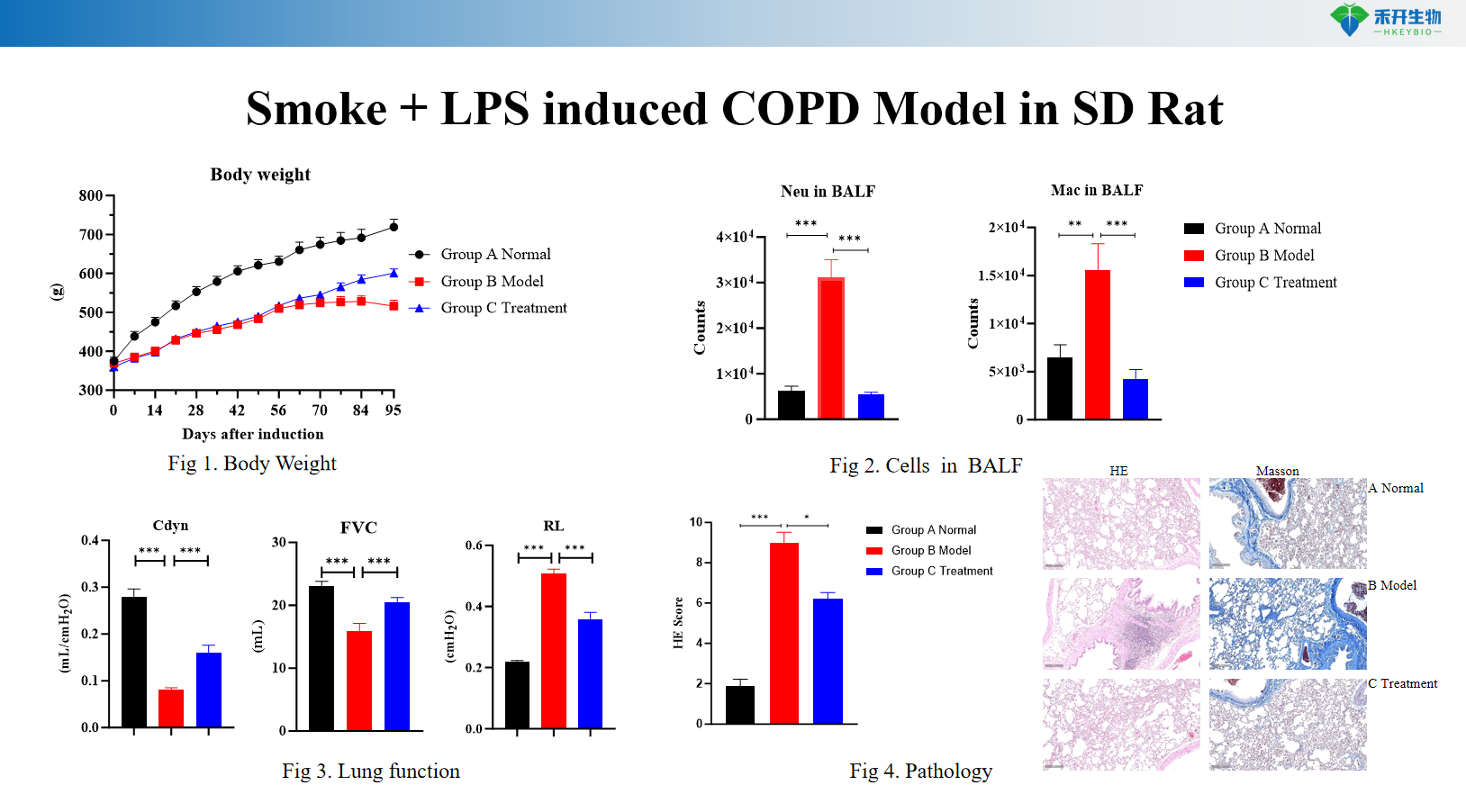
Titik akhir yang komprehensif – Berat badan, sitologi BALF (WBC, makrofag, monosit), fungsi paru-paru (resistensi, kepatuhan), histopatologi (skor HE), profil sitokin.
Nilai translasi – Ideal untuk menguji obat anti inflamasi (kortikosteroid, inhibitor PDE4), bronkodilator, dan mukolitik.
Paket data yang siap untuk IND – Studi dapat dilakukan sesuai dengan prinsip GLP.
Model COPD yang diinduksi Asap + LPS pada Tikus C57BL/6
Model COPD yang diinduksi asap pada Tikus C57BL/6
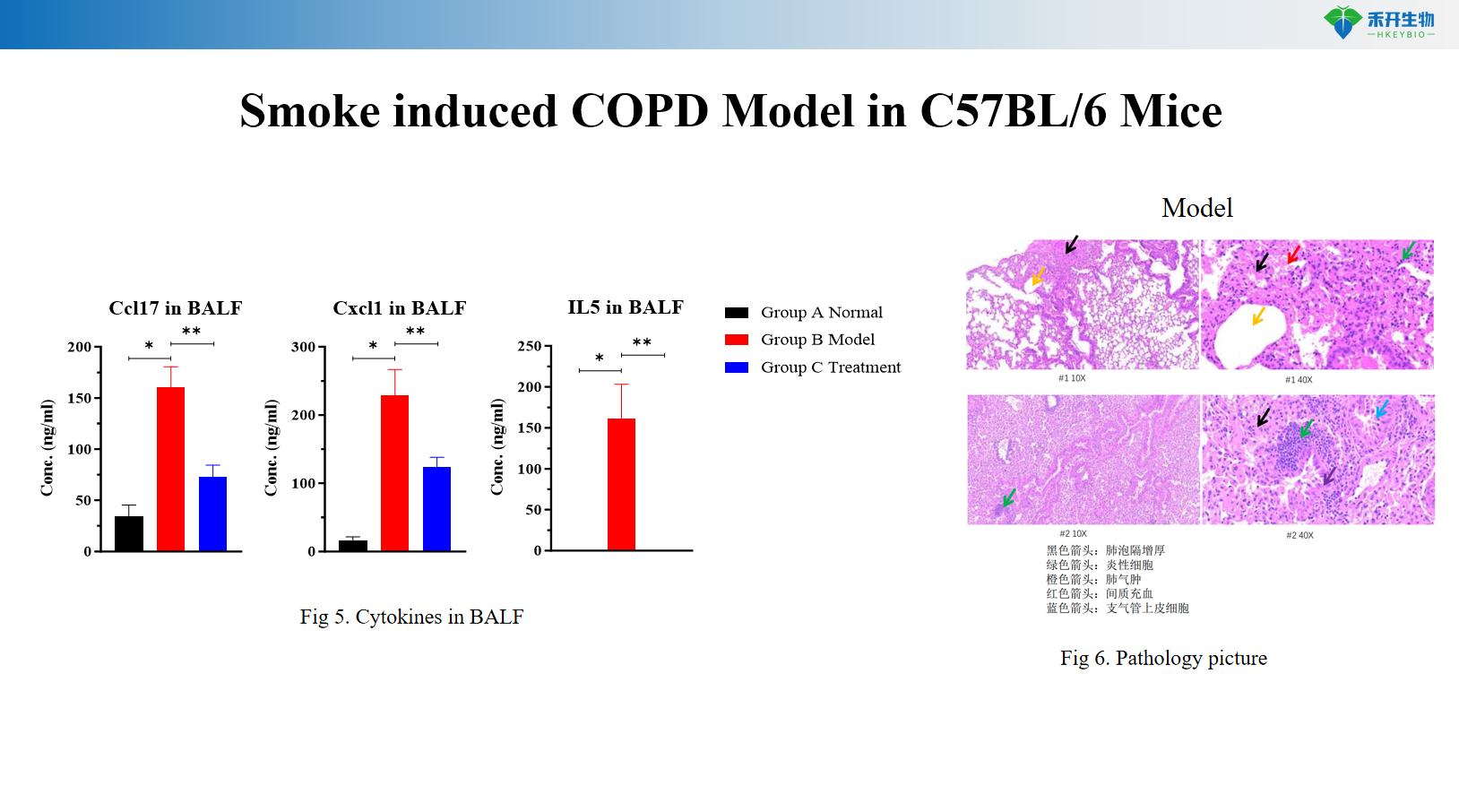
Model COPD yang diinduksi asap pada tikus transgenik C57BL/6
Model COPD yang diinduksi Asap + LPS pada Tikus SD
• Uji efikasi obat anti inflamasi (kortikosteroid, inhibitor PDE4, inhibitor p38 MAPK)
• Evaluasi bronkodilator (agonis β2, antikolinergik) dan terapi kombinasi
• Pengujian zat mukoaktif dan antioksidan
• Validasi target untuk jalur inflamasi dan stres oksidatif
• Studi farmakologi dan toksikologi yang mendukung IND
Parameter |
Model COPD Tikus |
Model COPD Tikus |
Spesies/Strain |
tikus C57BL/6 |
Tikus Sprague-Dawley |
Metode induksi |
Paparan asap rokok kronis (seluruh tubuh atau hidung saja) 5 hari/minggu selama 4–6 bulan + LPS intratrakeal (1–2 kali/minggu) |
|
Durasi studi |
4–7 bulan (induksi + pengobatan) |
4–7 bulan (induksi + pengobatan) |
Titik akhir yang penting |
Berat badan, jumlah sel BALF (total dan diferensial: makrofag, monosit, neutrofil), fungsi paru-paru (resistensi, kepatuhan, Penh), histopatologi (skor HE untuk emfisema dan peradangan), kadar sitokin pada BALF (IL-6, TNF-α, MCP-1), opsional: penanda stres oksidatif, metaplasia sel goblet (PAS), mean linear intersep (MLI) | |
Paket data |
Data mentah, laporan analisis, sitologi BALF, data fungsi paru, slide histologi, hasil ELISA, bioinformatika (opsional) | |
T: Mengapa asap rokok dan LPS digabungkan dalam model COPD?
J: Asap rokok menyebabkan peradangan kronis dan emfisema, sedangkan LPS (meniru infeksi bakteri) memperburuk peradangan saluran napas dan produksi lendir. Kombinasi ini lebih mirip dengan patologi PPOK pada manusia, termasuk eksaserbasi akut.
T: Apa persamaan utamanya dengan COPD pada manusia?
J: Model ini menunjukkan obstruksi aliran udara progresif, peradangan saluran napas (makrofag, neutrofil), emfisema, metaplasia sel goblet, dan efek sistemik, yang sangat mirip dengan PPOK pada manusia.
T: Apakah model ini dapat digunakan untuk studi yang mendukung IND?
J: Ya. Studi dapat dilakukan sesuai dengan prinsip GLP untuk pengajuan regulasi (FDA, EMA).
T: Apakah Anda menawarkan protokol penelitian yang disesuaikan (misalnya, durasi paparan asap yang berbeda, dosis LPS)?
J: Tentu saja. Tim ilmiah kami menyesuaikan protokol paparan asap, dosis LPS, dan analisis titik akhir untuk kandidat obat spesifik Anda.
