| Beschikbaarheid: | |
|---|---|
| Aantal: | |











Klinisch relevant – Gecombineerde blootstelling aan sigarettenrook en LPS bootst de menselijke COPD-etiologie en chronische ontstekingen na.
Meerdere soorten – Muis- en rattenmodellen beschikbaar om aan verschillende experimentele vereisten te voldoen (genetische hulpmiddelen versus groter formaat).
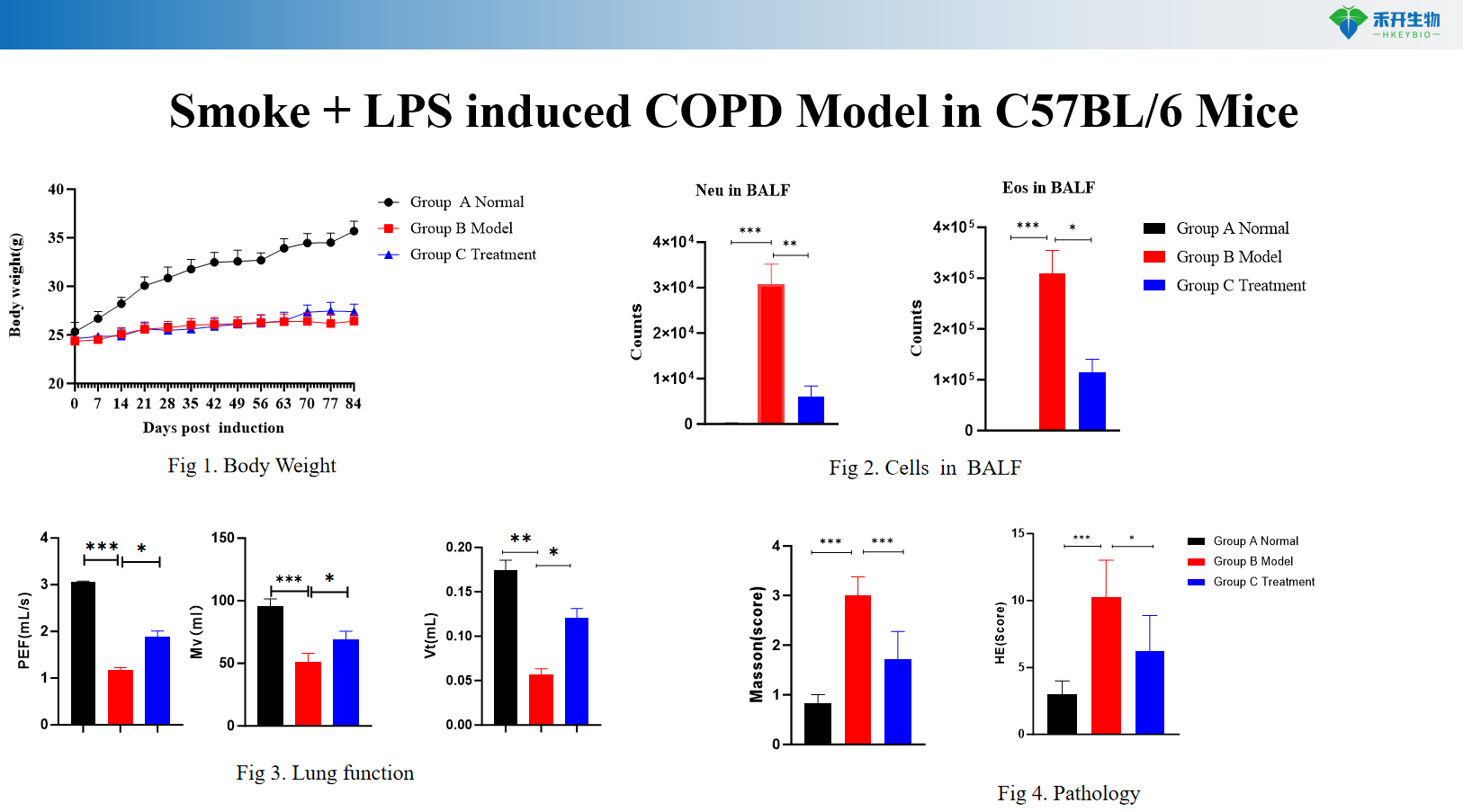
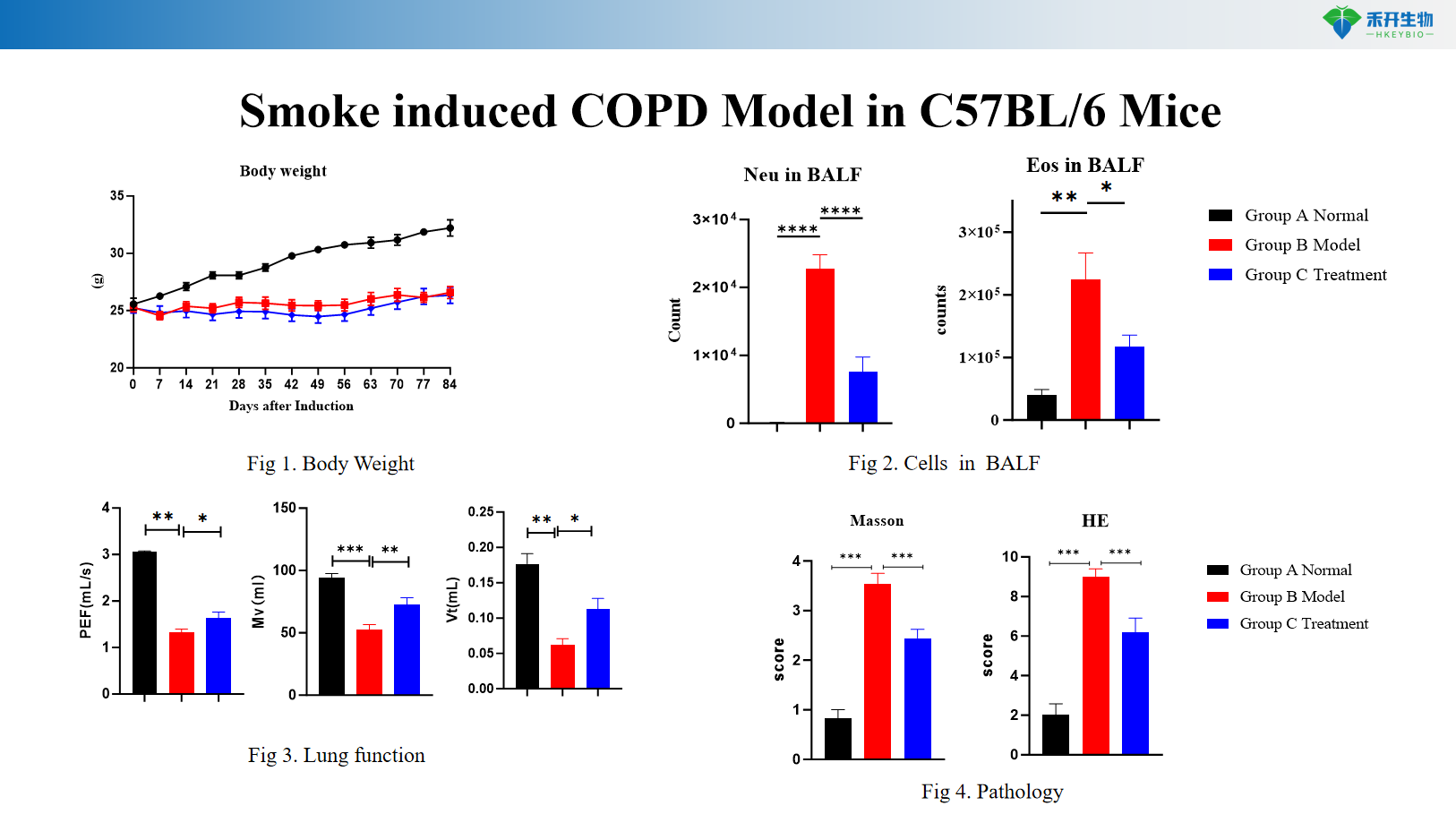
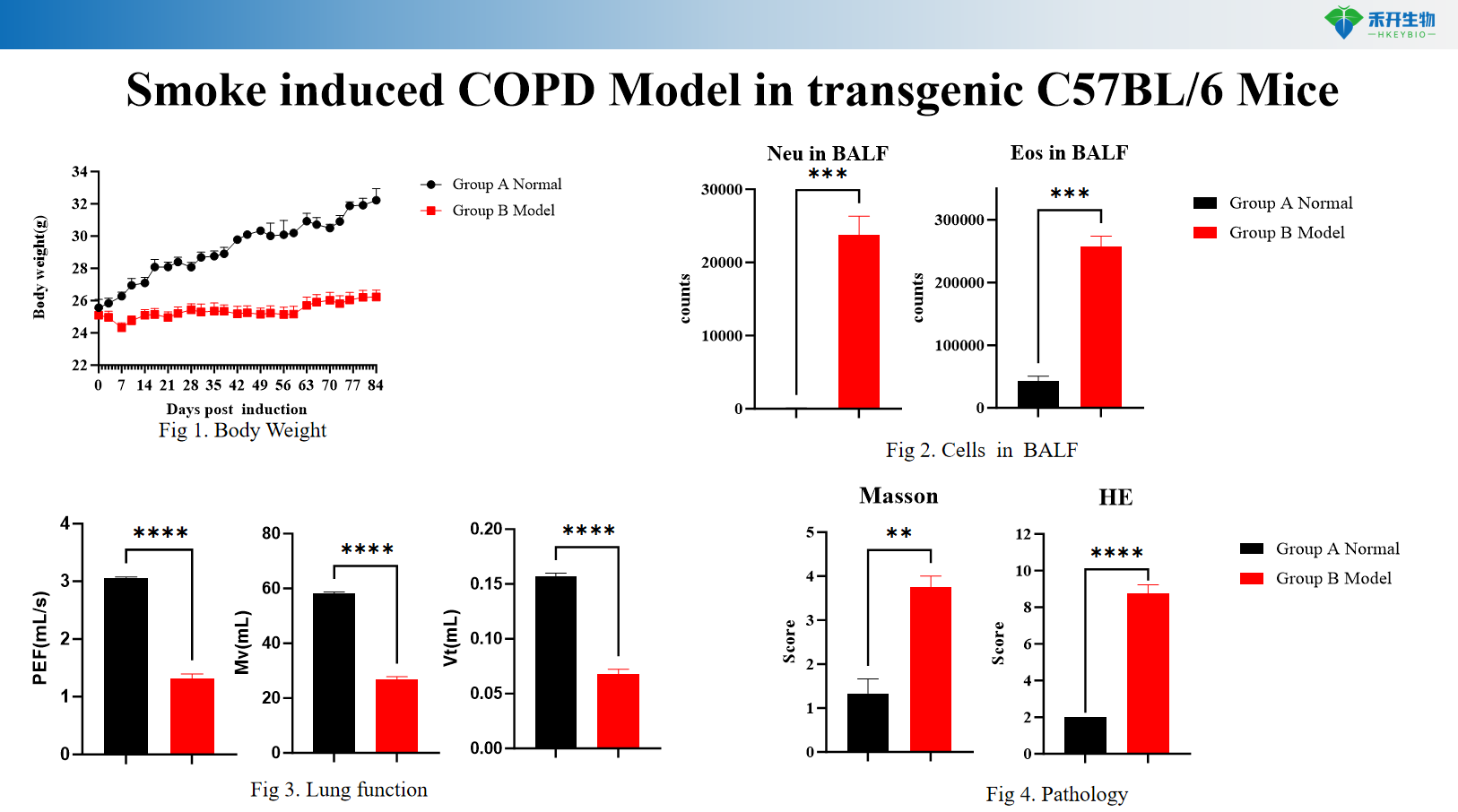
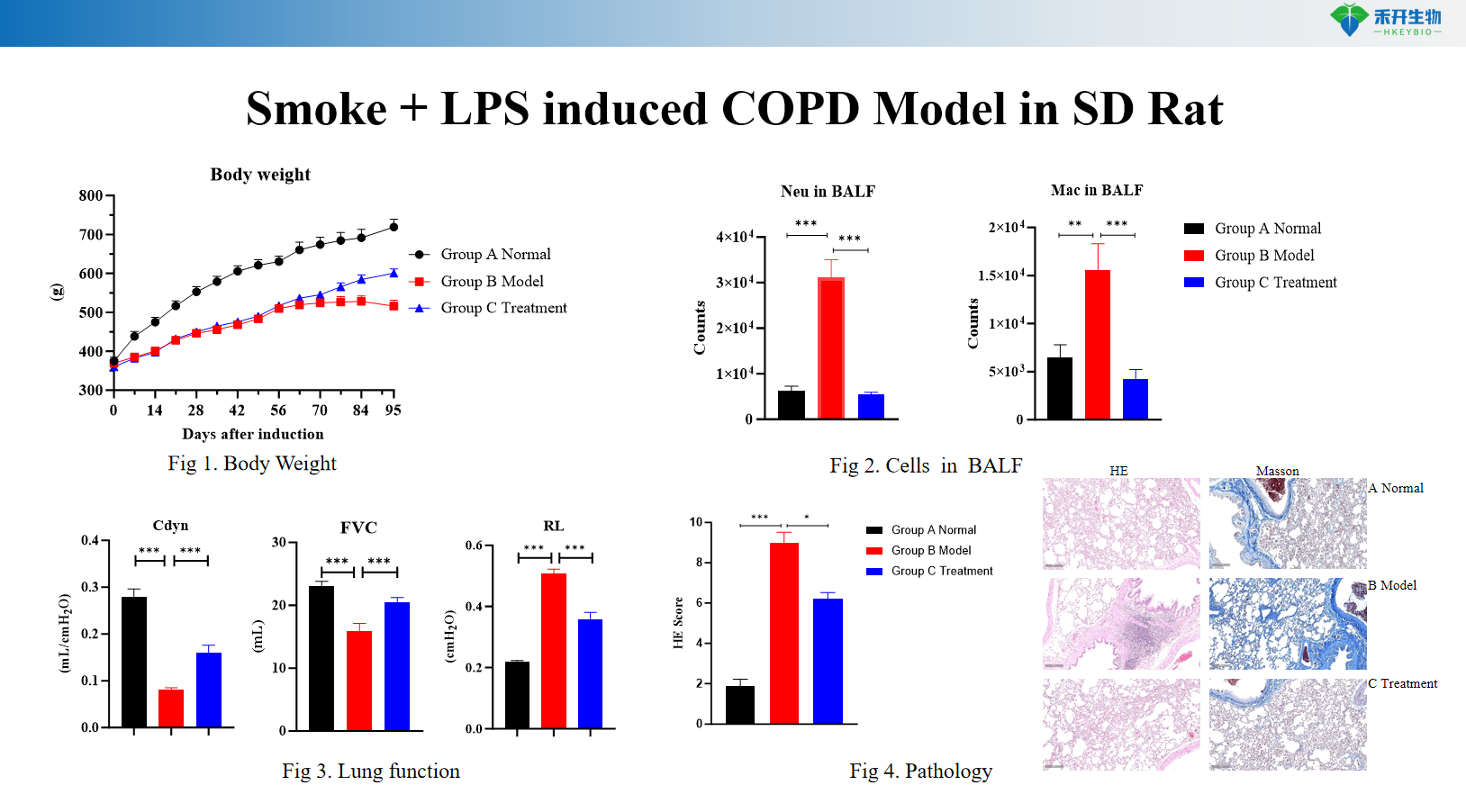
Uitgebreide eindpunten – Lichaamsgewicht, BALF-cytologie (WBC, macrofagen, monocyten), longfunctie (resistentie, compliantie), histopathologie (HE-score), cytokineprofilering.
Translationele waarde – Ideaal voor het testen van ontstekingsremmende medicijnen (corticosteroïden, PDE4-remmers), luchtwegverwijders en mucolytica.
IND-ready datapakketten – Onderzoeken kunnen worden uitgevoerd volgens GLP-principes.
Rook + LPS-geïnduceerd COPD-model in C57BL/6-muizen
Rookgeïnduceerd COPD-model bij C57BL/6-muizen
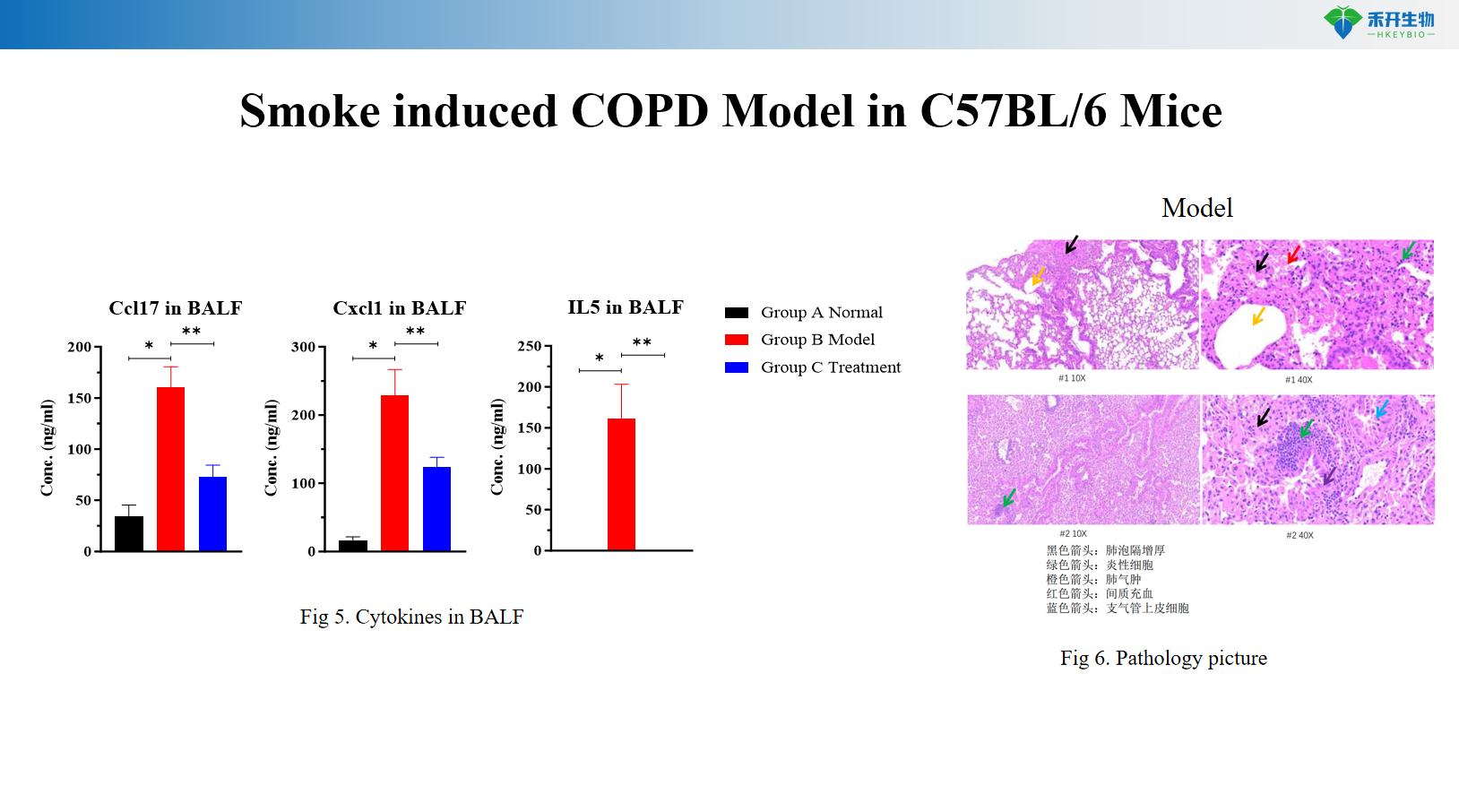
Door rook geïnduceerd COPD-model in transgene C57BL/6-muizen
Rook + LPS-geïnduceerd COPD-model in SD Rat
• Werkzaamheidstesten van ontstekingsremmende geneesmiddelen (corticosteroïden, PDE4-remmers, p38 MAPK-remmers)
• Evaluatie van luchtwegverwijders (β2-agonisten, anticholinergica) en combinatietherapieën
• Testen van mucoactieve stoffen en antioxidanten
• Doelvalidatie voor inflammatoire en oxidatieve stressroutes
• Farmacologische en toxicologische onderzoeken die IND mogelijk maken
Parameter |
COPD-model van de muis |
COPD-model van ratten |
Soort/stam |
C57BL/6 muis |
Sprague-Dawley-rat |
Inductiemethode |
Chronische blootstelling aan sigarettenrook (gehele lichaam of alleen de neus) 5 dagen/week gedurende 4–6 maanden + intratracheale LPS (1–2 keer/week) |
|
Studieduur |
4–7 maanden (inductie + behandeling) |
4–7 maanden (inductie + behandeling) |
Belangrijkste eindpunten |
Lichaamsgewicht, BALF-celaantallen (totaal en differentieel: macrofagen, monocyten, neutrofielen), longfunctie (resistentie, compliantie, Penh), histopathologie (HE-score voor emfyseem en ontsteking), cytokineniveaus in BALF (IL-6, TNF-α, MCP-1), optioneel: oxidatieve stressmarkers, bekercelmetaplasie (PAS), gemiddelde lineaire intercept (MLI) | |
Datapakket |
Ruwe gegevens, analyserapporten, BALF-cytologie, longfunctiegegevens, histologieglaasjes, ELISA-resultaten, bio-informatica (optioneel) | |
Vraag: Waarom sigarettenrook en LPS combineren in het COPD-model?
A: Sigarettenrook veroorzaakt chronische ontstekingen en emfyseem, terwijl LPS (dat een bacteriële infectie nabootst) de luchtwegontsteking en de slijmproductie verergert. De combinatie repliceert de menselijke COPD-pathologie beter, inclusief acute exacerbaties.
Vraag: Wat zijn de belangrijkste overeenkomsten met COPD bij mensen?
A: De modellen vertonen progressieve luchtwegobstructie, luchtwegontsteking (macrofagen, neutrofielen), emfyseem, slijmbekercelmetaplasie en systemische effecten, die sterk lijken op menselijk COPD.
Vraag: Kunnen deze modellen worden gebruikt voor onderzoeken die de IND mogelijk maken?
EEN: Ja. Studies kunnen worden uitgevoerd in overeenstemming met de GLP-principes voor indieningen bij de regelgevende instanties (FDA, EMA).
Vraag: Bieden jullie op maat gemaakte onderzoeksprotocollen aan (bijvoorbeeld verschillende blootstellingsduur aan rook, LPS-doses)?
EEN: Absoluut. Ons wetenschappelijk team stemt protocollen voor blootstelling aan rook, LPS-dosering en eindpuntanalyses af op uw specifieke kandidaat-geneesmiddel.
