| Disponibilidad: | |
|---|---|
| Cantidad: | |











Clínicamente relevante : la exposición combinada al humo del cigarrillo y al LPS imita la etiología humana de la EPOC y la inflamación crónica.
Múltiples especies : modelos de ratones y ratas disponibles para adaptarse a diferentes requisitos experimentales (herramientas genéticas versus mayor tamaño).
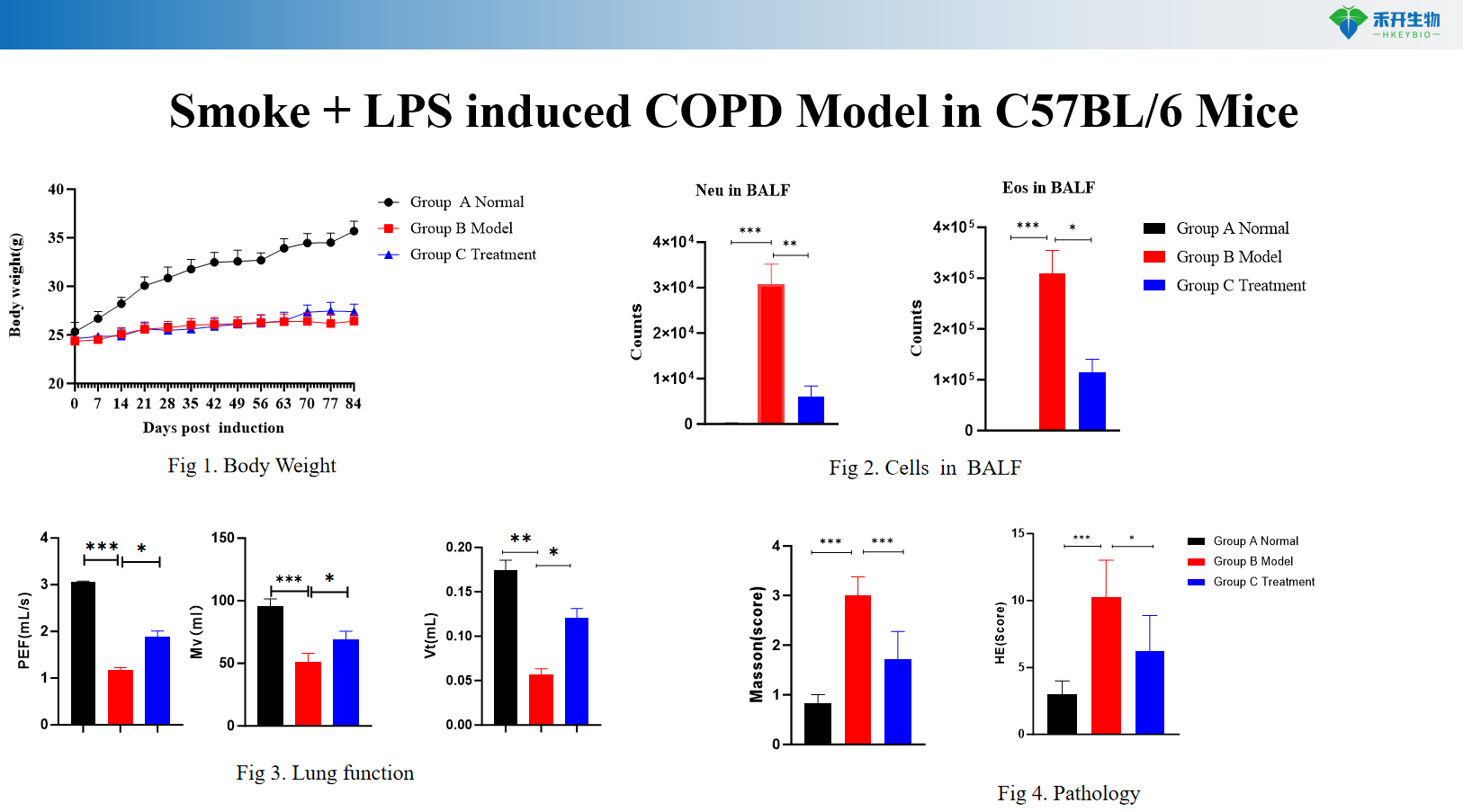
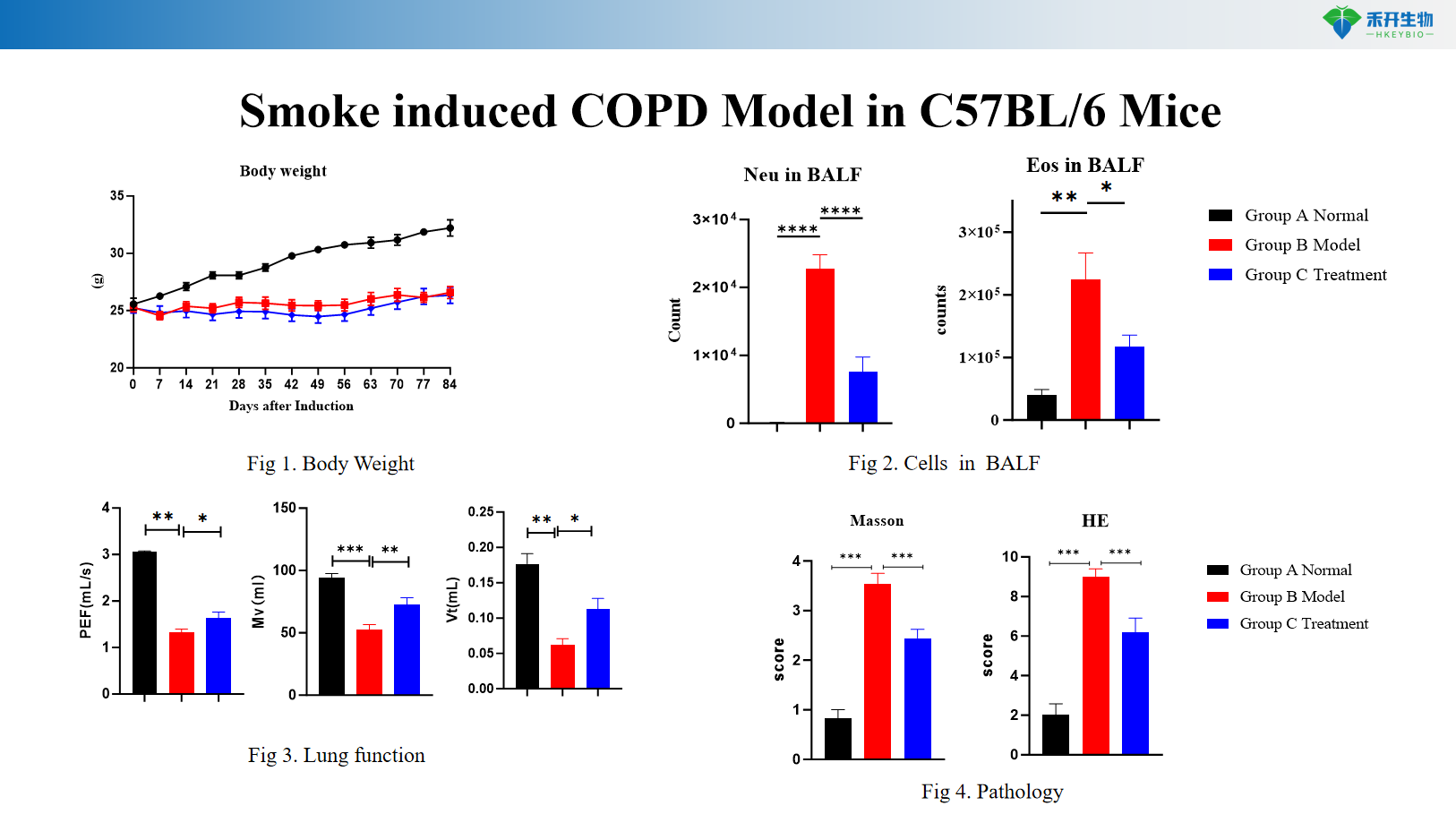
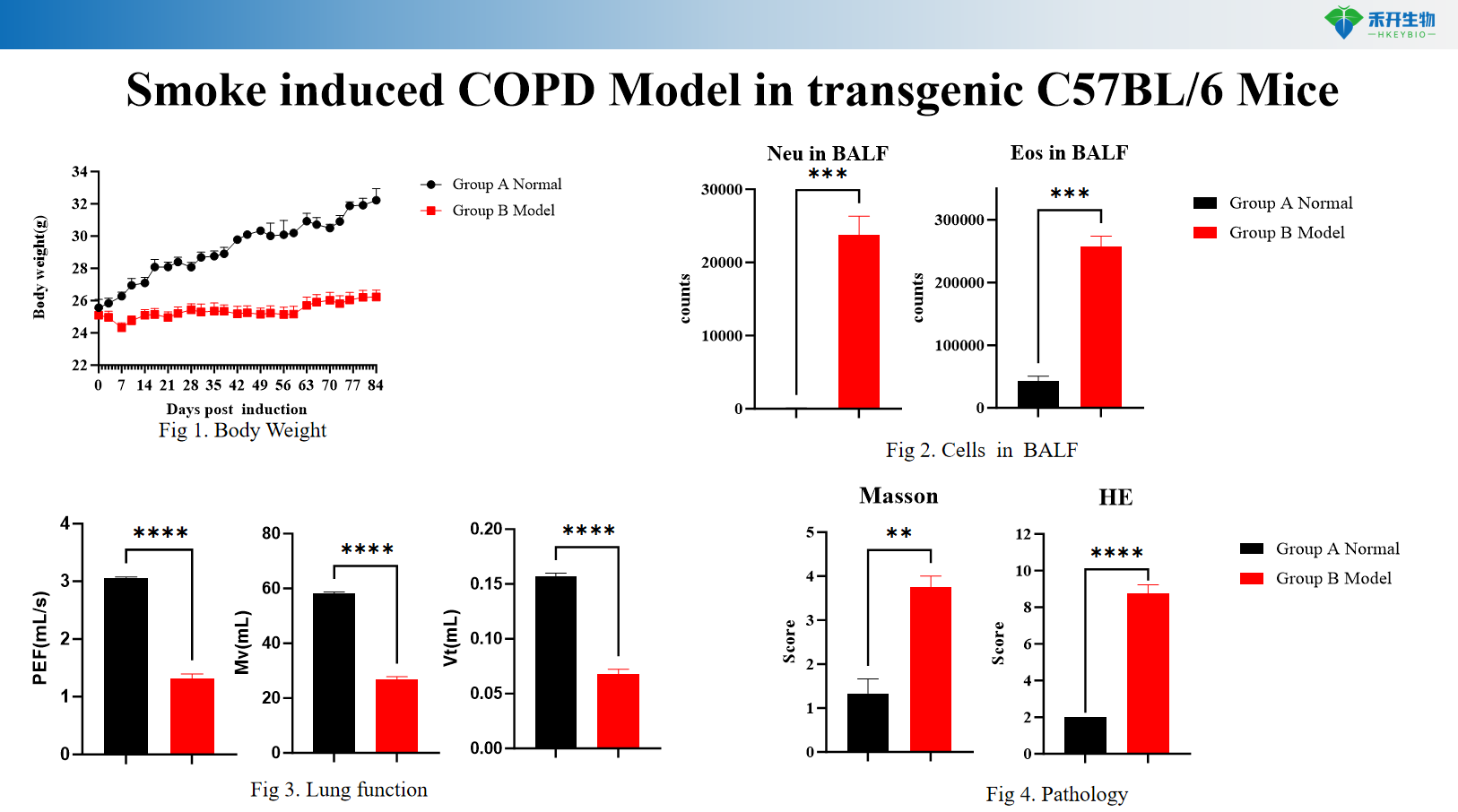
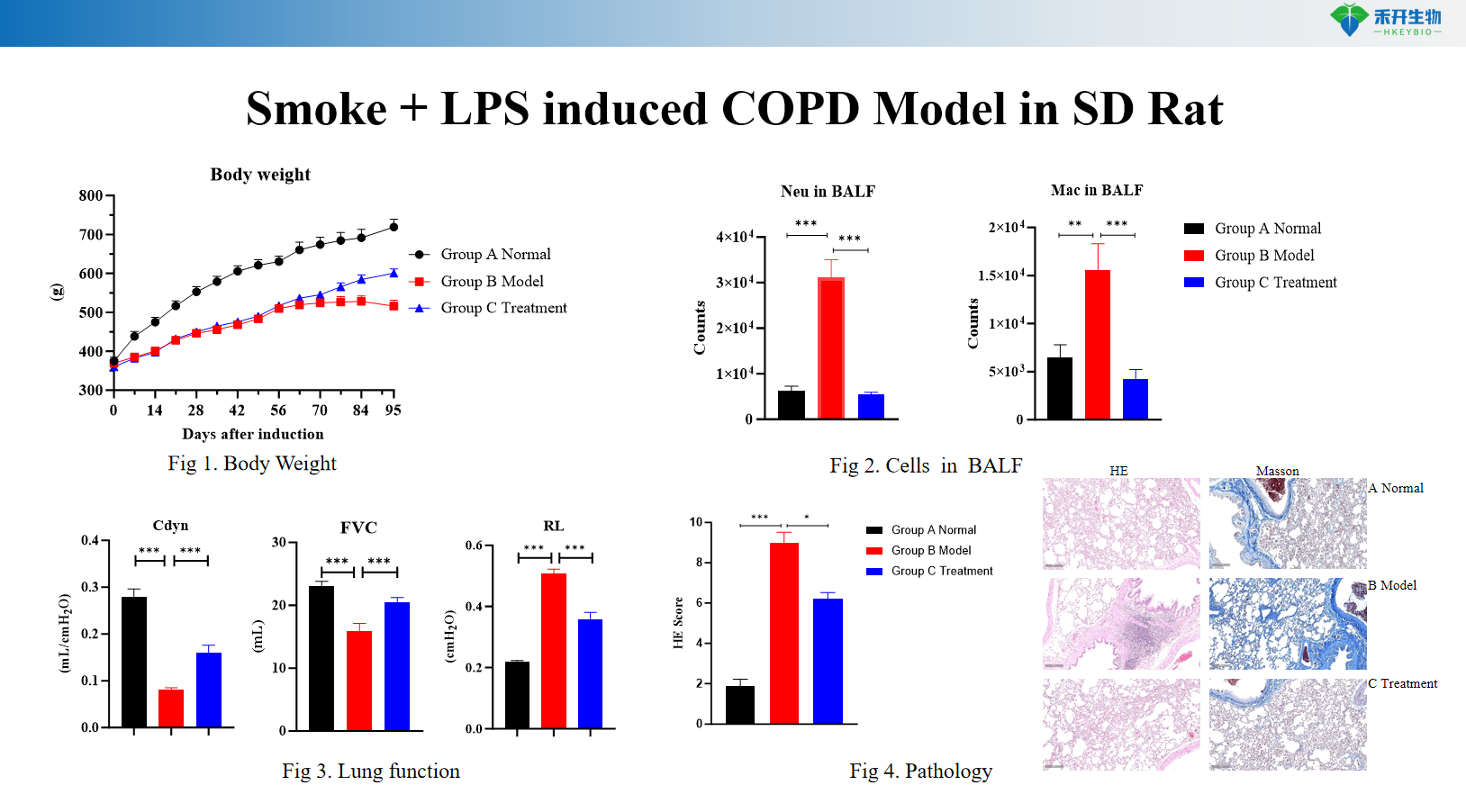
Criterios de valoración integrales : peso corporal, citología BALF (leucocitos, macrófagos, monocitos), función pulmonar (resistencia, cumplimiento), histopatología (puntuación HE), perfil de citocinas.
Valor traslacional : ideal para probar medicamentos antiinflamatorios (corticosteroides, inhibidores de la PDE4), broncodilatadores y mucolíticos.
Paquetes de datos preparados para IND : los estudios se pueden realizar de acuerdo con los principios GLP.
Modelo de EPOC inducida por humo + LPS en ratones C57BL/6
Modelo de EPOC inducida por humo en ratones C57BL/6
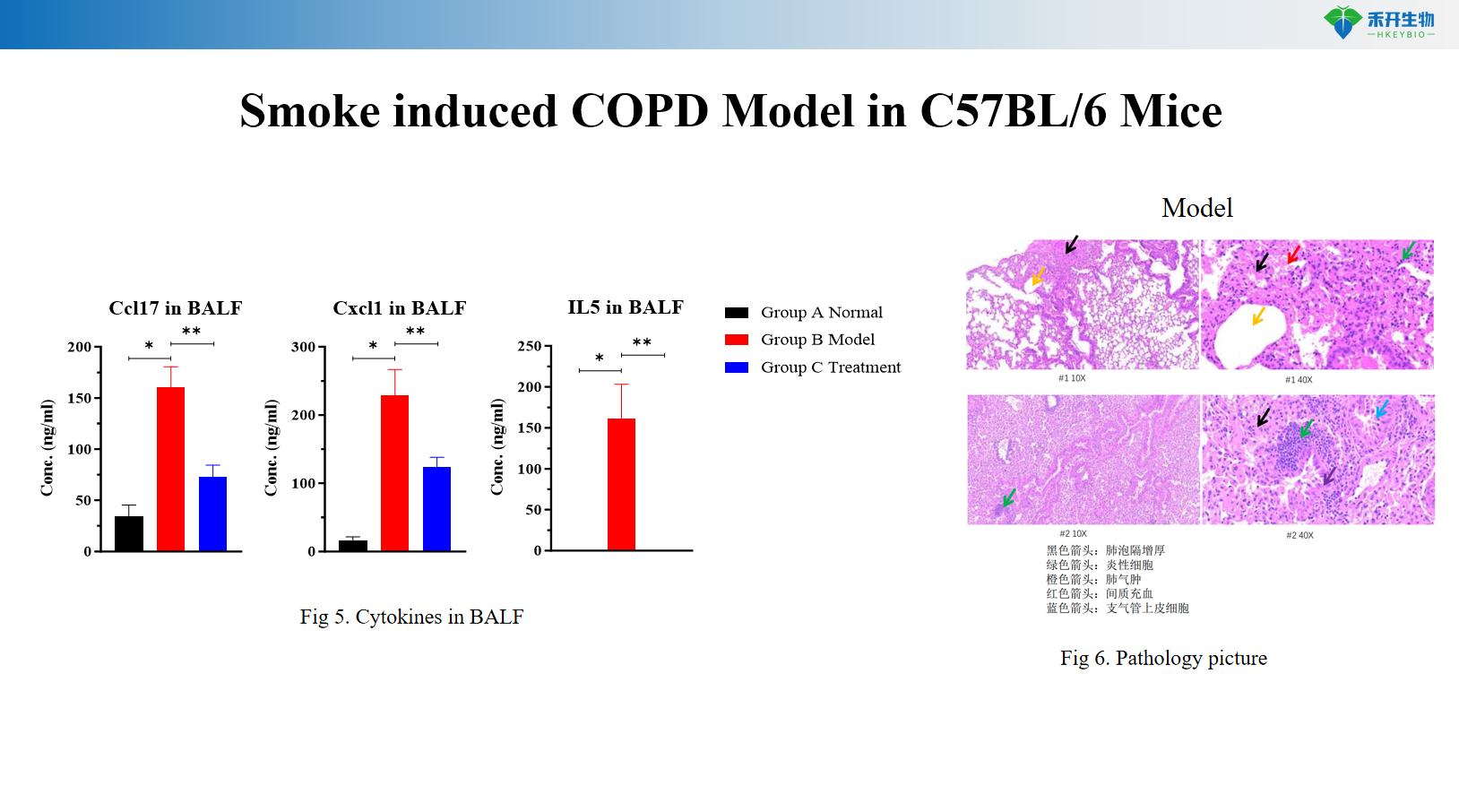
Modelo de EPOC inducida por humo en ratones transgénicos C57BL/6
Modelo de EPOC inducida por humo + LPS en rata SD
• Pruebas de eficacia de medicamentos antiinflamatorios (corticosteroides, inhibidores de PDE4, inhibidores de p38 MAPK)
• Evaluación de broncodilatadores (agonistas β2, anticolinérgicos) y terapias combinadas
• Pruebas de agentes mucoactivos y antioxidantes.
• Validación de objetivos para las vías de estrés inflamatorio y oxidativo
• Estudios de farmacología y toxicología que permitan el IND
Parámetro |
Modelo de EPOC de ratón |
Modelo de EPOC en ratas |
Especie/Cepa |
Ratón C57BL/6 |
Rata Sprague-Dawley |
Método de inducción |
Exposición crónica al humo del cigarrillo (de todo el cuerpo o sólo de la nariz) 5 días/semana durante 4 a 6 meses + LPS intratraqueal (1 a 2 veces/semana) |
|
Duración del estudio |
4-7 meses (inducción + tratamiento) |
4-7 meses (inducción + tratamiento) |
Puntos finales clave |
Peso corporal, recuento de células BALF (total y diferencial: macrófagos, monocitos, neutrófilos), función pulmonar (resistencia, distensibilidad, Penh), histopatología (puntuación HE para enfisema e inflamación), niveles de citoquinas en BALF (IL-6, TNF-α, MCP-1), opcional: marcadores de estrés oxidativo, metaplasia de células caliciformes (PAS), intercepción lineal media (MLI) | |
Paquete de datos |
Datos brutos, informes de análisis, citología BALF, datos de función pulmonar, portaobjetos de histología, resultados de ELISA, bioinformática (opcional) | |
P: ¿Por qué combinar el humo del cigarrillo y el LPS en el modelo de EPOC?
R: El humo del cigarrillo induce inflamación crónica y enfisema, mientras que el LPS (que imita una infección bacteriana) exacerba la inflamación de las vías respiratorias y la producción de moco. La combinación replica más fielmente la patología de la EPOC humana, incluidas las exacerbaciones agudas.
P: ¿Cuáles son las similitudes clave con la EPOC humana?
R: Los modelos exhiben obstrucción progresiva del flujo de aire, inflamación de las vías respiratorias (macrófagos, neutrófilos), enfisema, metaplasia de células caliciformes y efectos sistémicos, muy parecidos a la EPOC humana.
P: ¿Se pueden utilizar estos modelos para estudios que permitan IND?
R: Sí. Los estudios se pueden realizar de acuerdo con los principios GLP para presentaciones regulatorias (FDA, EMA).
P: ¿Ofrecen protocolos de estudio personalizados (p. ej., diferentes duraciones de exposición al humo, dosis de LPS)?
R: Absolutamente. Nuestro equipo científico adapta los protocolos de exposición al humo, la dosificación de LPS y los análisis de criterios de valoración a su fármaco candidato específico.
