| Verfügbarkeit: | |
|---|---|
| Menge: | |











Klinisch relevant – Die Kombination aus Zigarettenrauch und LPS-Exposition ahmt die COPD-Ätiologie und chronische Entzündung beim Menschen nach.
Mehrere Arten – Maus- und Rattenmodelle verfügbar, um unterschiedlichen experimentellen Anforderungen gerecht zu werden (genetische Werkzeuge vs. größere Größe).
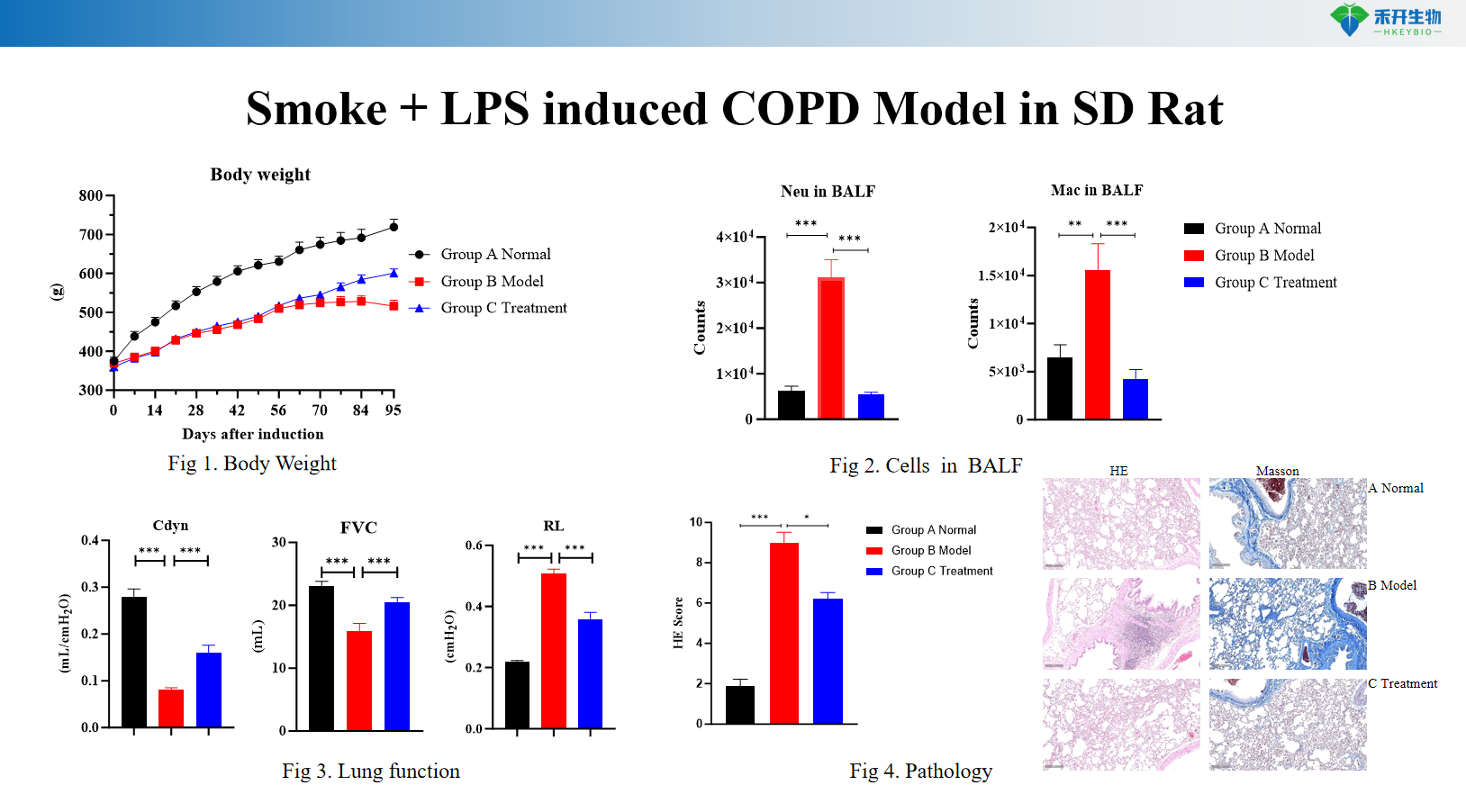
Umfassende Endpunkte – Körpergewicht, BALF-Zytologie (WBC, Makrophagen, Monozyten), Lungenfunktion (Resistenz, Compliance), Histopathologie (HE-Bewertung), Zytokinprofilierung.
Translationaler Wert – Ideal zum Testen entzündungshemmender Medikamente (Kortikosteroide, PDE4-Hemmer), Bronchodilatatoren und Mukolytika.
IND-fähige Datenpakete – Studien können gemäß den GLP-Grundsätzen durchgeführt werden.
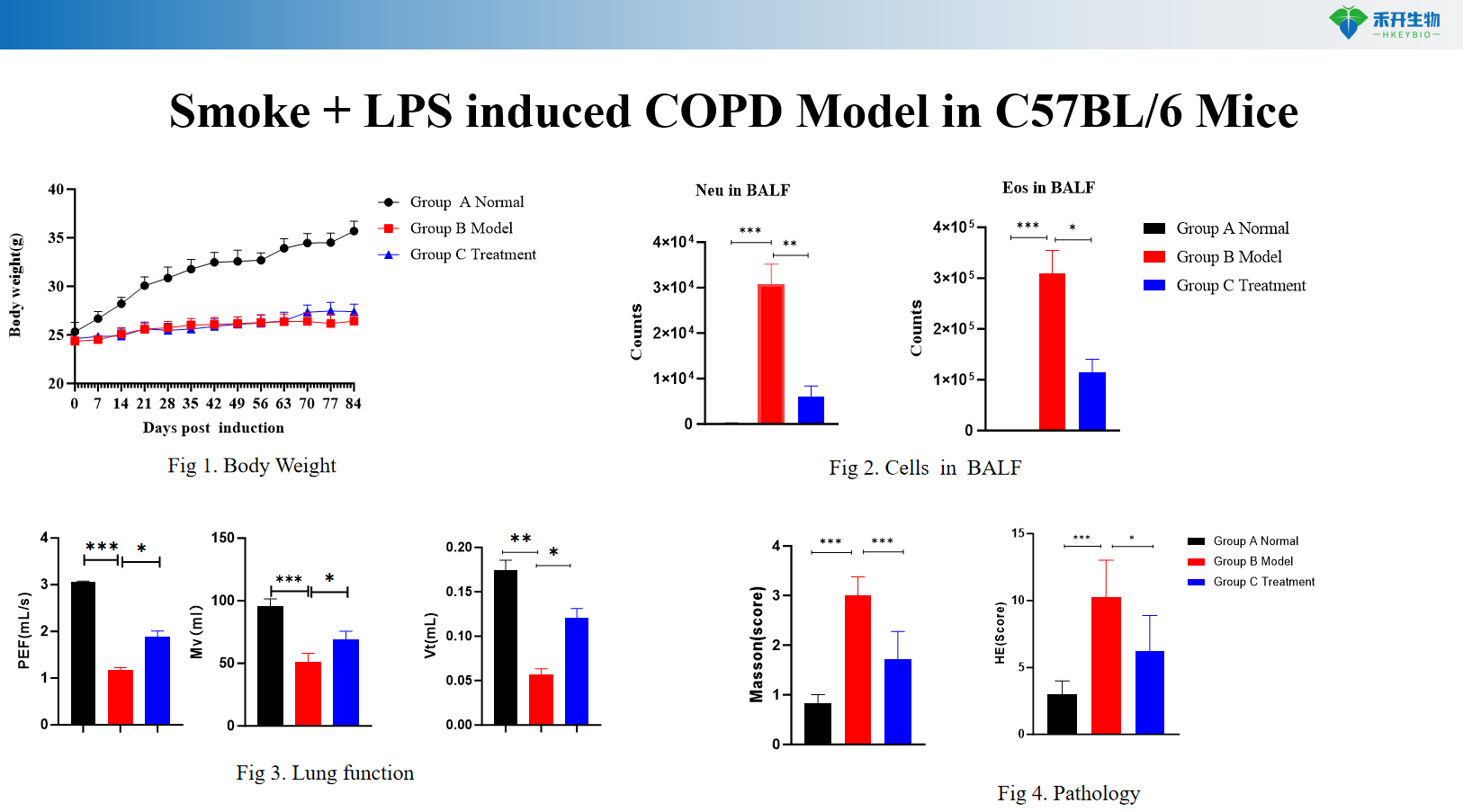
Rauch + LPS-induziertes COPD-Modell bei C57BL/6-Mäusen
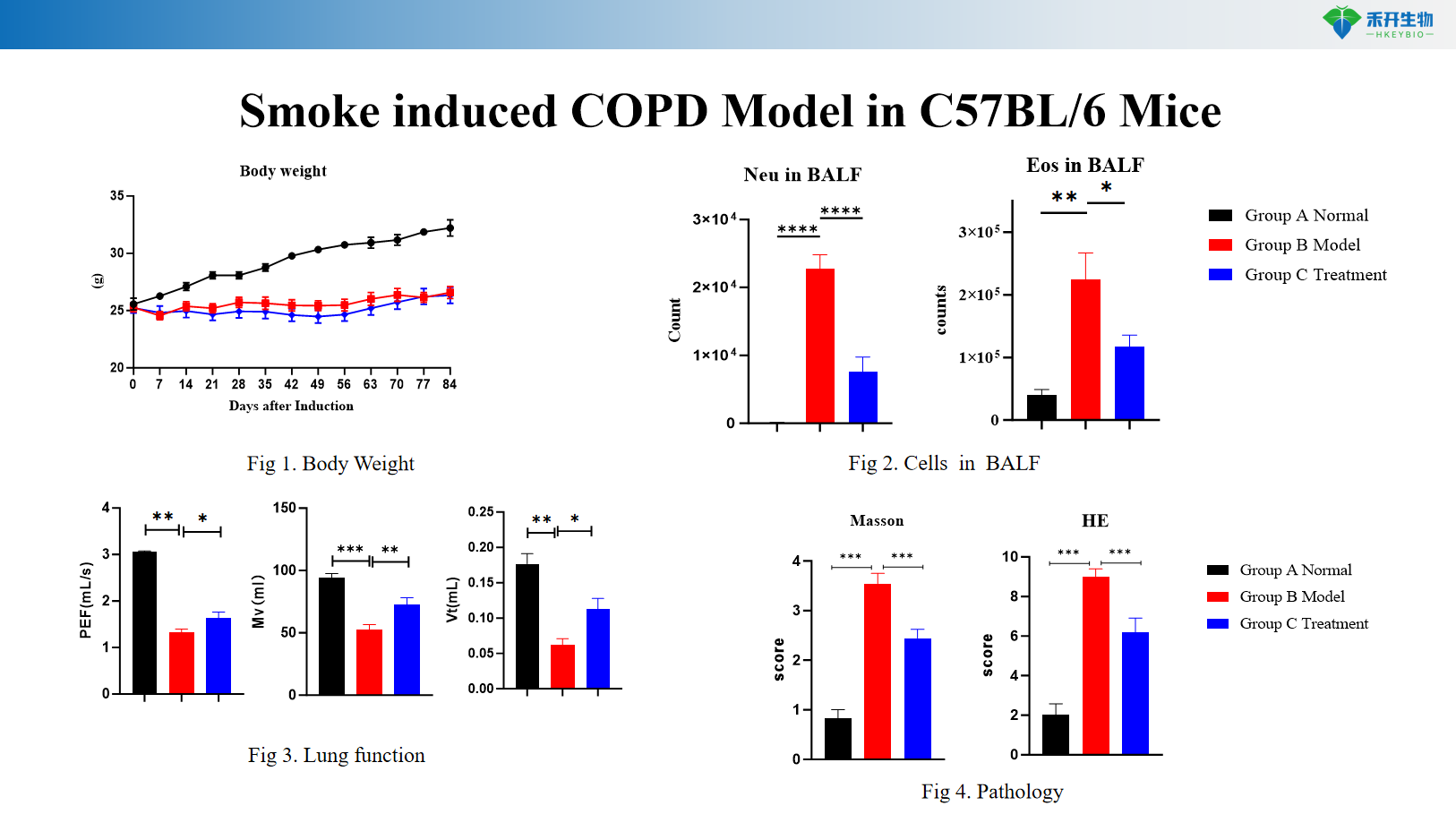
Rauchinduziertes COPD-Modell bei C57BL/6-Mäusen
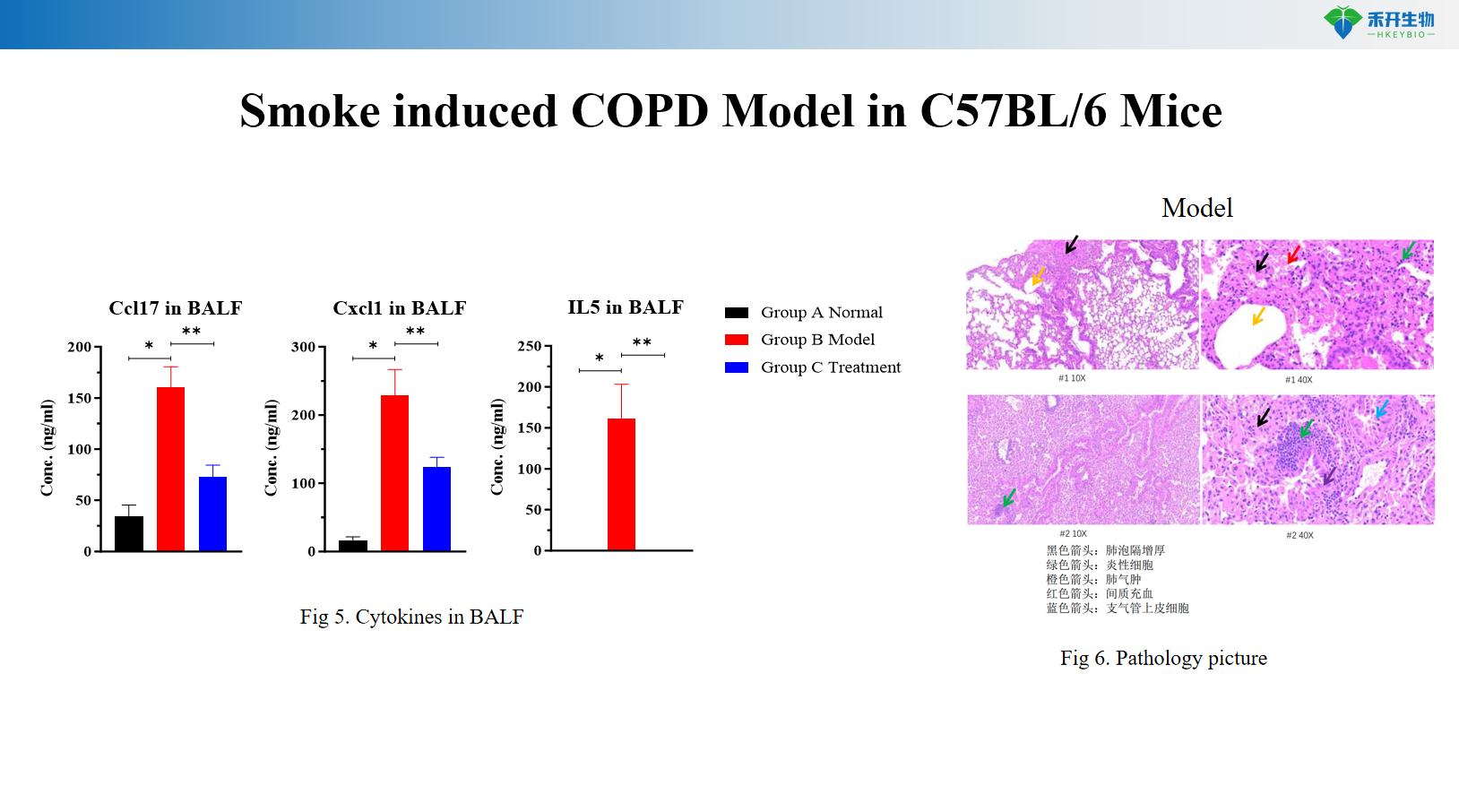
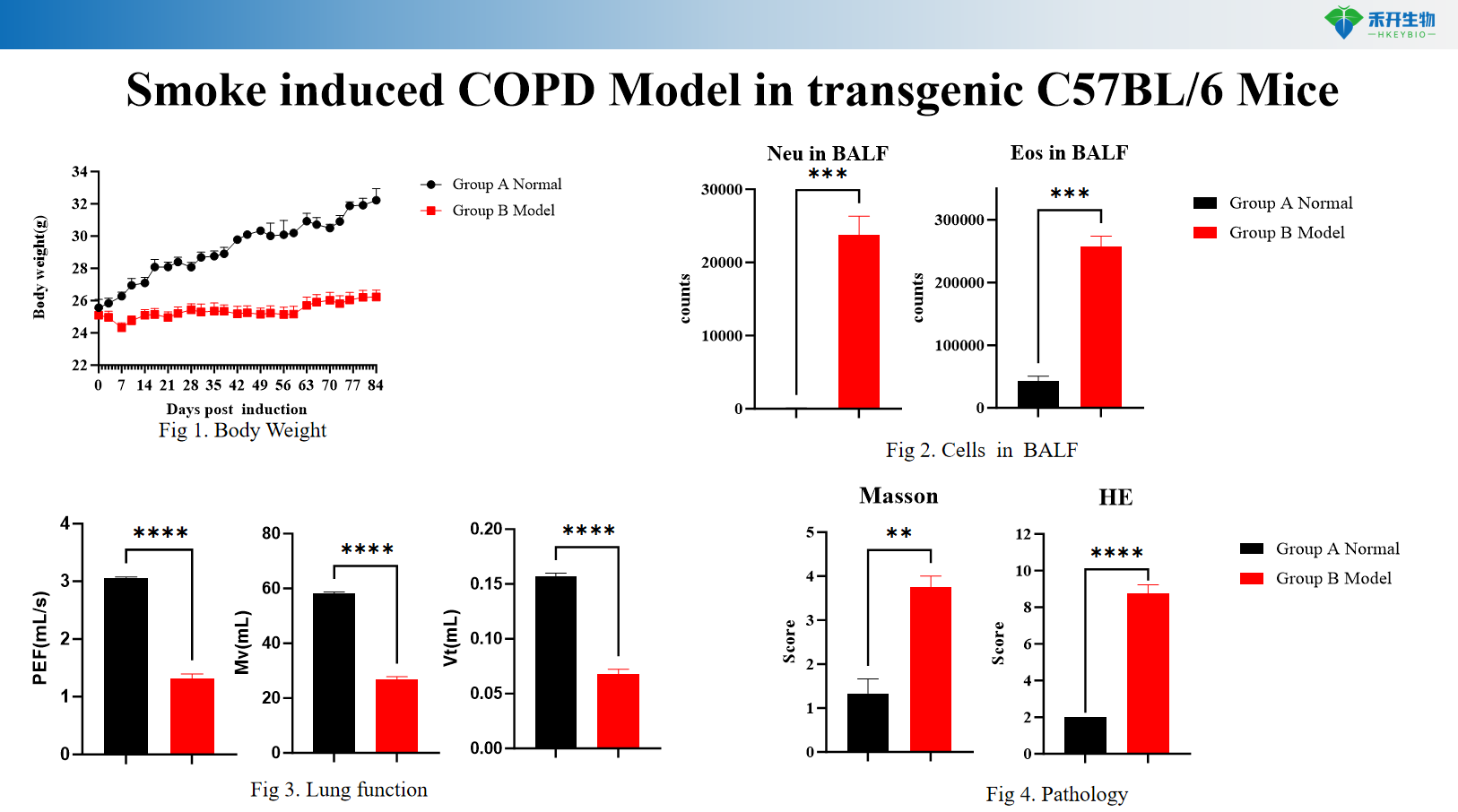
Rauchinduziertes COPD-Modell in transgenen C57BL/6-Mäusen
Rauch + LPS-induziertes COPD-Modell bei SD-Ratten
• Wirksamkeitsprüfung entzündungshemmender Medikamente (Kortikosteroide, PDE4-Inhibitoren, p38-MAPK-Inhibitoren)
• Bewertung von Bronchodilatatoren (β2-Agonisten, Anticholinergika) und Kombinationstherapien
• Prüfung von mukoaktiven Wirkstoffen und Antioxidantien
• Zielvalidierung für entzündliche und oxidative Stresswege
• IND-ermöglichende Pharmakologie- und Toxikologiestudien
Parameter |
Maus-COPD-Modell |
Ratten-COPD-Modell |
Art/Stamm |
C57BL/6-Maus |
Sprague-Dawley-Ratte |
Induktionsmethode |
Chronische Zigarettenrauchexposition (Ganzkörper oder nur Nase) 5 Tage/Woche für 4–6 Monate + intratracheales LPS (1–2 Mal/Woche) |
|
Studiendauer |
4–7 Monate (Einleitung + Behandlung) |
4–7 Monate (Einleitung + Behandlung) |
Wichtige Endpunkte |
Körpergewicht, BALF-Zellzahlen (gesamt und differenziell: Makrophagen, Monozyten, Neutrophile), Lungenfunktion (Resistenz, Compliance, Penh), Histopathologie (HE-Bewertung für Emphysem und Entzündung), Zytokinspiegel in BALF (IL-6, TNF-α, MCP-1), optional: Marker für oxidativen Stress, Becherzellmetaplasie (PAS), mittlerer linearer Achsenabschnitt (MLI) | |
Datenpaket |
Rohdaten, Analyseberichte, BALF-Zytologie, Lungenfunktionsdaten, Histologie-Objektträger, ELISA-Ergebnisse, Bioinformatik (optional) | |
F: Warum sollten Zigarettenrauch und LPS im COPD-Modell kombiniert werden?
A: Zigarettenrauch löst chronische Entzündungen und Emphyseme aus, während LPS (imitiert eine bakterielle Infektion) die Entzündung der Atemwege und die Schleimproduktion verschlimmert. Die Kombination bildet die menschliche COPD-Pathologie einschließlich akuter Exazerbationen besser nach.
F: Was sind die wichtigsten Gemeinsamkeiten mit der menschlichen COPD?
A: Die Modelle weisen eine fortschreitende Obstruktion des Luftstroms, eine Entzündung der Atemwege (Makrophagen, Neutrophile), ein Emphysem, eine Becherzellmetaplasie und systemische Effekte auf, die der menschlichen COPD sehr ähneln.
F: Können diese Modelle für IND-fähige Studien verwendet werden?
A: Ja. Studien können gemäß den GLP-Grundsätzen für Zulassungsanträge (FDA, EMA) durchgeführt werden.
F: Bieten Sie maßgeschneiderte Studienprotokolle an (z. B. unterschiedliche Rauchexpositionsdauern, LPS-Dosen)?
A: Absolut. Unser wissenschaftliches Team passt Rauchexpositionsprotokolle, LPS-Dosierung und Endpunktanalysen an Ihren spezifischen Medikamentenkandidaten an.
