| Tilgjengelighet: | |
|---|---|
| Antall: | |











Klinisk relevant – Kombinert sigarettrøyk og LPS-eksponering etterligner menneskelig KOLS-etiologi og kronisk betennelse.
Flere arter – Muse- og rottemodeller tilgjengelig for å dekke ulike eksperimentelle krav (genetiske verktøy vs. større størrelse).
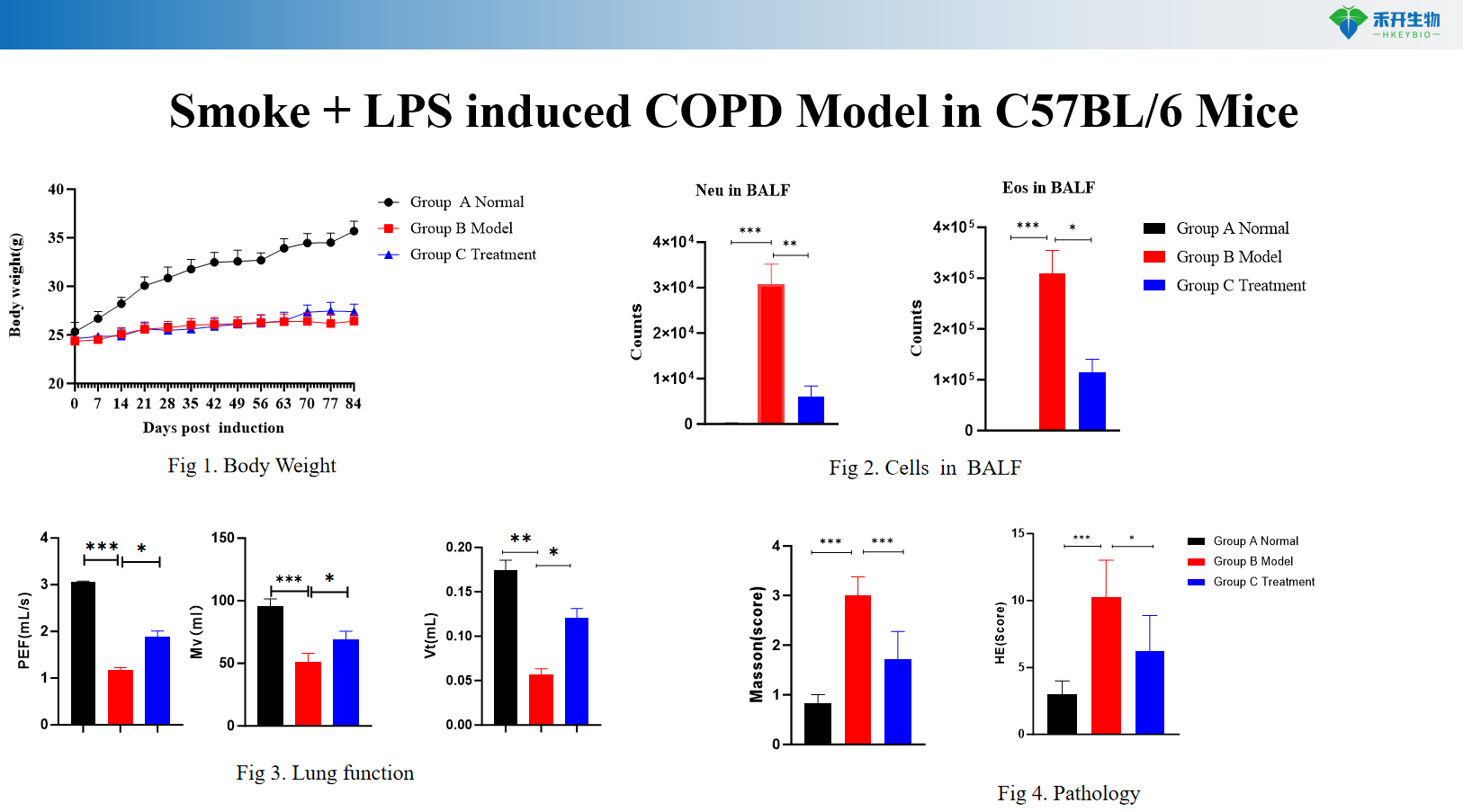
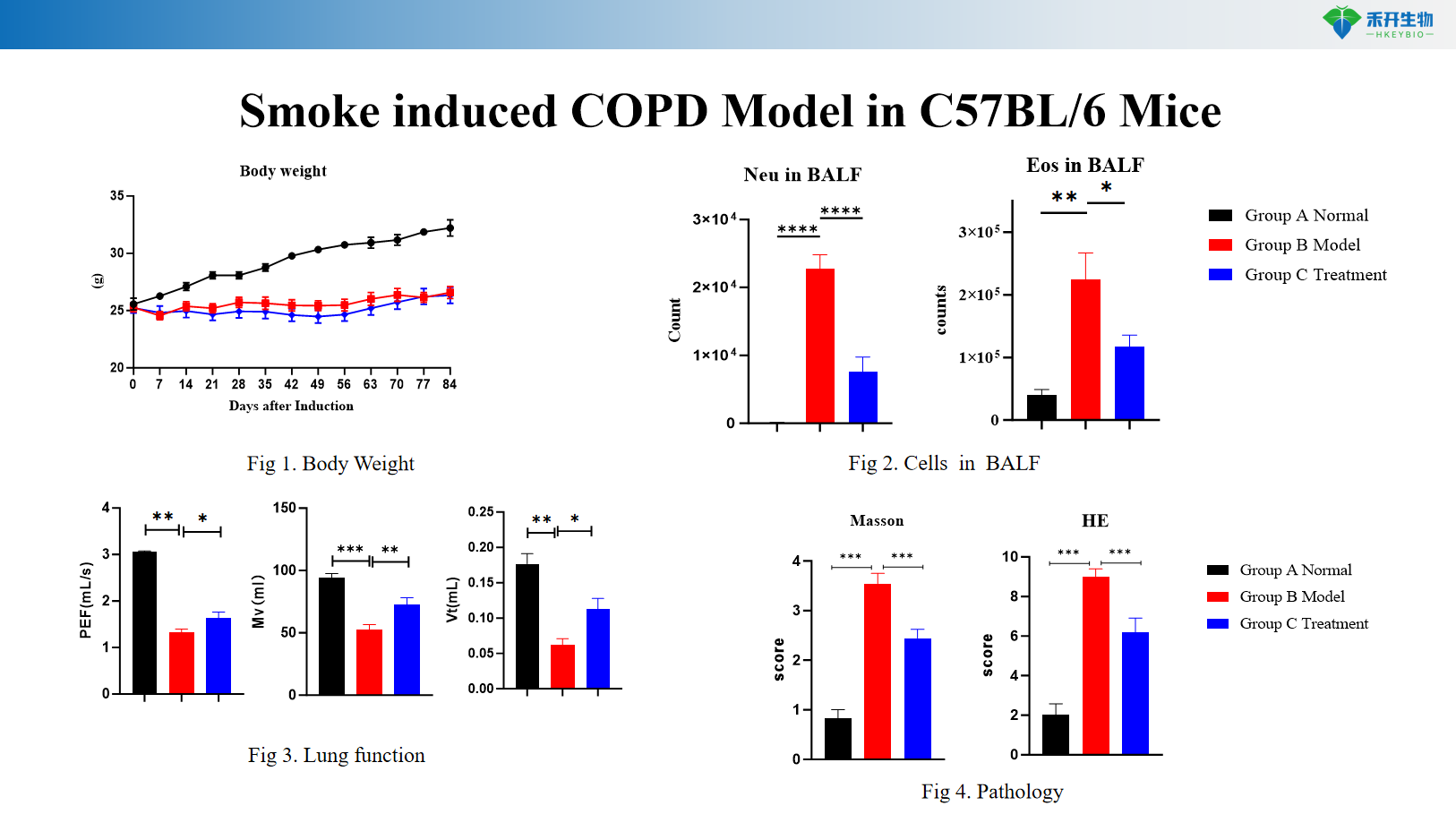
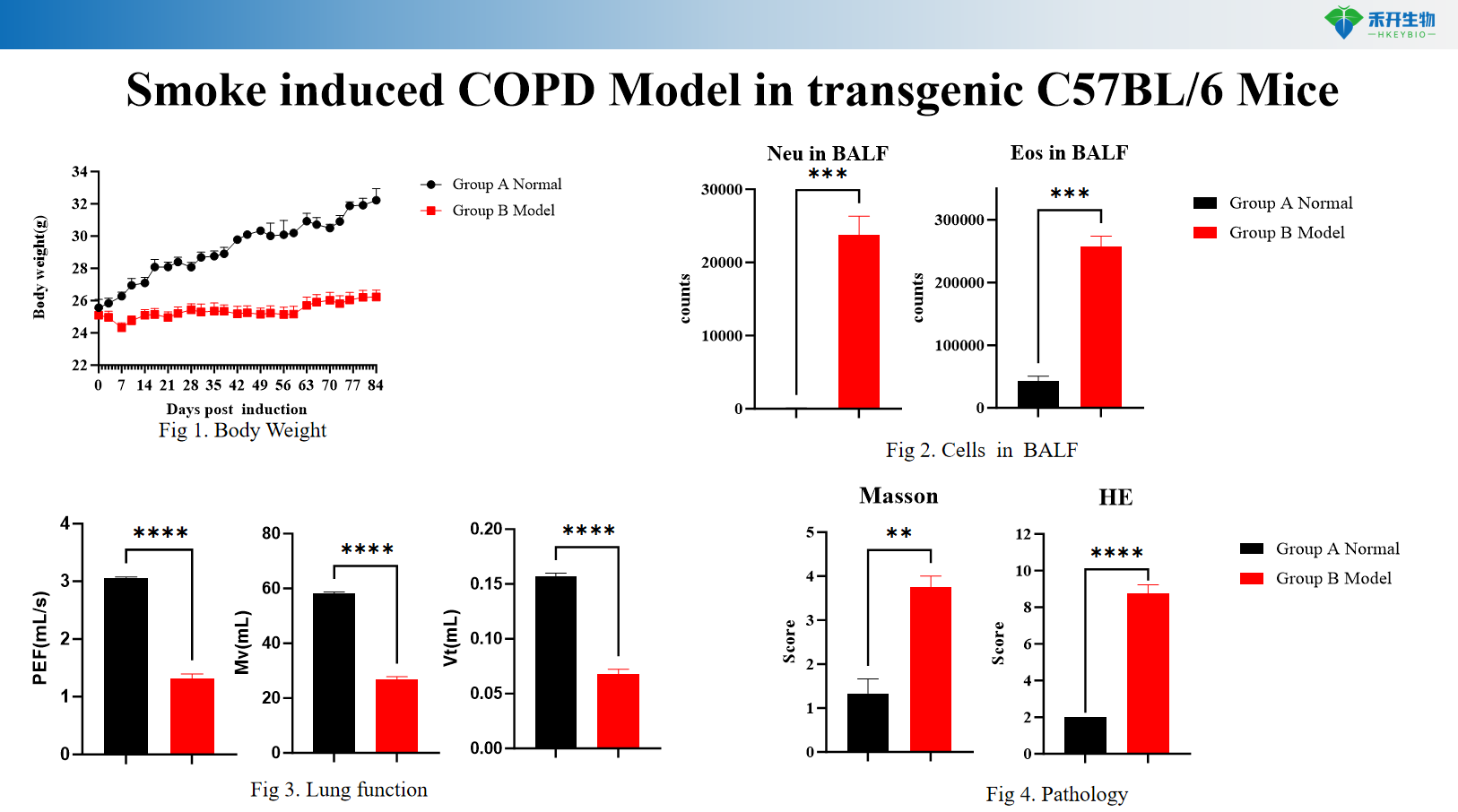
Omfattende endepunkter – Kroppsvekt, BALF-cytologi (WBC, makrofager, monocytter), lungefunksjon (resistens, compliance), histopatologi (HE-scoring), cytokinprofilering.
Translasjonsverdi – Ideell for testing av antiinflammatoriske legemidler (kortikosteroider, PDE4-hemmere), bronkodilatatorer og mukolytika.
IND-klare datapakker – Studier kan utføres i henhold til GLP-prinsipper.
Røyk + LPS-indusert KOLS-modell i C57BL/6-mus
Røykindusert KOLS-modell i C57BL/6-m
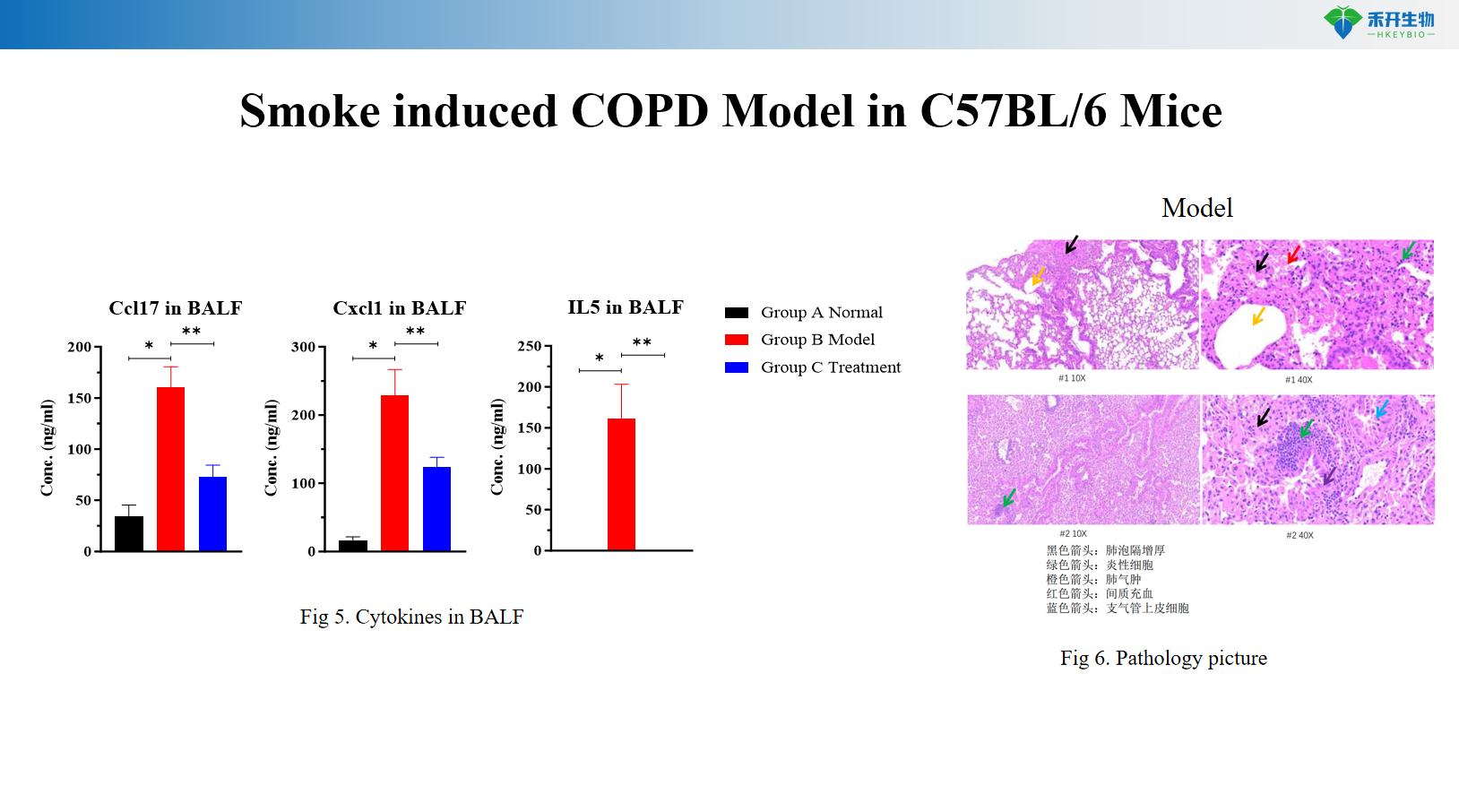
Røykindusert KOLS-modell i transgene C57BL/6-mus
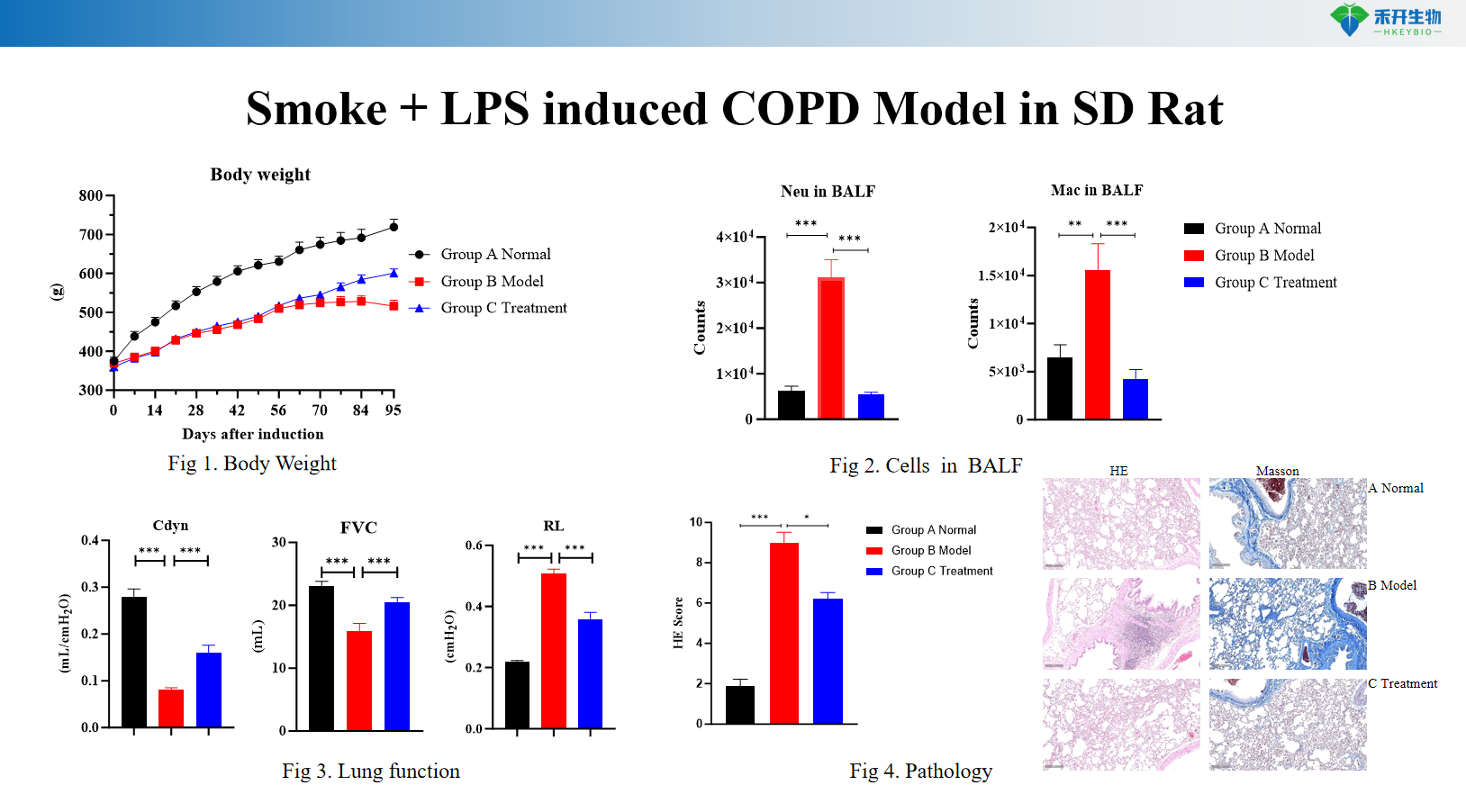
Røyk + LPS-indusert KOLS-modell i SD-rotte
• Effekttesting av antiinflammatoriske legemidler (kortikosteroider, PDE4-hemmere, p38 MAPK-hemmere)
• Evaluering av bronkodilatatorer (β2-agonister, antikolinergika) og kombinasjonsbehandlinger
• Testing av mukoaktive midler og antioksidanter
• Målvalidering for inflammatoriske og oksidative stressveier
• IND-aktiverende farmakologi og toksikologistudier
Parameter |
Mus KOLS-modell |
Rotte KOLS-modell |
Arter/Stamme |
C57BL/6 mus |
Sprague-Dawley rotte |
Induksjonsmetode |
Kronisk eksponering for sigarettrøyk (kun for hele kroppen eller nesen) 5 dager/uke i 4–6 måneder + intratrakeal LPS (1–2 ganger/uke) |
|
Studievarighet |
4–7 måneder (induksjon + behandling) |
4–7 måneder (induksjon + behandling) |
Viktige endepunkter |
Kroppsvekt, BALF-celletall (totalt og differensielt: makrofager, monocytter, nøytrofiler), lungefunksjon (resistens, compliance, Penh), histopatologi (HE-skåring for emfysem og betennelse), cytokinnivåer i BALF (IL-6, TNF-α, MCP-1), valgfritt: oksidative stress-meta-markører (PAS-celle-markører), interplasiacellebeger (PAS) | |
Datapakke |
Rådata, analyserapporter, BALF-cytologi, lungefunksjonsdata, histologiske lysbilder, ELISA-resultater, bioinformatikk (valgfritt) | |
Spørsmål: Hvorfor kombinere sigarettrøyk og LPS i KOLS-modellen?
A: Sigarettrøyk induserer kronisk betennelse og emfysem, mens LPS (etterligner bakteriell infeksjon) forverrer luftveisbetennelse og slimproduksjon. Kombinasjonen gjenskaper tettere menneskelig KOLS-patologi, inkludert akutte eksacerbasjoner.
Spørsmål: Hva er de viktigste likhetene med menneskelig KOLS?
A: Modellene viser progressiv luftstrømsobstruksjon, luftveisbetennelse (makrofager, nøytrofiler), emfysem, begercellemetaplasi og systemiske effekter, som ligner mye på KOLS.
Spørsmål: Kan disse modellene brukes til IND-aktiverende studier?
A: Ja. Studier kan utføres i samsvar med GLP-prinsipper for regulatoriske innleveringer (FDA, EMA).
Spørsmål: Tilbyr du tilpassede studieprotokoller (f.eks. forskjellige røykeksponeringsvarigheter, LPS-doser)?
A: Absolutt. Vårt vitenskapelige team skreddersyr røykeksponeringsprotokoller, LPS-dosering og endepunktsanalyser til din spesifikke medikamentkandidat.
