| Ketersediaan: | |
|---|---|
| Kuantitas: | |











Portofolio model yang luas – Model alergen (OVA, HDM, Fel d 1), kombinasi adjuvan (LPS, c‑di‑GMP), dan TSLP (MC903) yang mencakup endotipe asma eosinofilik, neutrofilik, dan campuran granulositik.
Tersedia berbagai strain – tikus transgenik C57BL/6, BALB/c, HIS yang dimanusiakan, dan IL4/IL4R.
Titik akhir yang komprehensif – Berat badan, AHR (Penh, resistensi), jumlah sel BALF (eosinofil, neutrofil, makrofag), IgE total serum dan IgE spesifik alergen, profil sitokin (IL‑4, IL‑5, IL‑13, IL‑17), histopatologi paru (HE, Masson, PAS), hematologi.
Nilai translasi – Ideal untuk menguji biologis (anti‑IL‑4Rα, anti‑IL‑5, anti‑IL‑13, anti‑TSLP, anti‑IL‑33), inhibitor JAK, kortikosteroid, dan bronkodilator.
Paket data siap pakai IND – Studi dapat dilakukan sesuai dengan prinsip GLP.
Model Asma yang Diinduksi OVA pada Tikus C57BL/6
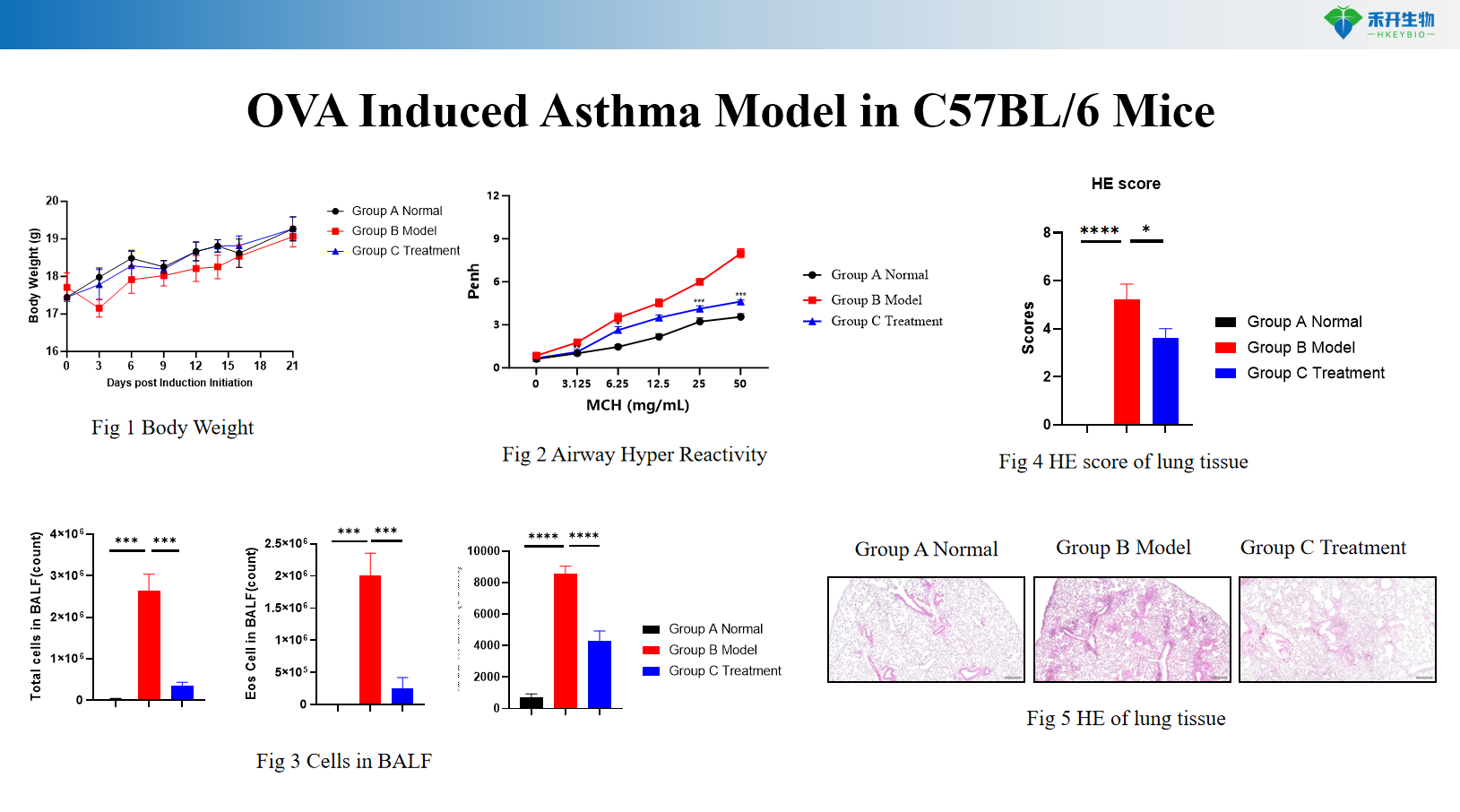
Model Asma yang Diinduksi OVA pada Tikus BALB/c
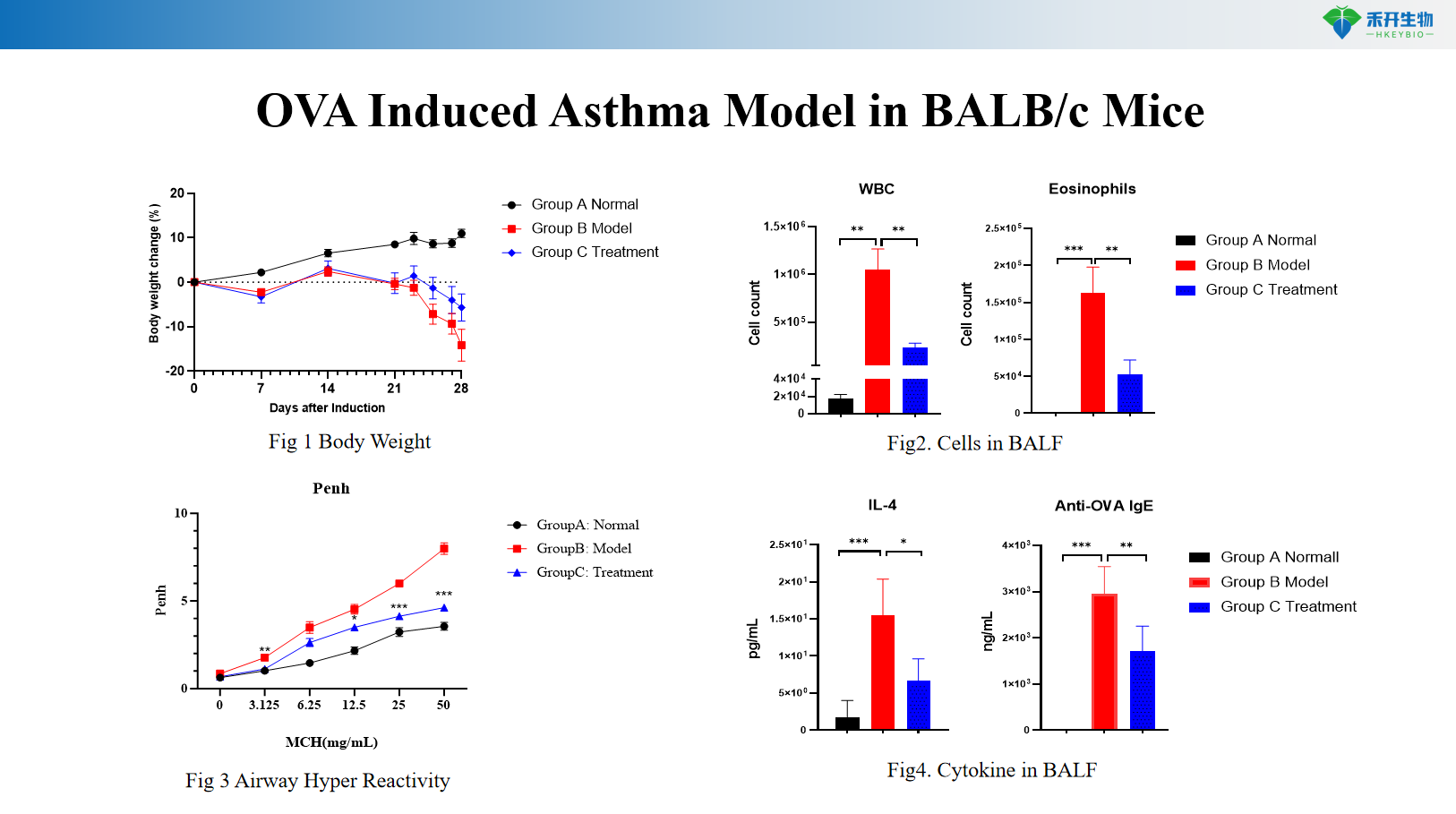
Model Asma yang Diinduksi OVA pada Tikus HIS
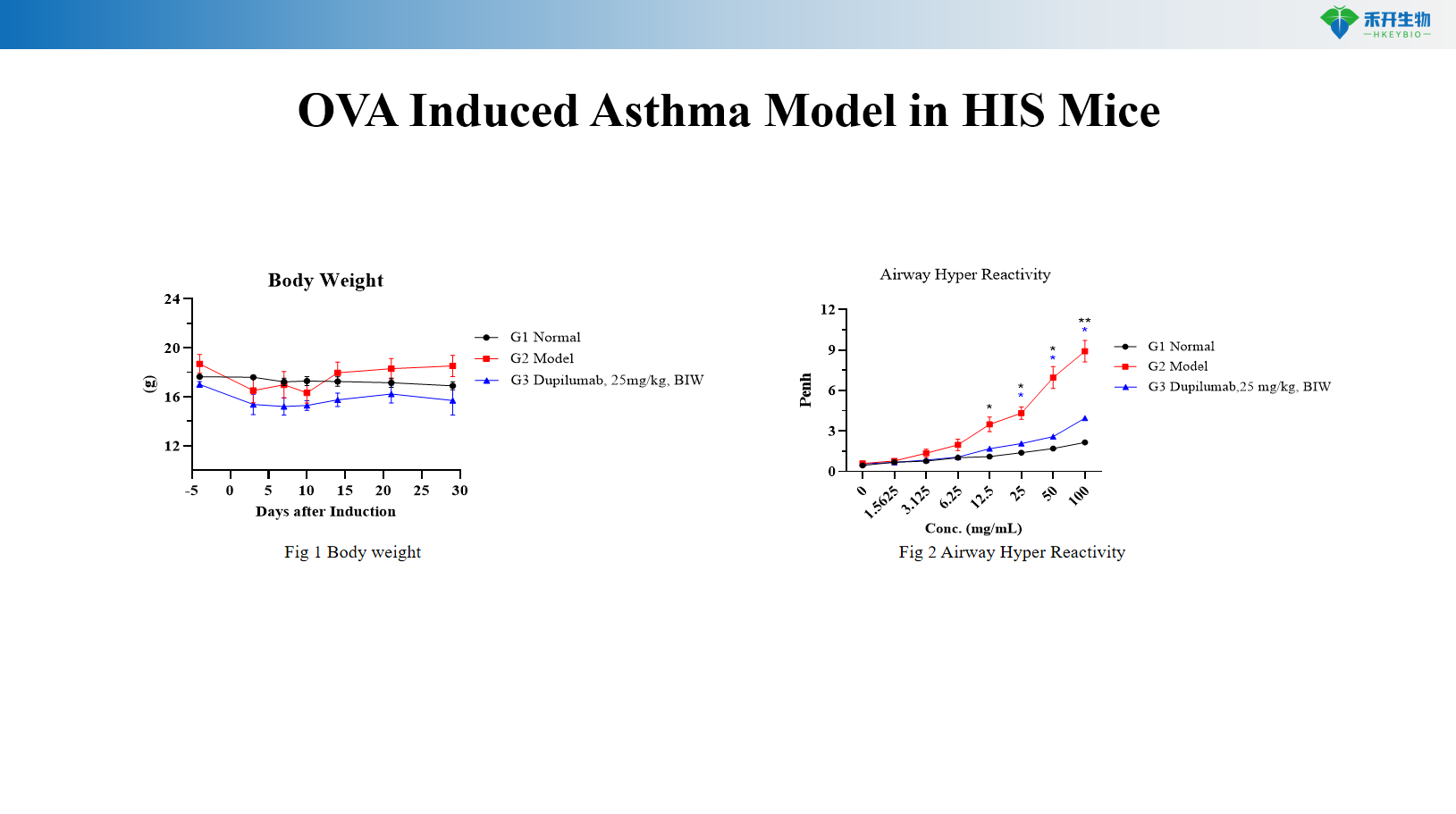
Model Asma yang Diinduksi OVA+MC903 pada Tikus C57BL/6
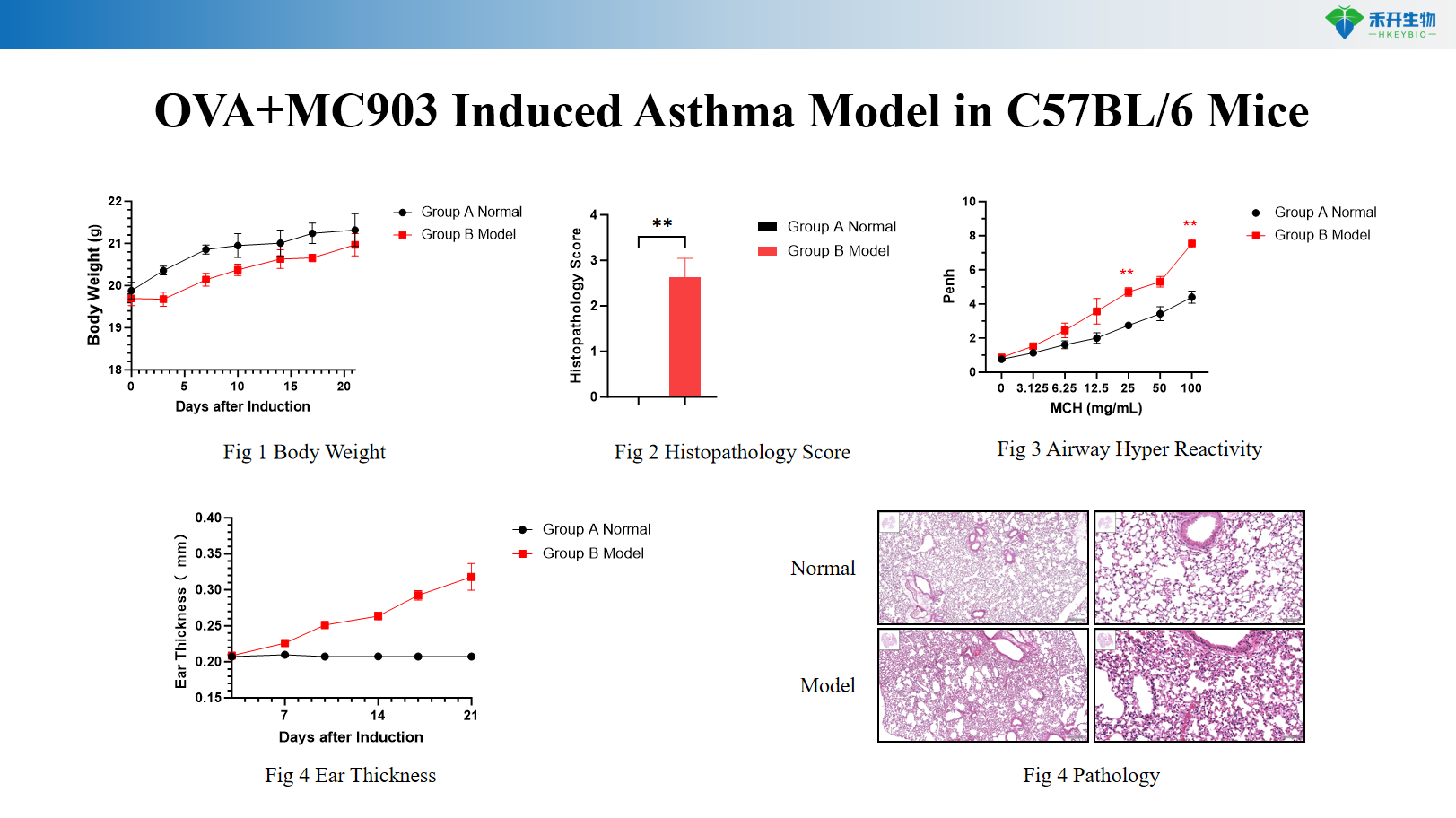
Model Asma Neutrofilik yang Diinduksi OVA+LPS pada Tikus C57BL/6
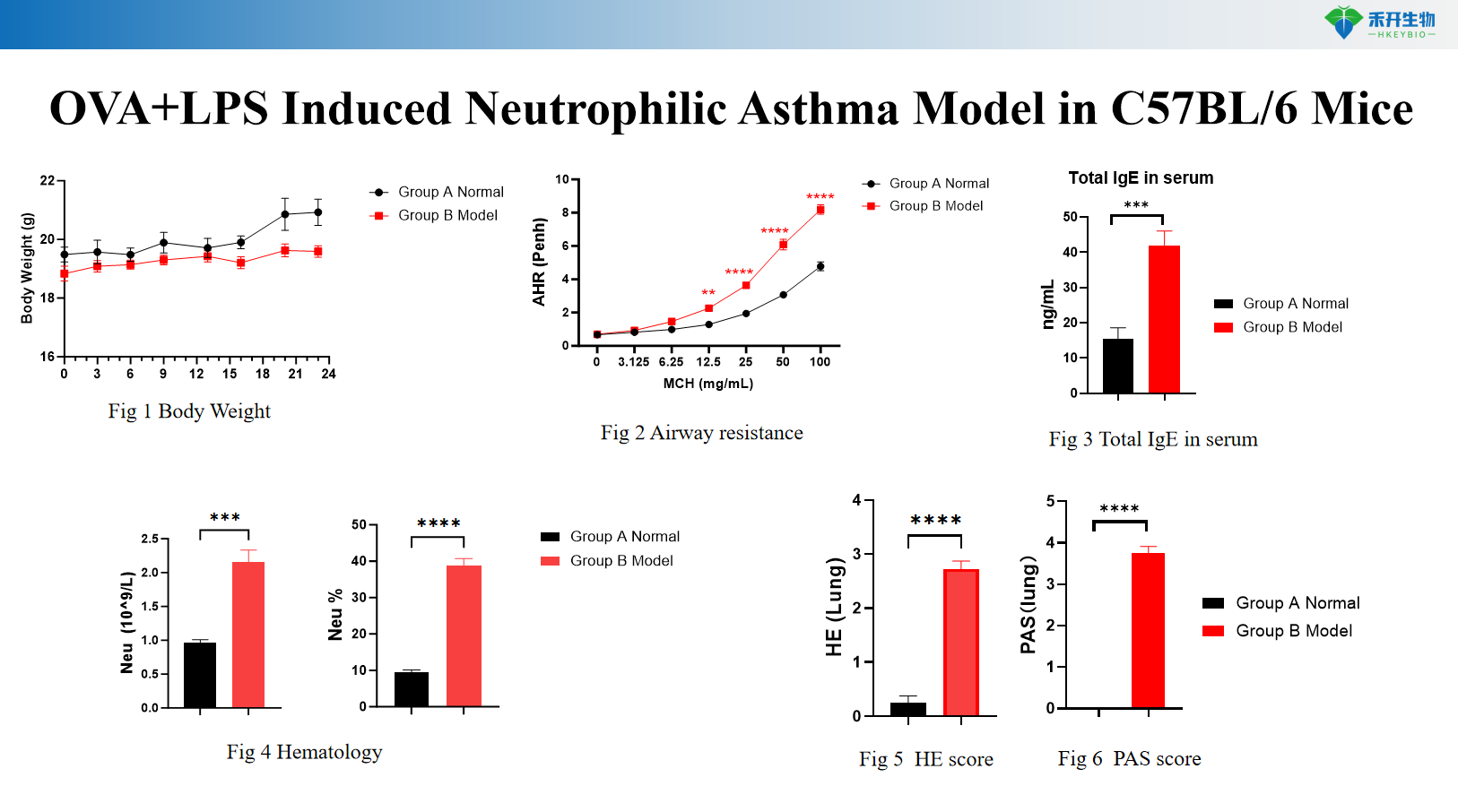
Model Asma yang Diinduksi HDM pada Tikus C57BL/6
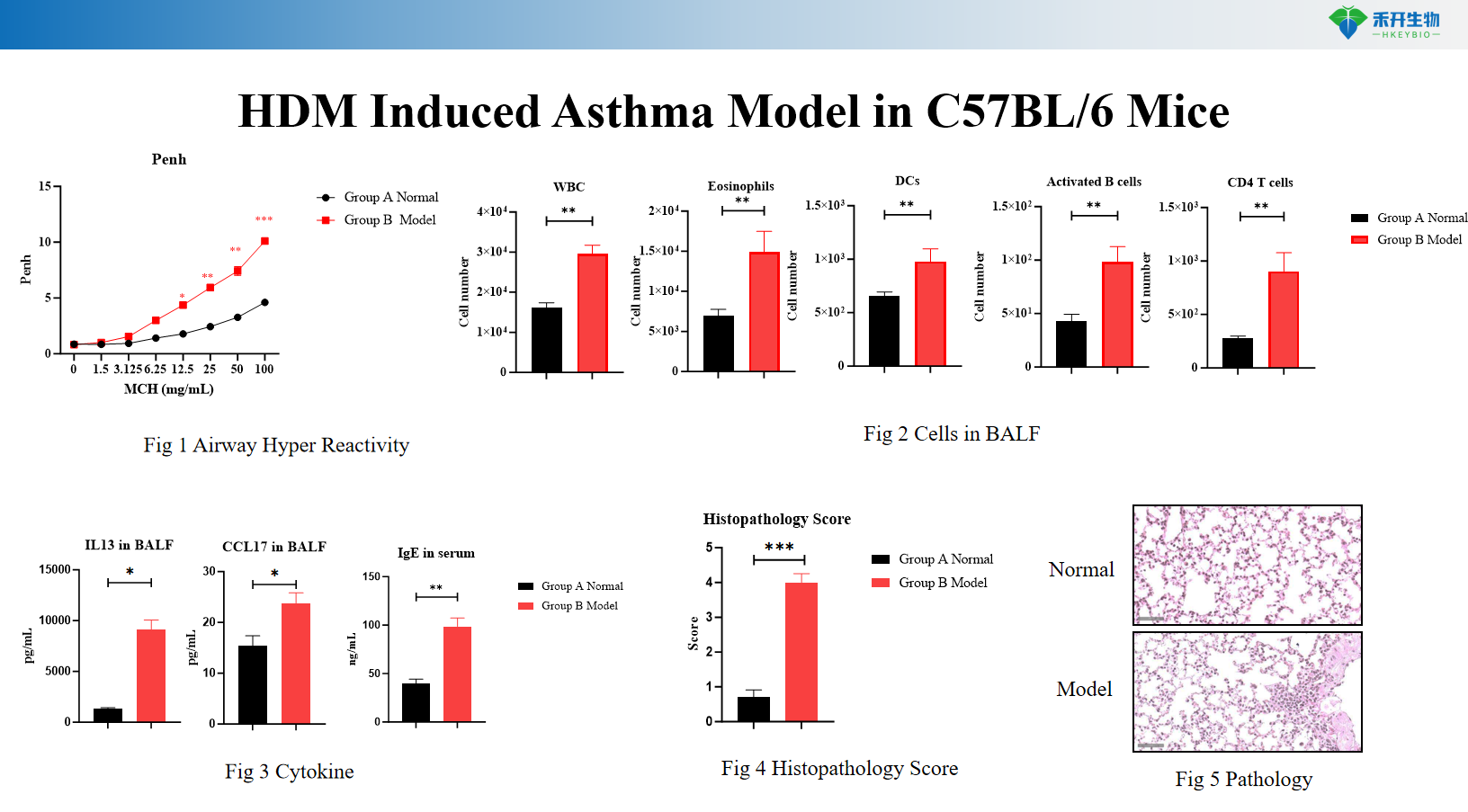
Model Asma yang Diinduksi HDM pada Tikus IL4/IL4R
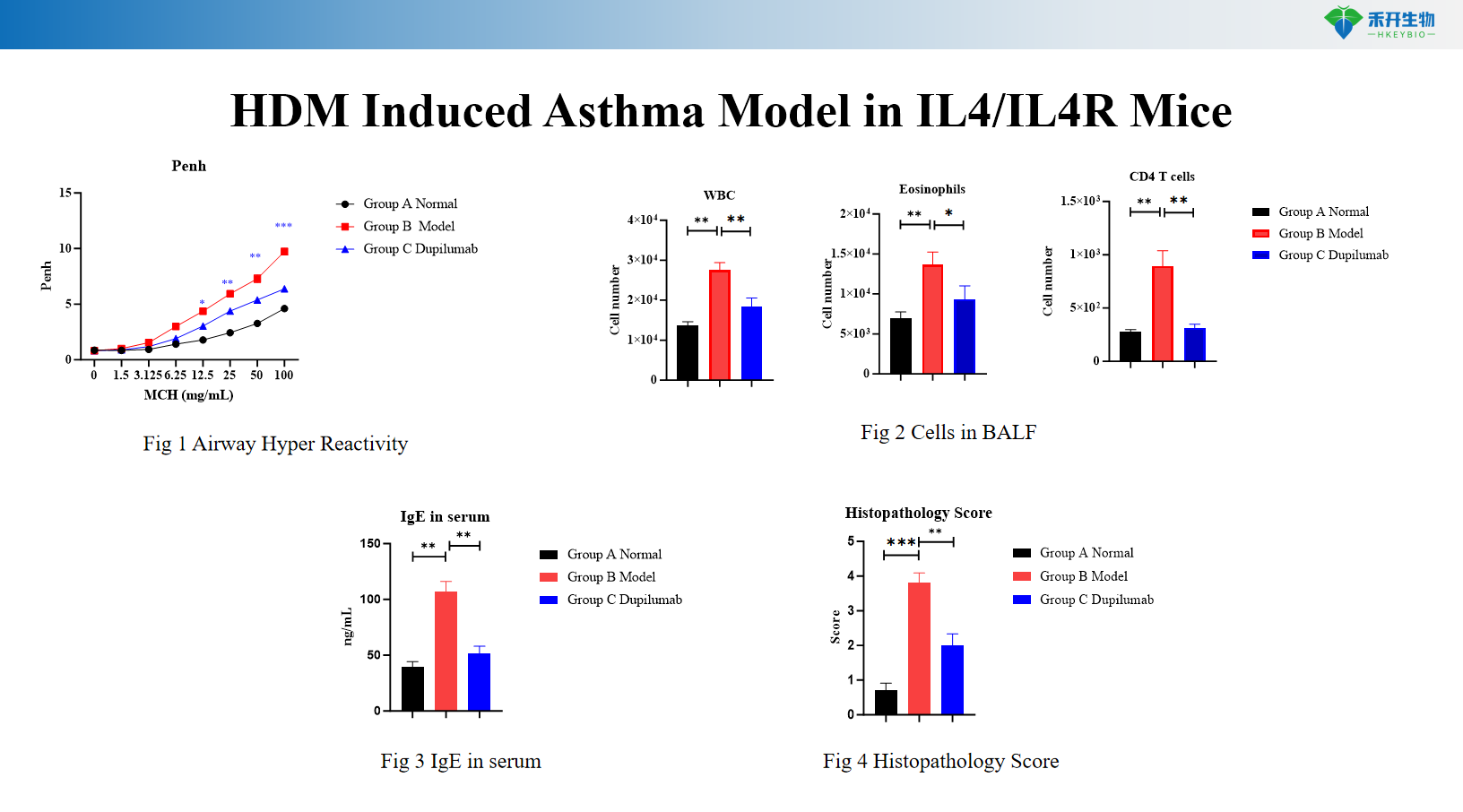
Model Asma yang Diinduksi HDM+LPS pada Tikus C57BL/6
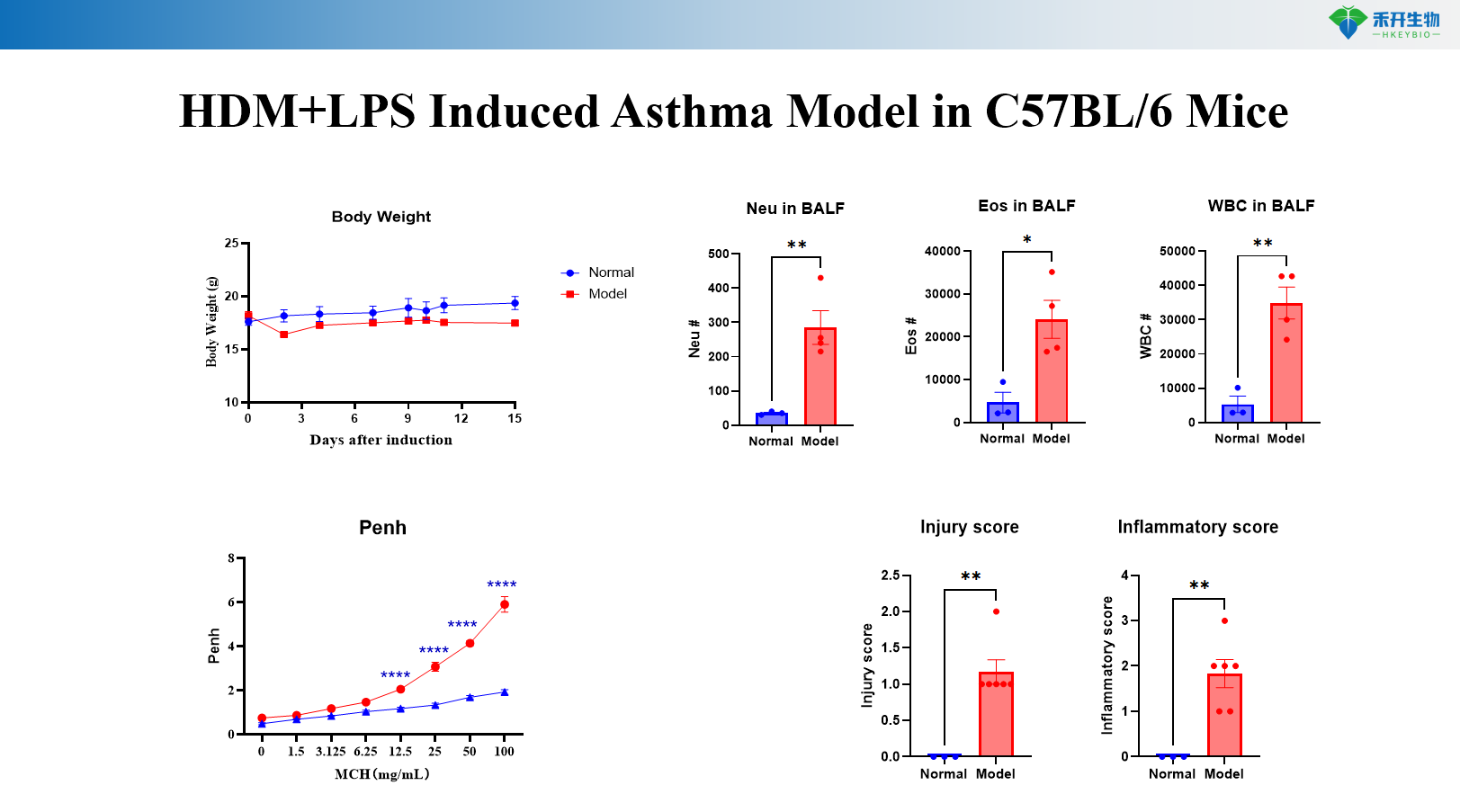
Model Asma yang Diinduksi HDM+MC903 pada Tikus C57BL/6

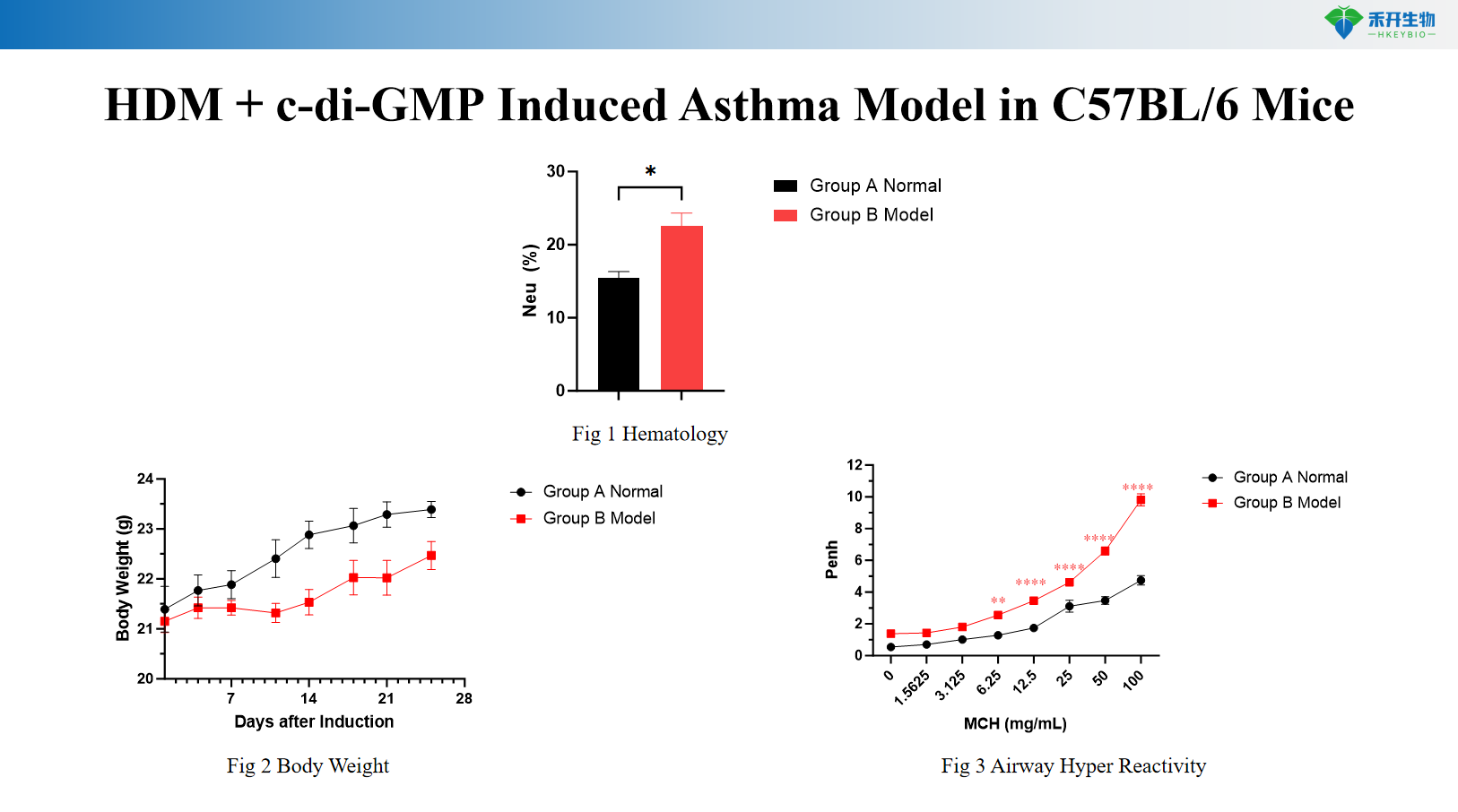
Model Asma yang Diinduksi HDM + c-di-GMP pada Tikus C57BL/6
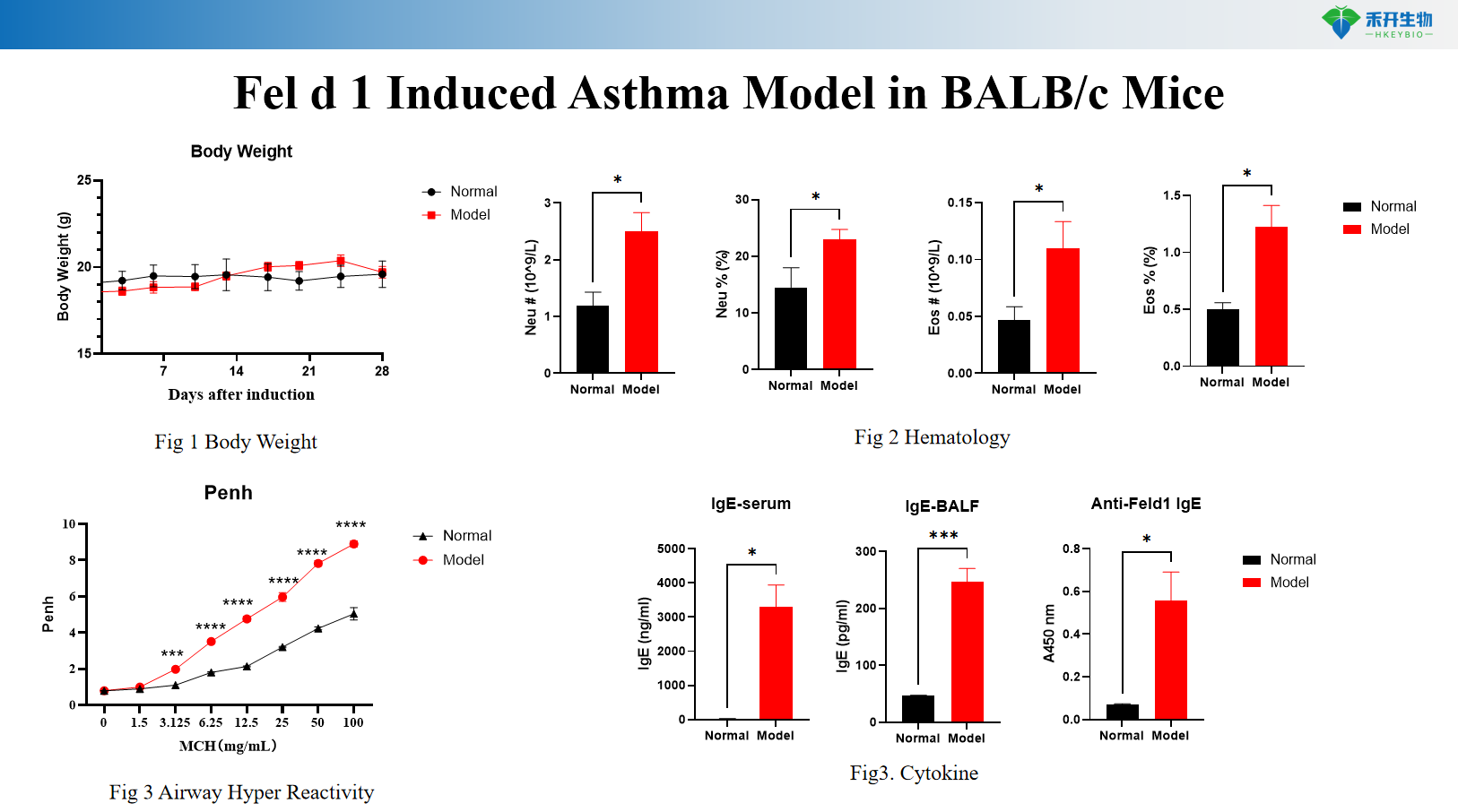
Fel d 1 Model Asma yang Diinduksi pada Tikus BALB/c
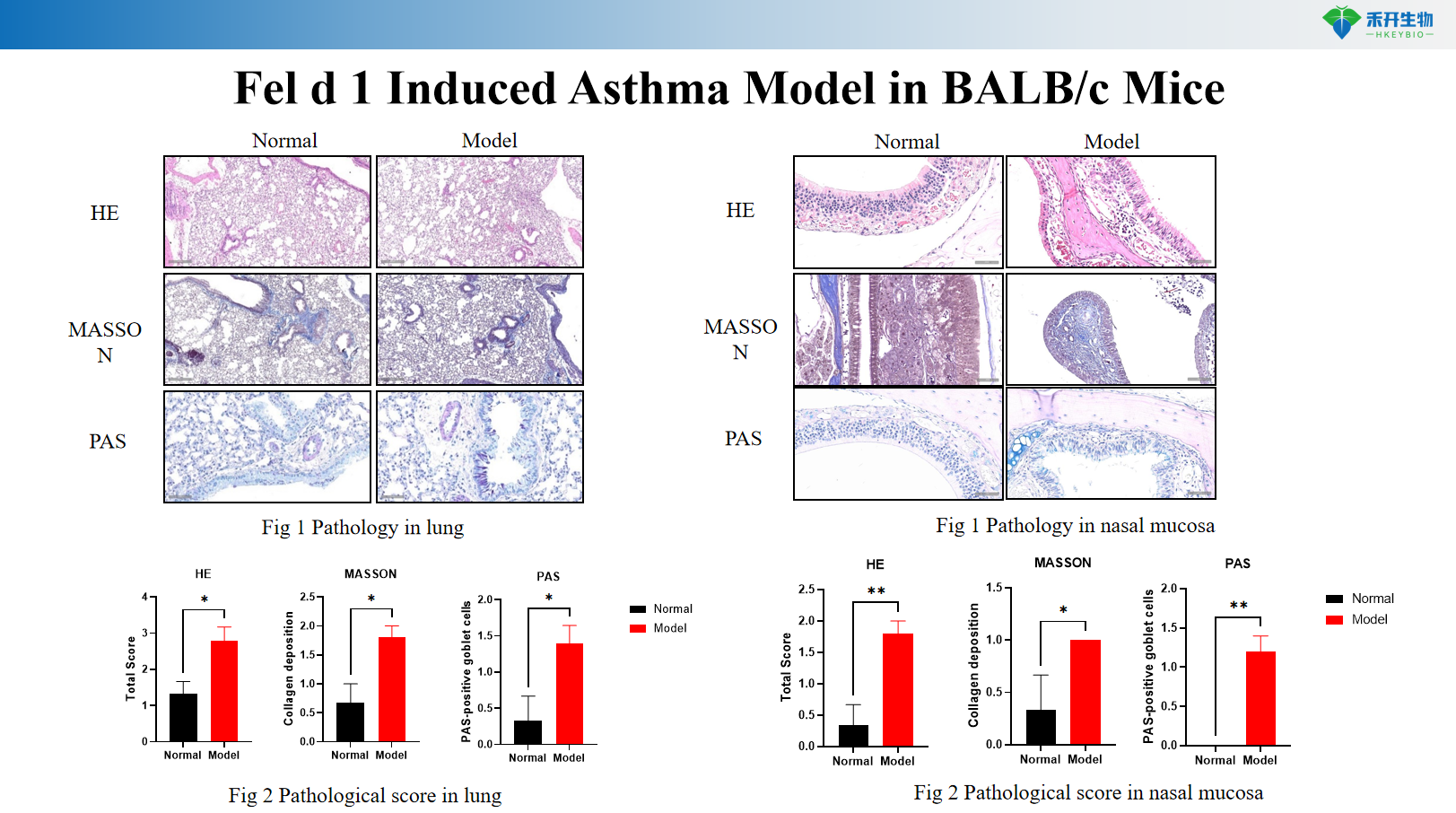
• Uji efikasi obat biologis (anti-IL-4Rα, anti-IL-5, anti-IL-13, anti-TSLP, anti-IL-33)
• Evaluasi inhibitor molekul kecil (inhibitor JAK, inhibitor PDE4, antagonis CRTH2)
• Validasi target untuk jalur sitokin Th2, Th17, dan turunan epitel
• Penemuan biomarker (IgE, tanda sitokin, penanda eosinofil/neutrofil)
• Studi farmakologi dan toksikologi yang mendukung IND
Parameter |
Spesifikasi |
Spesies/Strain |
C57BL/6, BALB/c, manusiawi, transgenik IL4/IL4R |
Metode induksi |
OVA ± tawas ± MC903 ± LPS; HDM ± LPS ± MC903 ± c‑di‑GMP; Fel d 1 + tawas |
Durasi studi |
3–8 minggu (fase sensitisasi + tantangan) |
Titik akhir yang penting |
Berat badan, AHR (invasif/non-invasif), sitologi BALF (eosinofil, neutrofil, makrofag), IgE total serum & IgE spesifik alergen, kadar sitokin (IL‑4, IL‑5, IL‑13, IL‑17, IFN‑γ), histopatologi paru (HE, Masson, PAS) dengan skoring, hematologi (opsional) |
| Kontrol positif | Antibodi deksametason atau anti‑IL‑4Rα tersedia sebagai senyawa referensi |
Paket data |
Data mentah, laporan analisis, jumlah sel BALF, hasil ELISA, slide histologi, data fungsi paru-paru, bioinformatika (opsional) |
T: Bagaimana cara memilih model AD yang tepat untuk kandidat obat saya?
J: Untuk asma eosinofilik (Th2‑tinggi), direkomendasikan model OVA atau HDM dalam BALB/c atau C57BL/6. Untuk asma granulositik neutrofilik atau campuran, model OVA+LPS atau HDM+c‑di‑GMP di C57BL/6 sesuai. Tikus yang dimanusiakan HIS ideal untuk menguji biologi spesifik manusia. Tikus transgenik IL4/IL4R cocok untuk studi jalur Th2. Tim ilmiah kami dapat memandu pemilihan model berdasarkan target spesifik Anda.
T: Apa perbedaan antara model yang diinduksi OVA dan HDM?
J: OVA adalah model alergen yang memerlukan bahan pembantu untuk sensitisasi, menghasilkan respons Th2 yang kuat. HDM adalah alergen manusia yang relevan secara klinis yang mengandung protease yang mengaktifkan imunitas bawaan dan adaptif, lebih mirip dengan patogenesis asma alergi manusia.
T: Apakah model ini dapat digunakan untuk studi yang mendukung IND?
J: Ya. Studi dapat dilakukan sesuai dengan prinsip GLP untuk pengajuan regulasi (FDA, EMA).
T: Apakah Anda menawarkan protokol penelitian yang disesuaikan (misalnya, jadwal sensitisasi/tantangan yang berbeda, terapi kombinasi)?
J: Tentu saja. Tim ilmiah kami menyesuaikan protokol induksi, jadwal pengobatan, dan analisis titik akhir untuk kandidat obat spesifik Anda.
T: Apa jadwal umum untuk studi kemanjuran percontohan?
J: Sebagian besar model asma diselesaikan dalam waktu 4–6 minggu, termasuk sensitisasi, tantangan, pengobatan, dan analisis titik akhir.
