| Tilgængelighed: | |
|---|---|
| Antal: | |











Bred modelportefølje – Allergen (OVA, HDM, Fel d 1), adjuvans-kombinerede (LPS, c-di-GMP) og TSLP-drevne (MC903) modeller, der dækker eosinofile, neutrofile og blandede granulocytiske astmaendotyper.
Flere stammer - C57BL/6, BALB/c, HIS humaniserede og IL4/IL4R transgene mus tilgængelige.
Omfattende endepunkter – Kropsvægt, AHR (Penh, resistens), BALF-celletal (eosinofiler, neutrofiler, makrofager), totalt serum-IgE og allergen-specifikt IgE, cytokinprofilering (IL-4, IL-5, IL-13, IL-17), hæmpatologi, (PHE, Mahistoatology, AS).
Translationel værdi – Ideel til test af biologiske lægemidler (anti-IL-4Ra, anti-IL-5, anti-IL-13, anti-TSLP, anti-IL-33), JAK-hæmmere, kortikosteroider og bronkodilatatorer.
IND-klare datapakker – Undersøgelser kan udføres i overensstemmelse med GLP-principperne.
OVA-induceret astmamodel i C57BL/6-mus
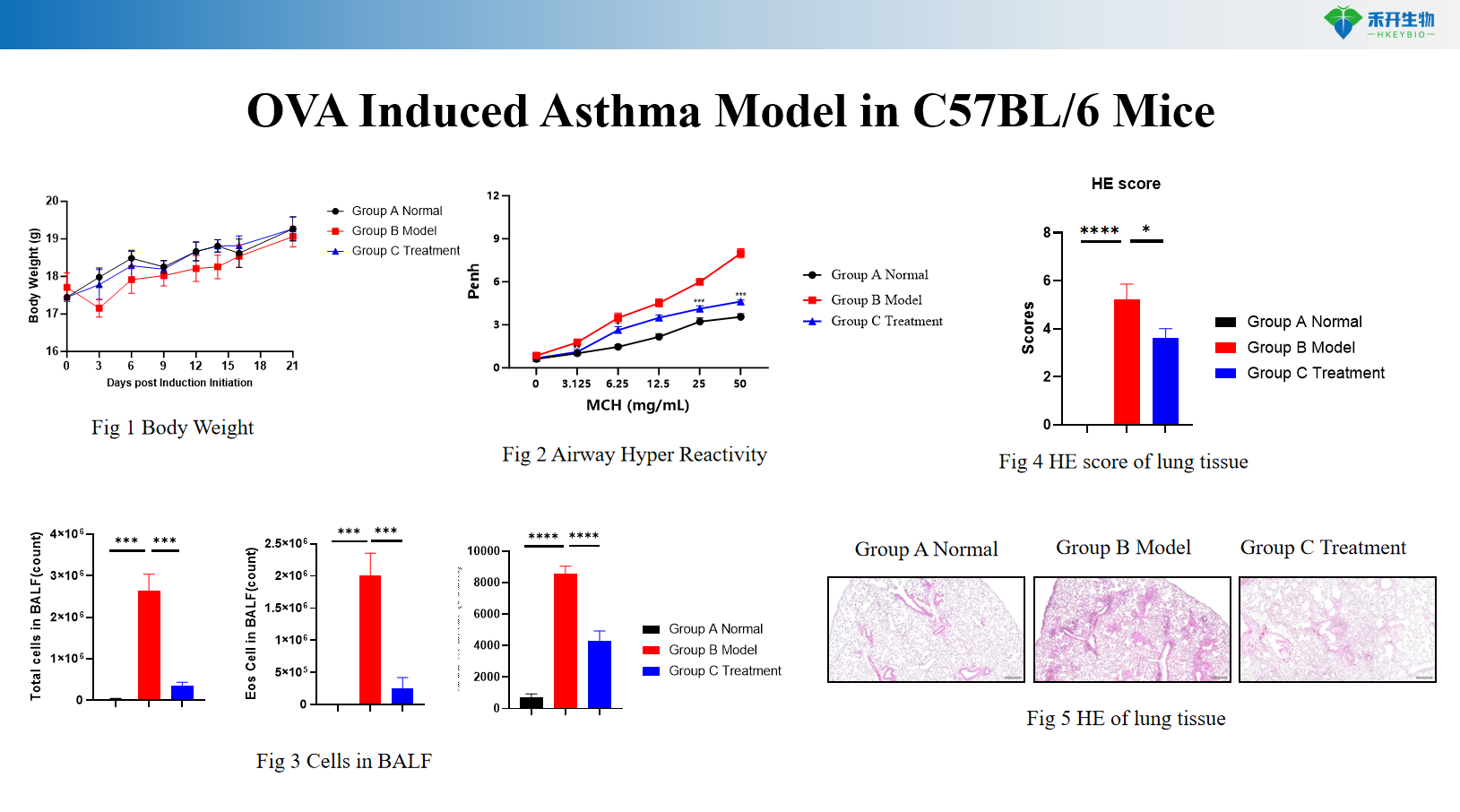
OVA-induceret astmamodel i BALB/c-mus
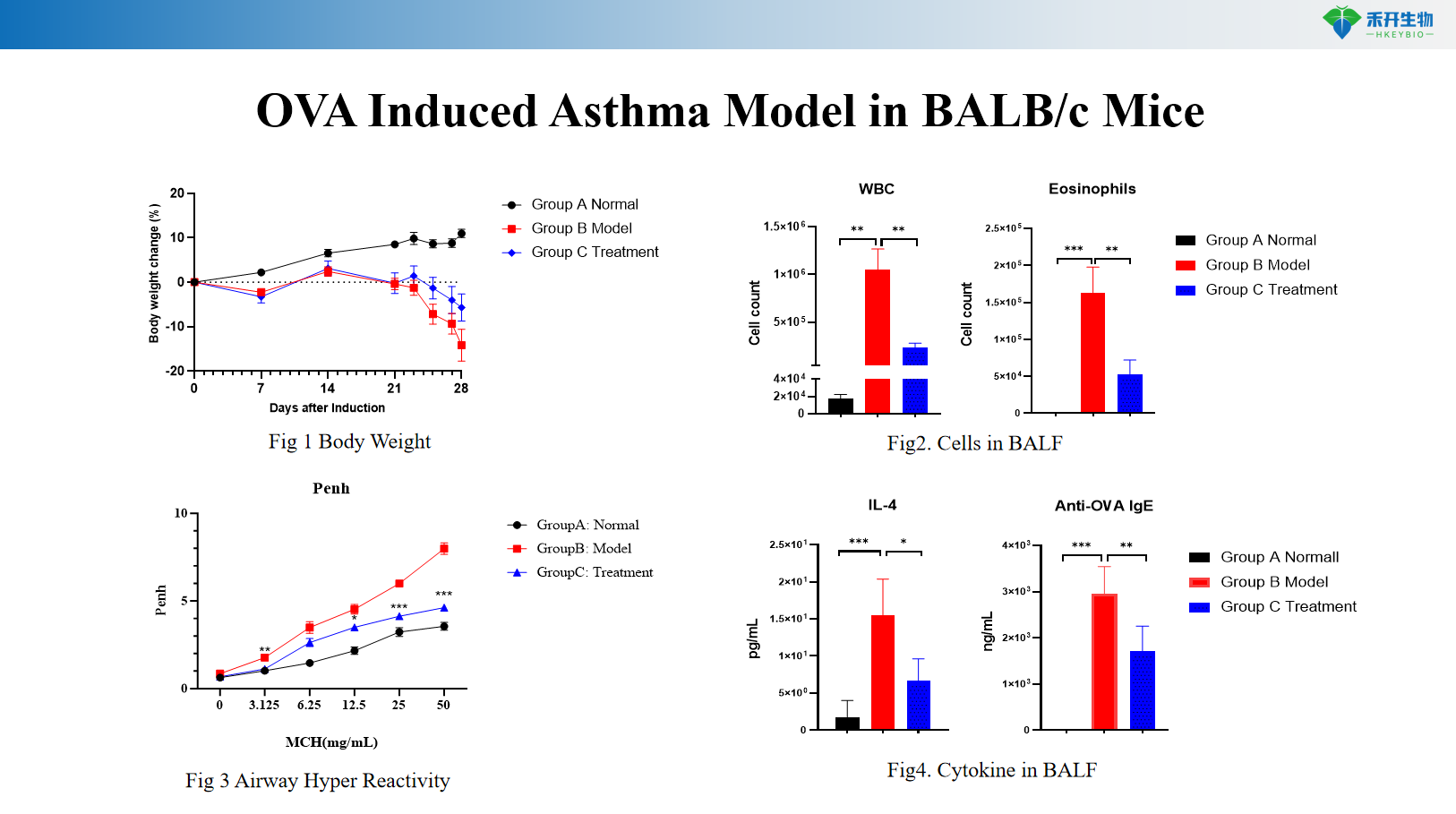
OVA-induceret astmamodel i HIS mus
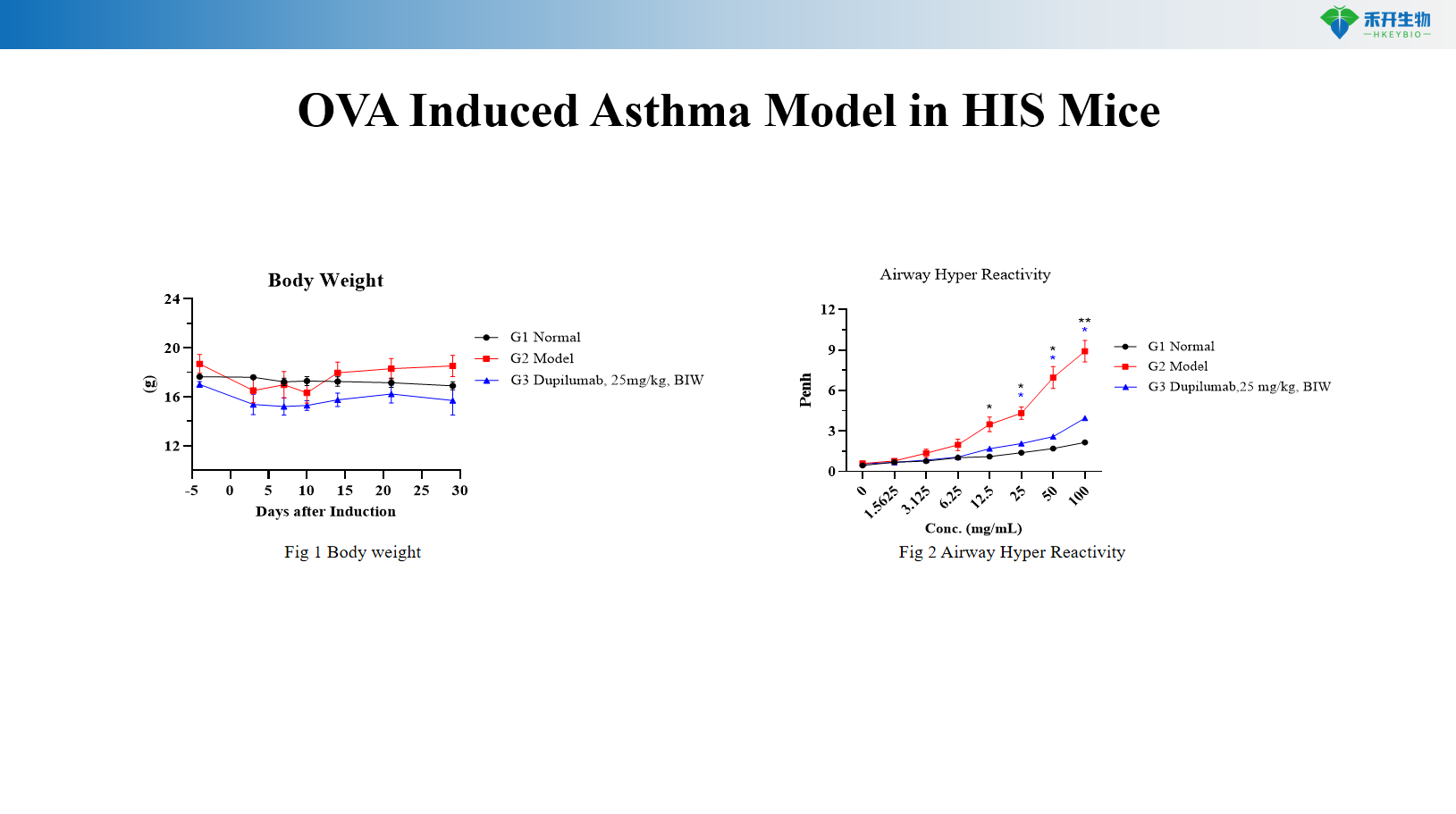
OVA+MC903-induceret astmamodel i C57BL/6-mus
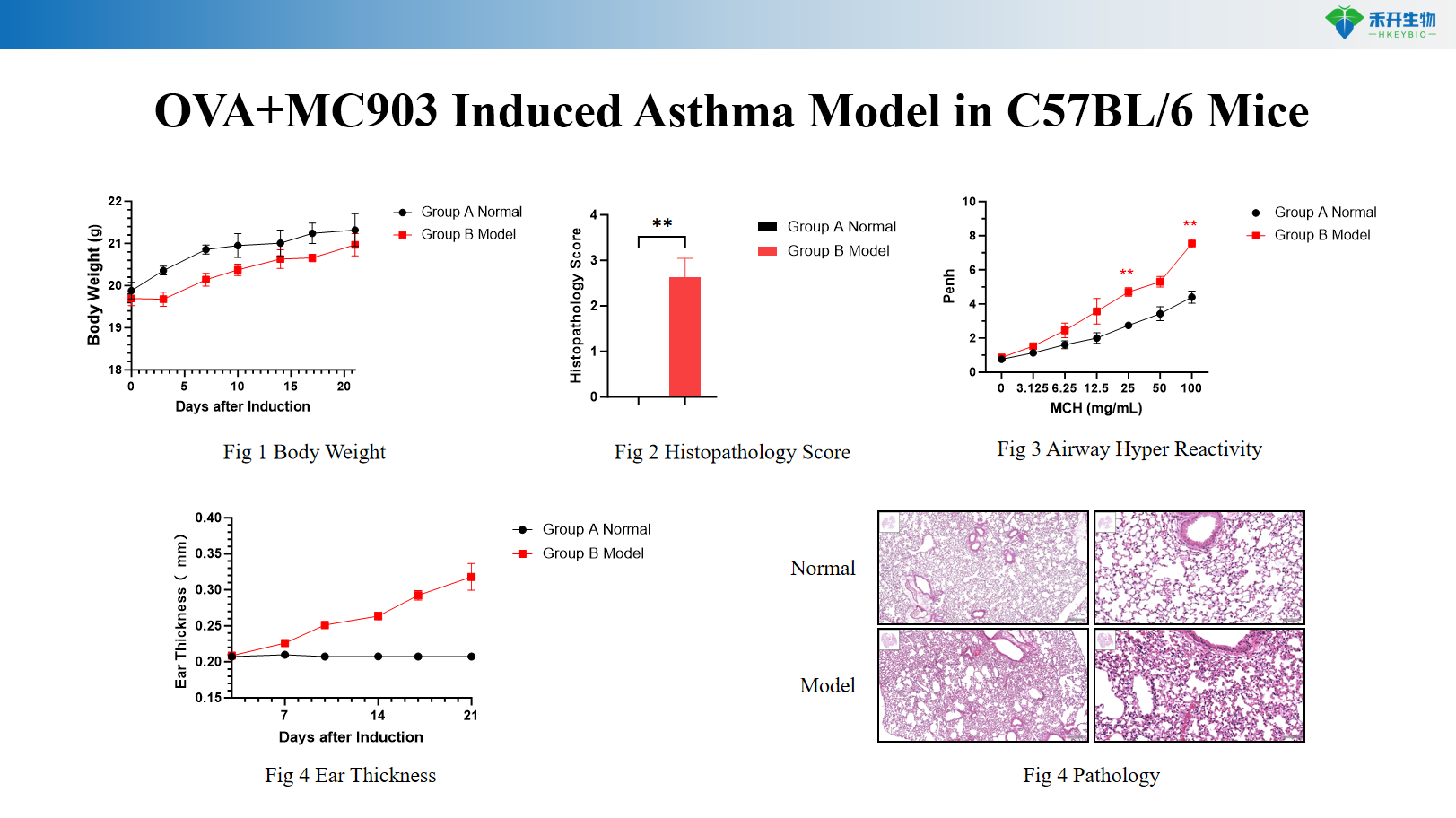
OVA+LPS-induceret neutrofil astmamodel i C57BL/6-mus
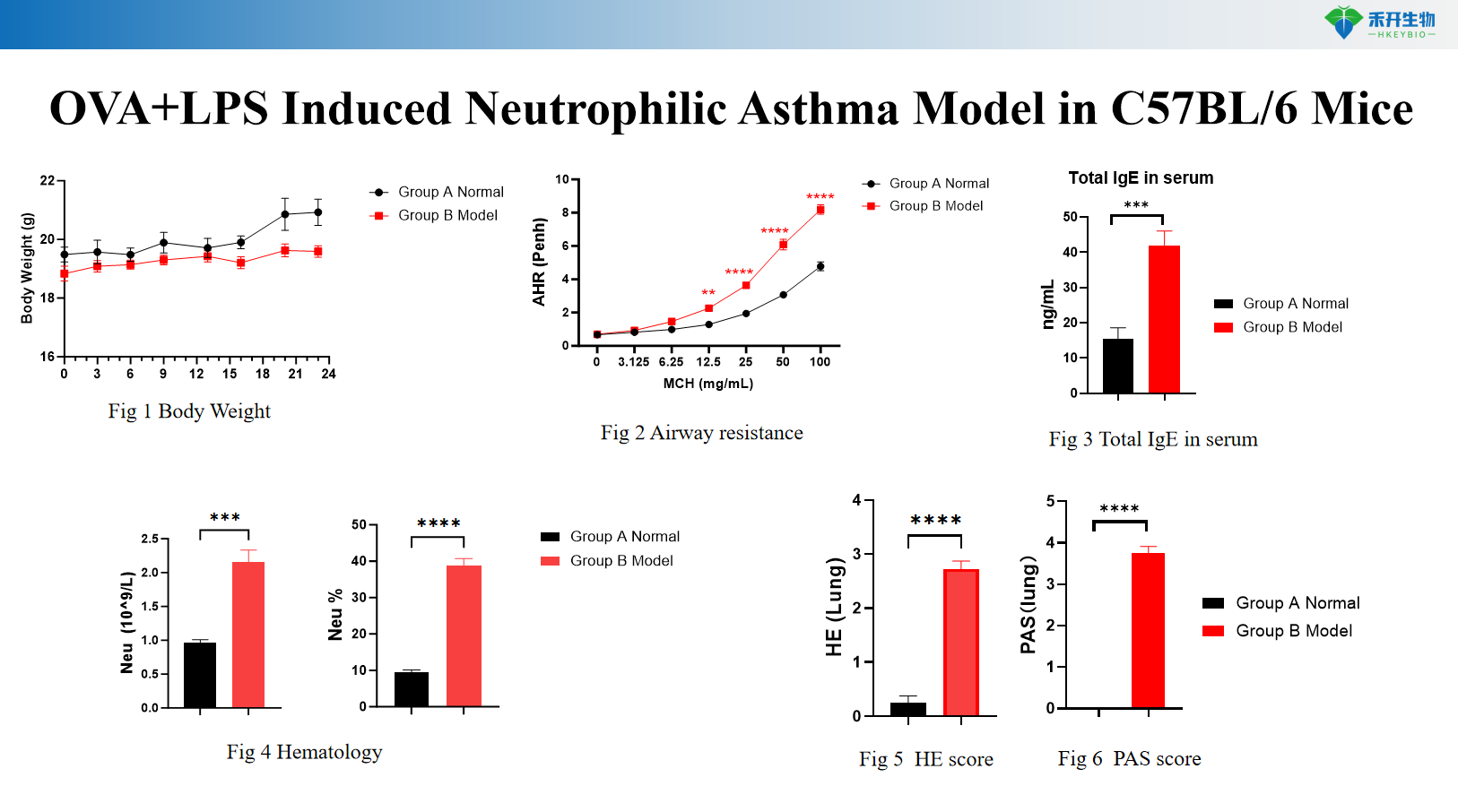
HDM-induceret astmamodel i C57BL/6-mus
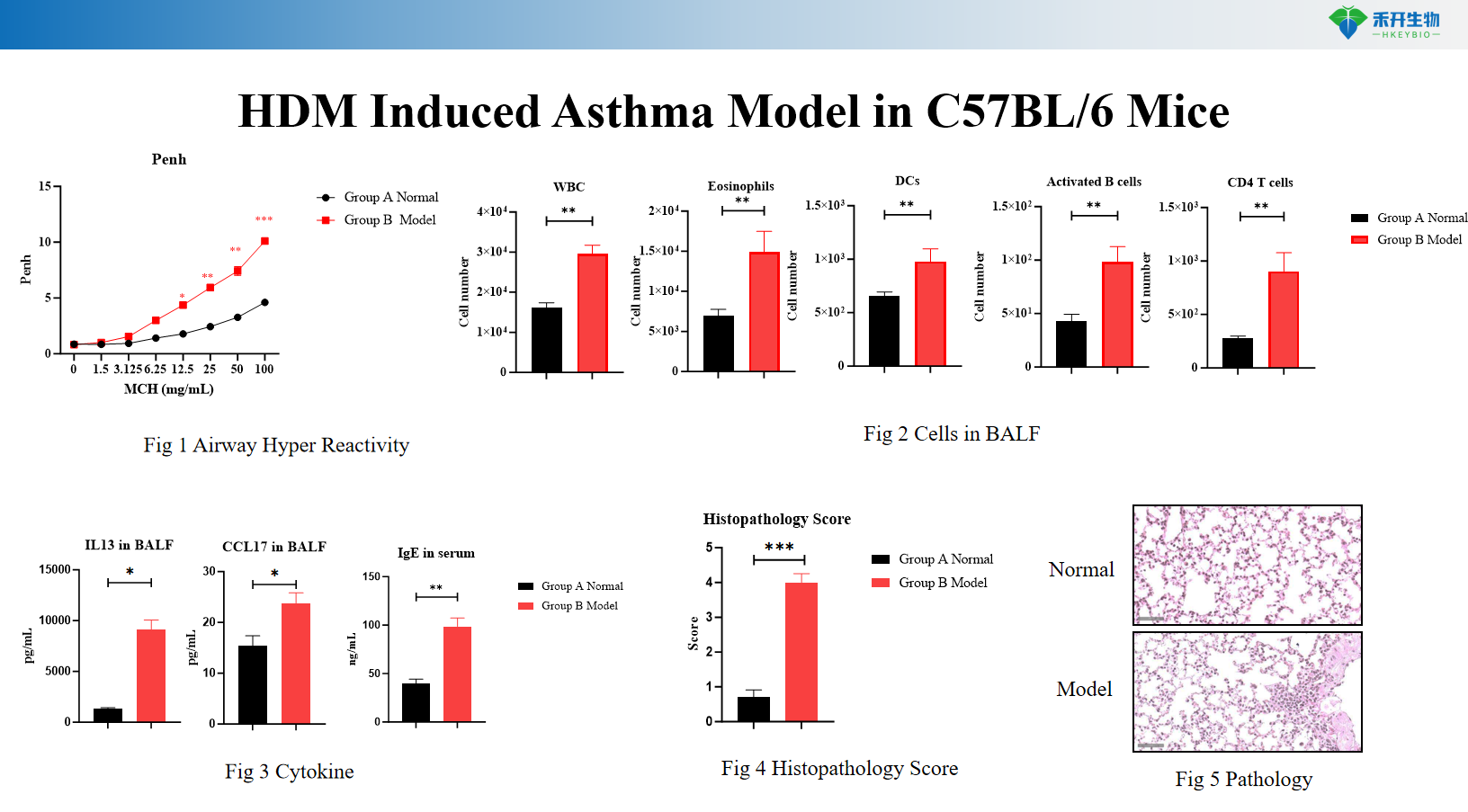
HDM-induceret astmamodel i IL4/IL4R-mus
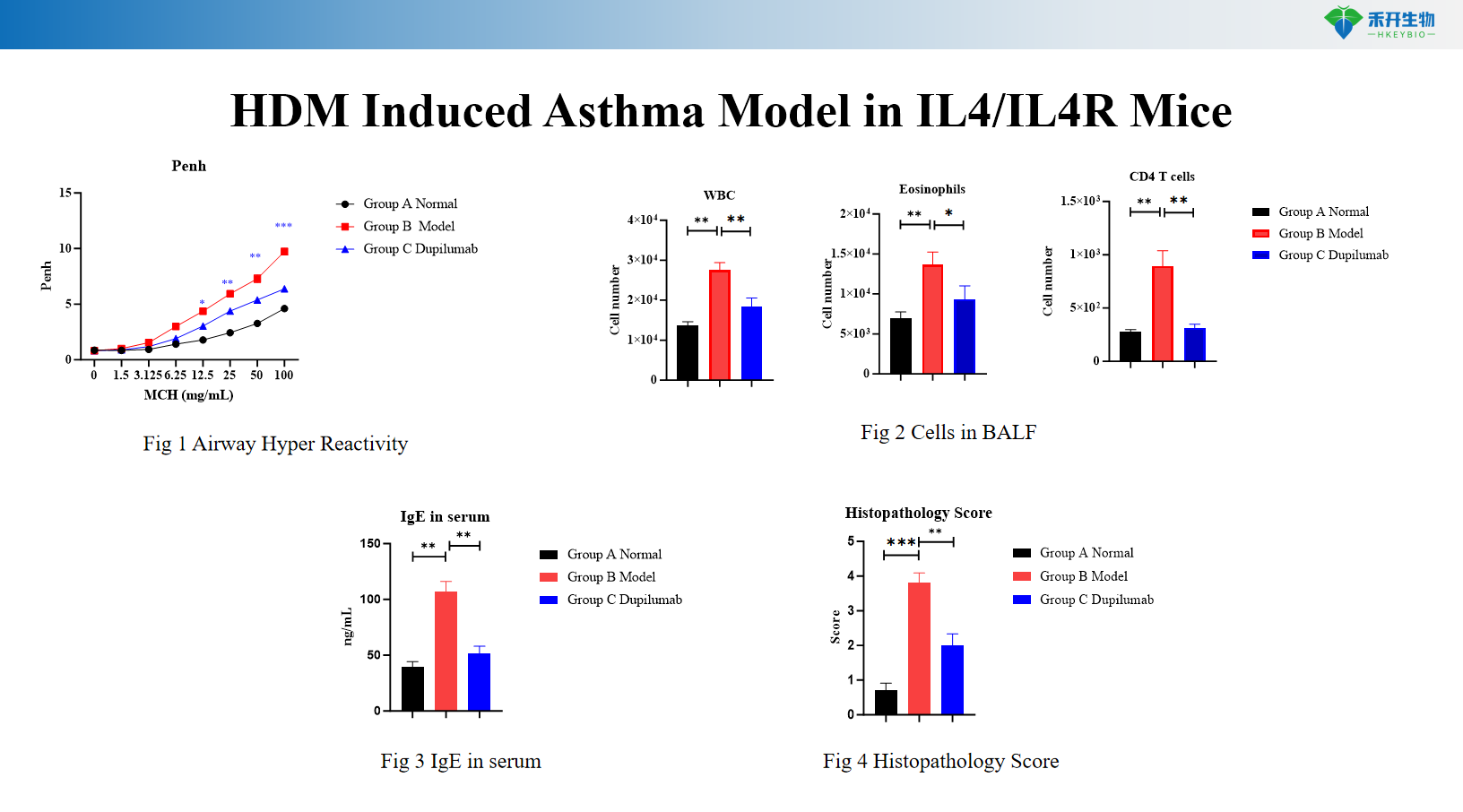
HDM+LPS-induceret astmamodel i C57BL/6-mus
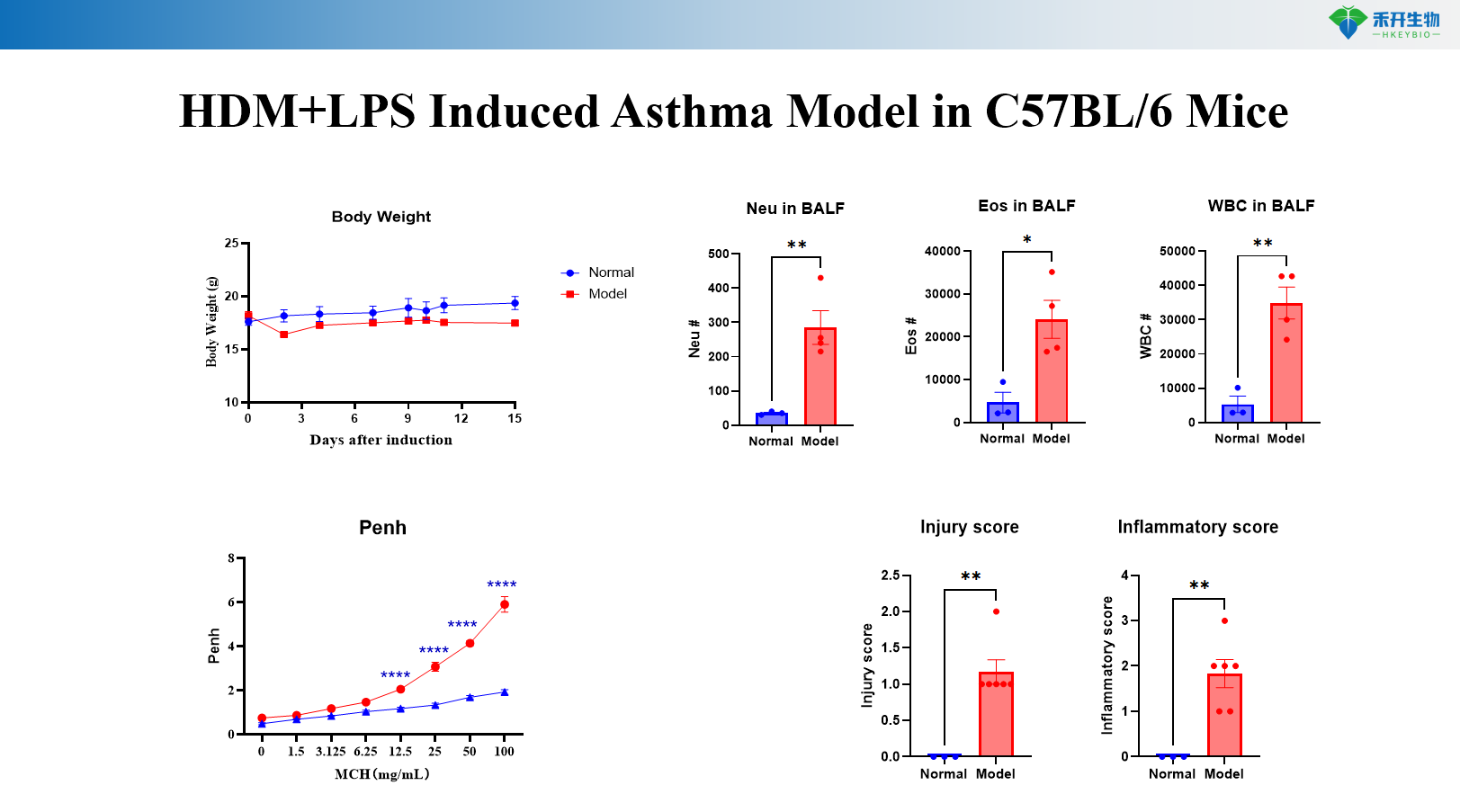
HDM+MC903-induceret astmamodel i C57BL/6-mus

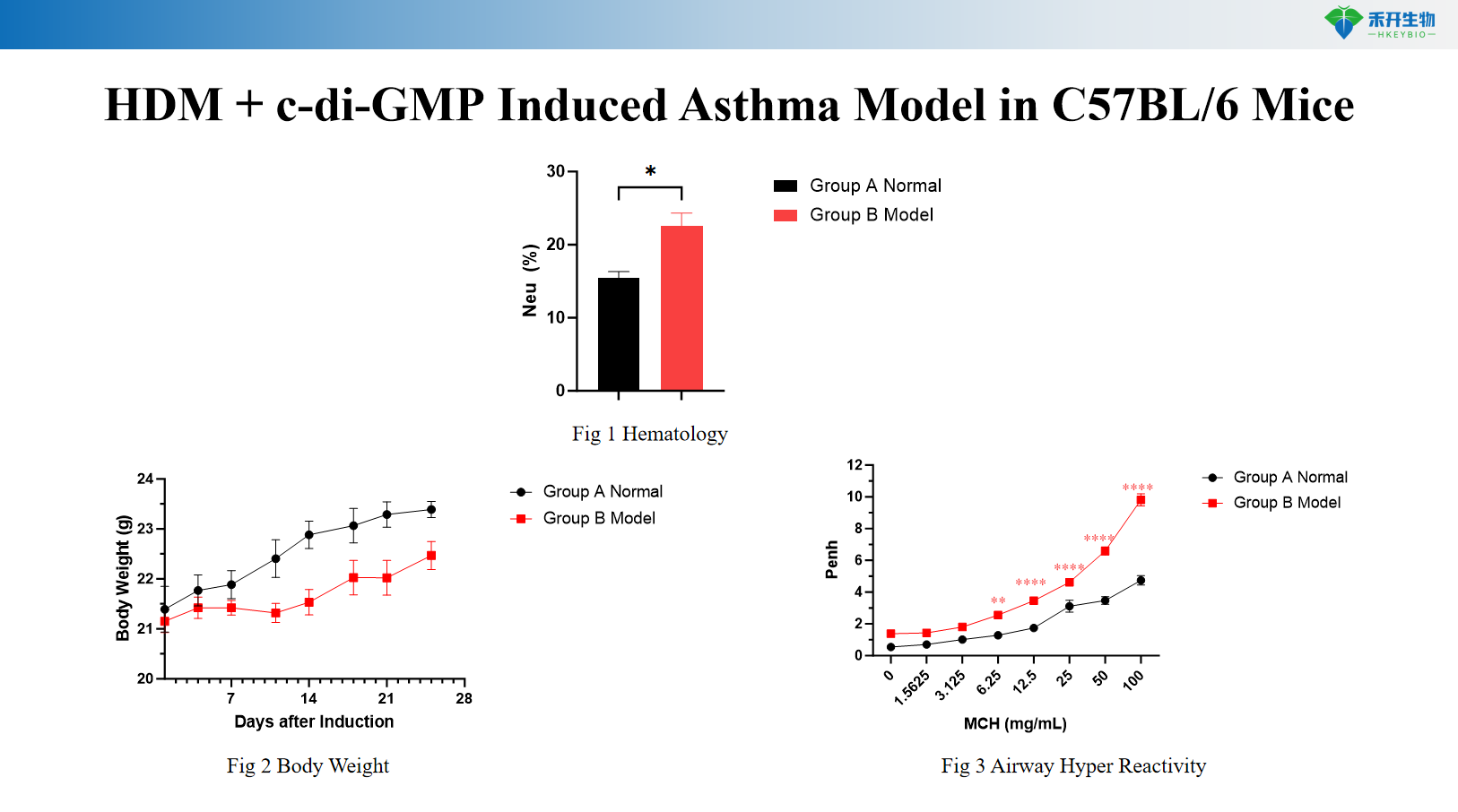
HDM + c-di-GMP-induceret astmamodel i C57BL/6-mus
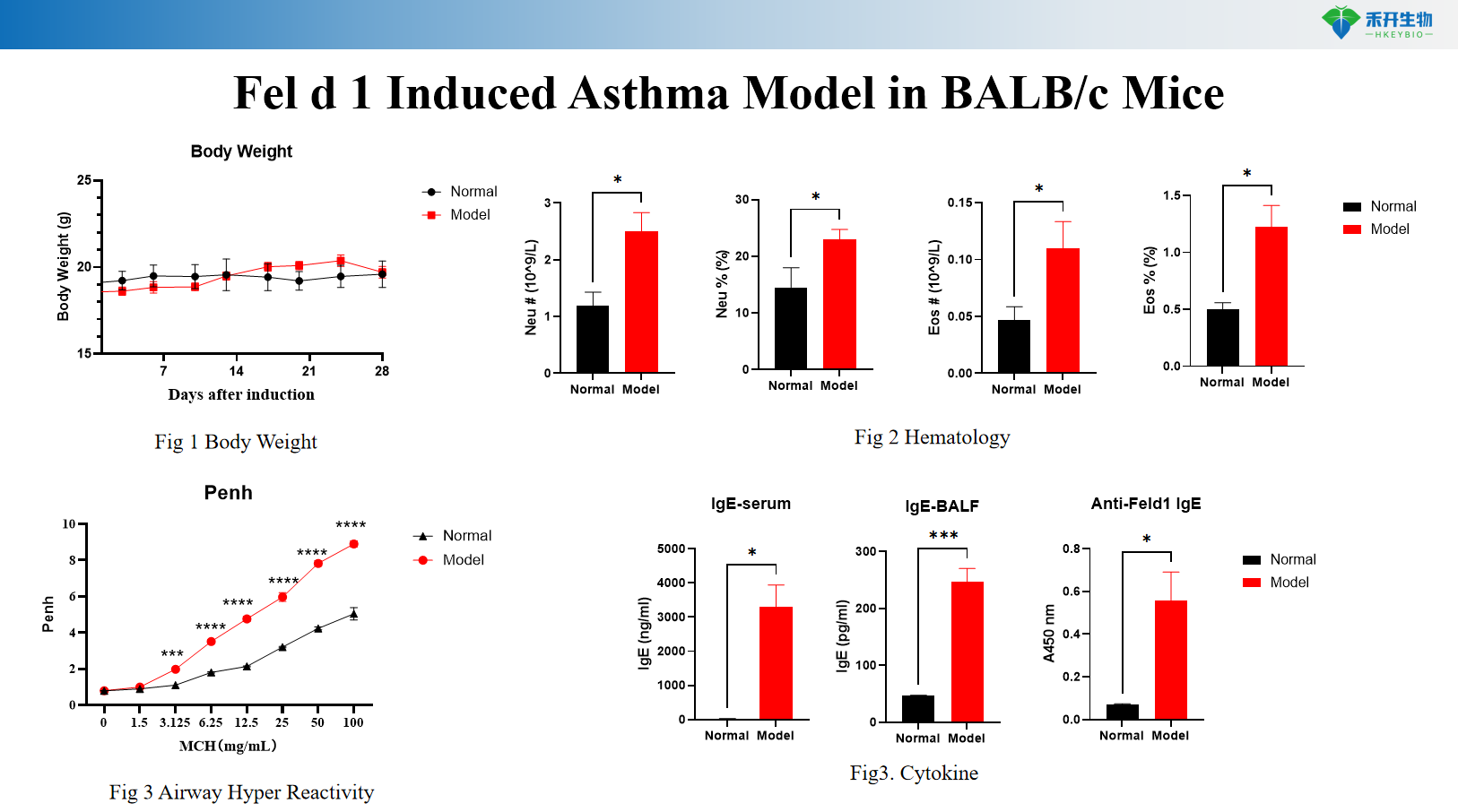
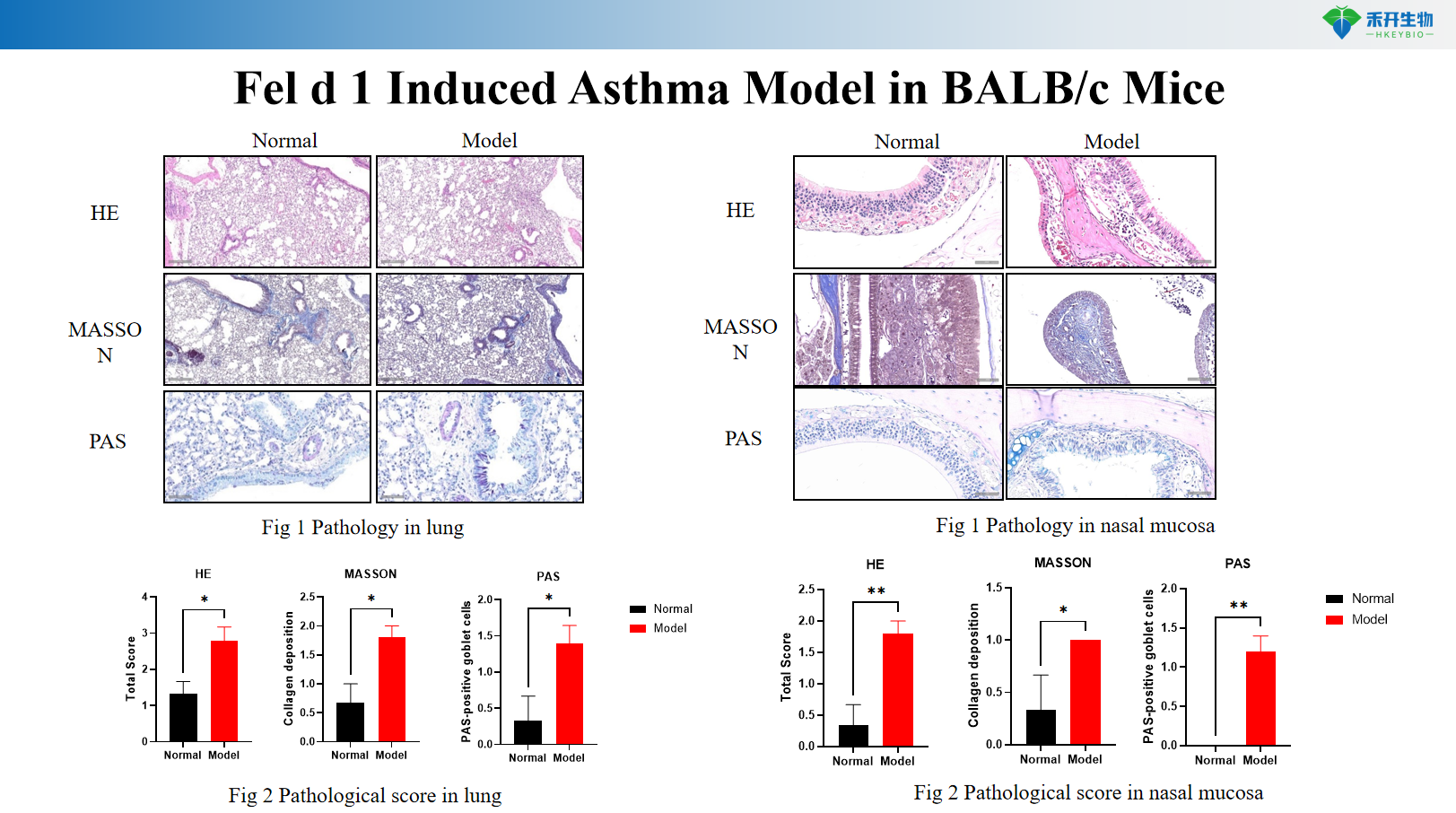
Fel d 1-induceret astmamodel i BALB/c-mus
• Effektivitetstest af biologiske lægemidler (anti-IL-4Ra, anti-IL-5, anti-IL-13, anti-TSLP, anti-IL-33)
• Evaluering af små molekyle hæmmere (JAK hæmmere, PDE4 hæmmere, CRTH2 antagonister)
• Målvalidering for Th2, Th17 og epitelafledte cytokinveje
• Biomarkøropdagelse (IgE, cytokinsignaturer, eosinofile/neutrofile markører)
• IND-aktiverende farmakologi og toksikologiske undersøgelser
Parameter |
Specifikation |
Art/Stamme |
C57BL/6, BALB/c, HIS humaniseret, IL4/IL4R transgen |
Induktionsmetode |
OVA ± alun ± MC903 ± LPS; HDM ± LPS ± MC903 ± c-di-GMP; Fel d 1 + alun |
Studievarighed |
3-8 uger (sensibilisering + udfordringsfaser) |
Nøgleendepunkter |
Kropsvægt, AHR (invasiv/ikke-invasiv), BALF-cytologi (eosinofiler, neutrofiler, makrofager), totalt serum-IgE & allergen-specifikt IgE, cytokinniveauer (IL-4, IL-5, IL-13, IL-17-histo, γNAS)-patologi, P-lunge, IFNAS- scoring, hæmatologi (valgfrit) |
| Positiv kontrol | Dexamethason eller anti-IL-4Ra-antistof tilgængelig som referenceforbindelser |
Datapakke |
Rådata, analyserapporter, BALF-celletal, ELISA-resultater, histologiske dias, lungefunktionsdata, bioinformatik (valgfrit) |
Q: Hvordan vælger jeg den rigtige AD-model til min lægemiddelkandidat?
A: Til eosinofil (Th2-høj) astma anbefales OVA- eller HDM-modeller i BALB/c eller C57BL/6. Til neutrofil eller blandet granulocytisk astma er OVA+LPS- eller HDM+c-di-GMP-modeller i C57BL/6 passende. HIS humaniserede mus er ideelle til at teste menneskespecifikke biologiske lægemidler. IL4/IL4R transgene mus er velegnede til Th2 pathway undersøgelser. Vores videnskabelige team kan guide modelvalg baseret på dit specifikke mål.
Q: Hvad er forskellen mellem OVA- og HDM-inducerede modeller?
A: OVA er et modelallergen, der kræver adjuvans til sensibilisering, hvilket producerer robuste Th2-responser. HDM er et klinisk relevant humant allergen indeholdende proteaser, der aktiverer både medfødt og adaptiv immunitet, hvilket i højere grad efterligner human allergisk astmapatogenese.
Sp: Kan disse modeller bruges til IND-aktiverende undersøgelser?
A: Ja. Undersøgelser kan udføres i overensstemmelse med GLP-principperne for regulatoriske indsendelser (FDA, EMA).
Spørgsmål: Tilbyder du tilpassede undersøgelsesprotokoller (f.eks. forskellige sensibiliserings-/udfordringsplaner, kombinationsterapier)?
A: Absolut. Vores videnskabelige team skræddersyr induktionsprotokoller, behandlingsplaner og slutpunktsanalyser til din specifikke lægemiddelkandidat.
Q: Hvad er den typiske tidslinje for et piloteffektivitetsstudie?
A: De fleste astmamodeller afsluttes inden for 4-6 uger, inklusive sensibilisering, udfordring, behandling og endepunktsanalyse.
