| Dostępność: | |
|---|---|
| Ilość: | |











Szerokie portfolio modeli – modele alergenowe (OVA, HDM, Fel d 1), skojarzone adiuwanty (LPS, c-di-GMP) i oparte na TSLP (MC903) obejmujące endotypy astmy eozynofilowej, neutrofilowej i mieszanej granulocytarnej.
Dostępnych jest wiele szczepów – myszy humanizowane C57BL/6, BALB/c, HIS i transgeniczne IL4/IL4R.
Kompleksowe punkty końcowe – masa ciała, AHR (Penh, oporność), liczba komórek BALF (eozynofile, neutrofile, makrofagi), całkowite IgE w surowicy i IgE swoiste dla alergenu, profilowanie cytokin (IL-4, IL-5, IL-13, IL-17), histopatologia płuc (HE, Masson, PAS), hematologia.
Wartość translacyjna – Idealny do testowania leków biologicznych (anty-IL-4Rα, anty-IL-5, anty-IL-13, anty-TSLP, anty-IL-33), inhibitorów JAK, kortykosteroidów i leków rozszerzających oskrzela.
Pakiety danych gotowe do IND – Badania można prowadzić zgodnie z zasadami DPL.
Model astmy indukowanej OVA u myszy C57BL/6
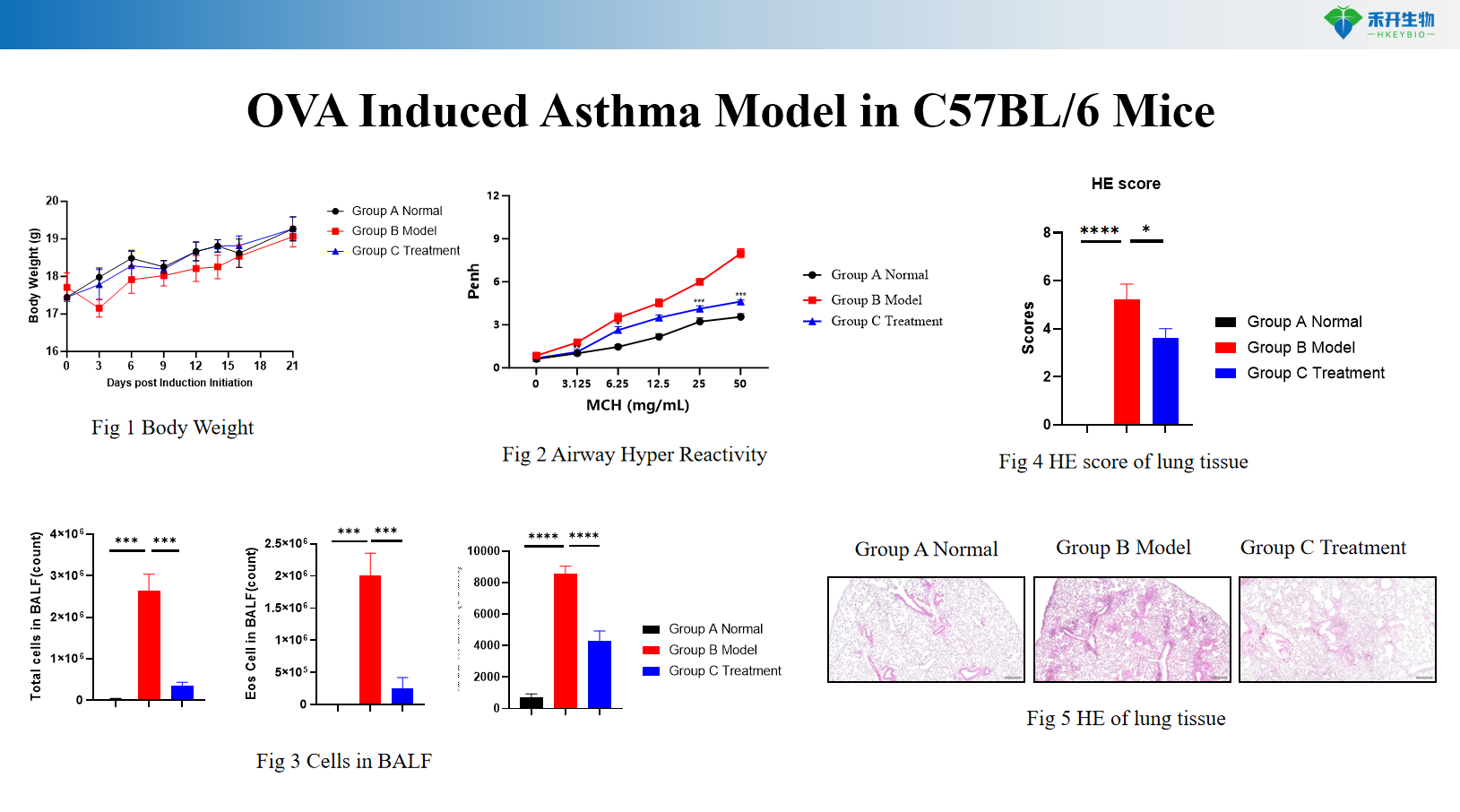
Model astmy indukowanej OVA u myszy BALB/c
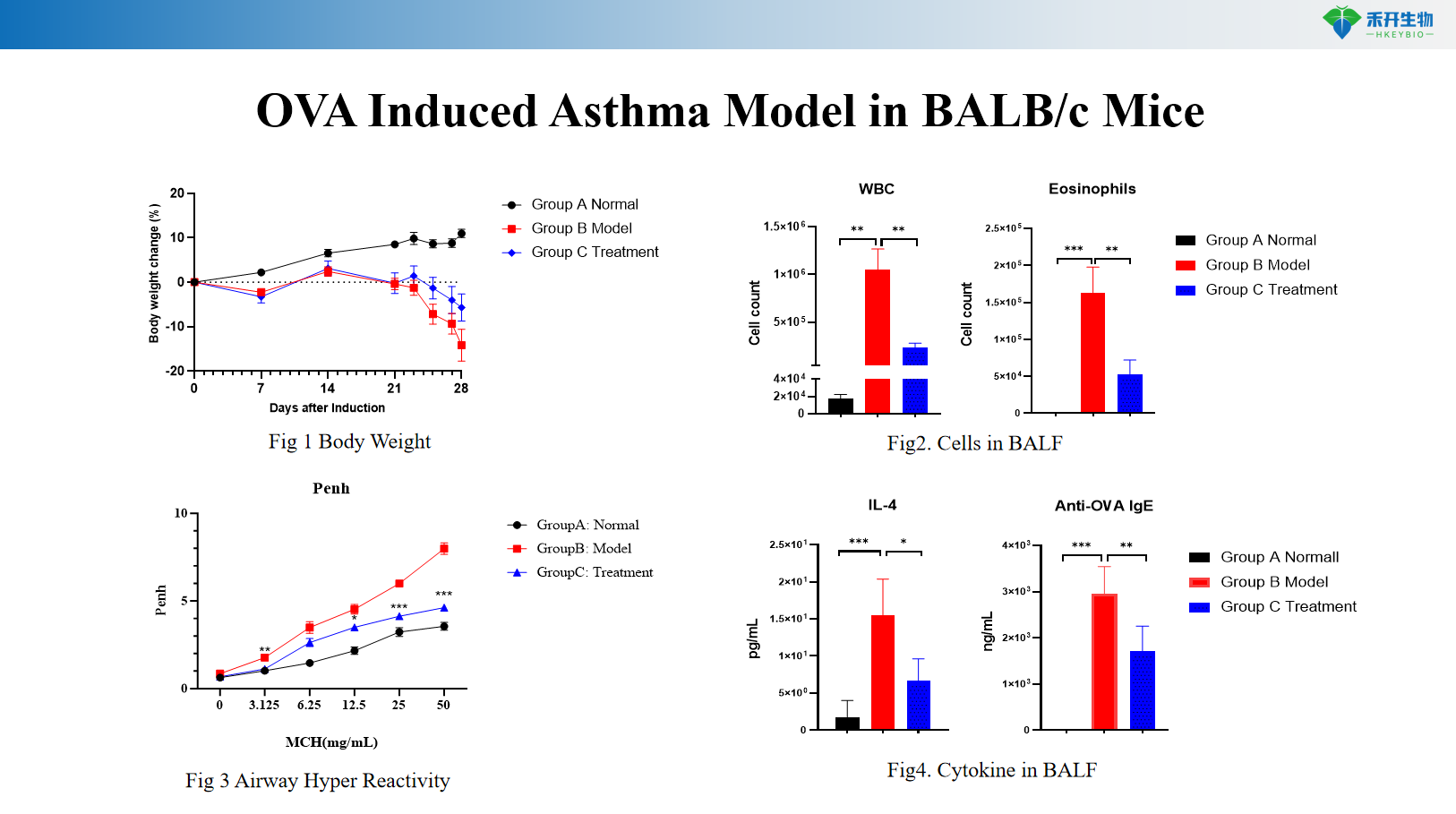
Model astmy indukowanej OVA u myszy HIS
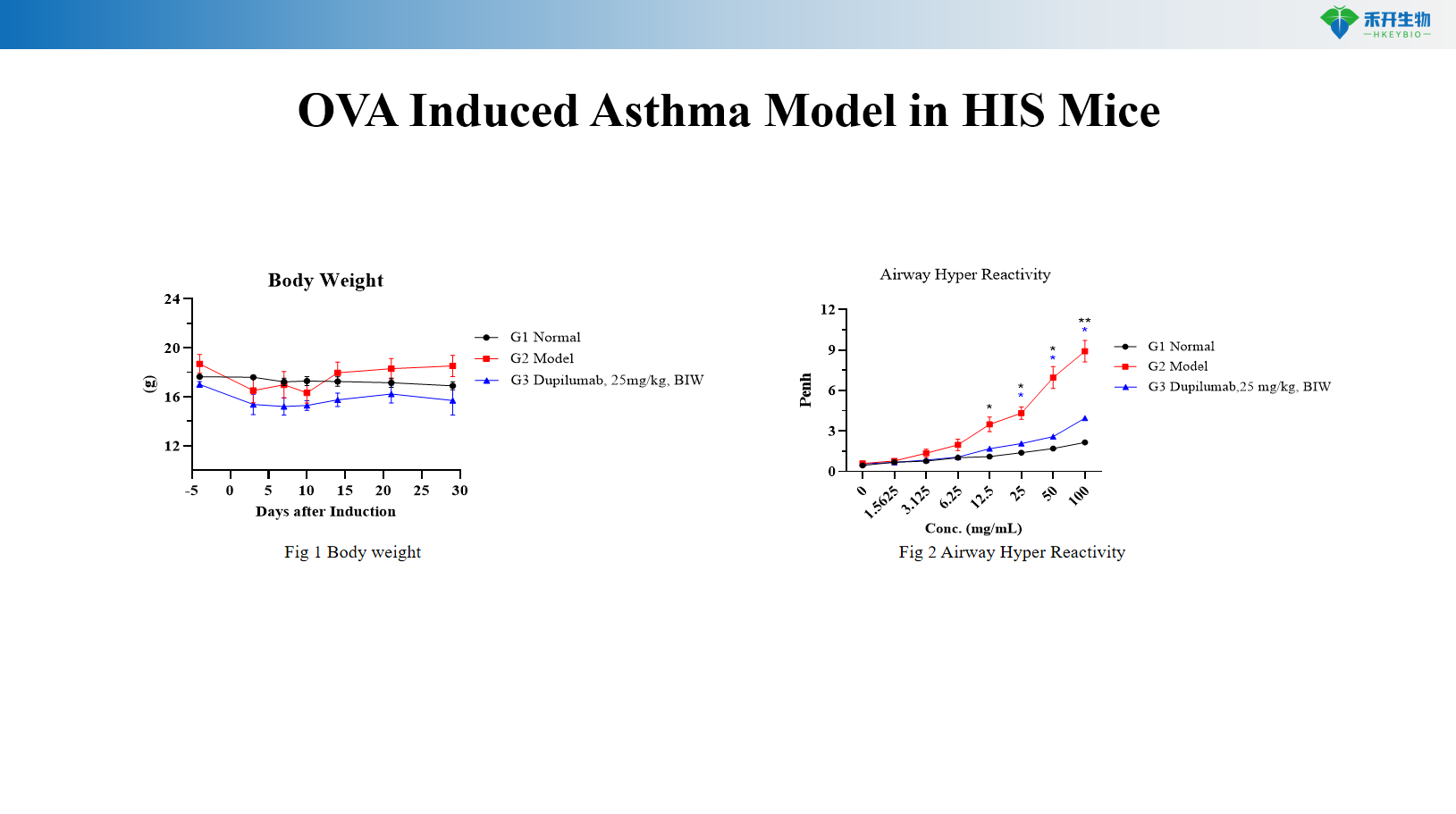
Model astmy indukowanej OVA+MC903 u myszy C57BL/6
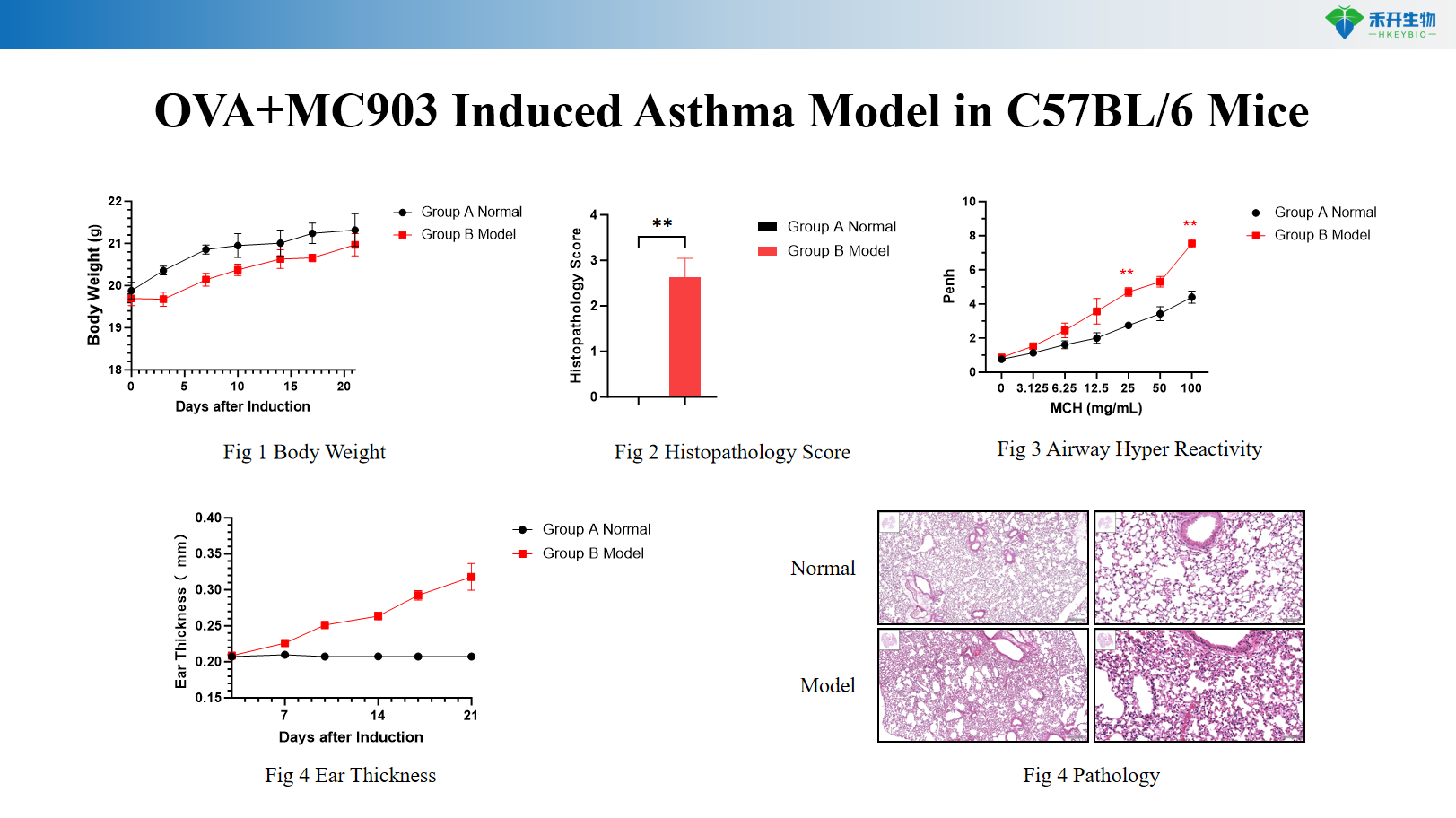
Model astmy neutrofilowej indukowanej OVA+LPS u myszy C57BL/6
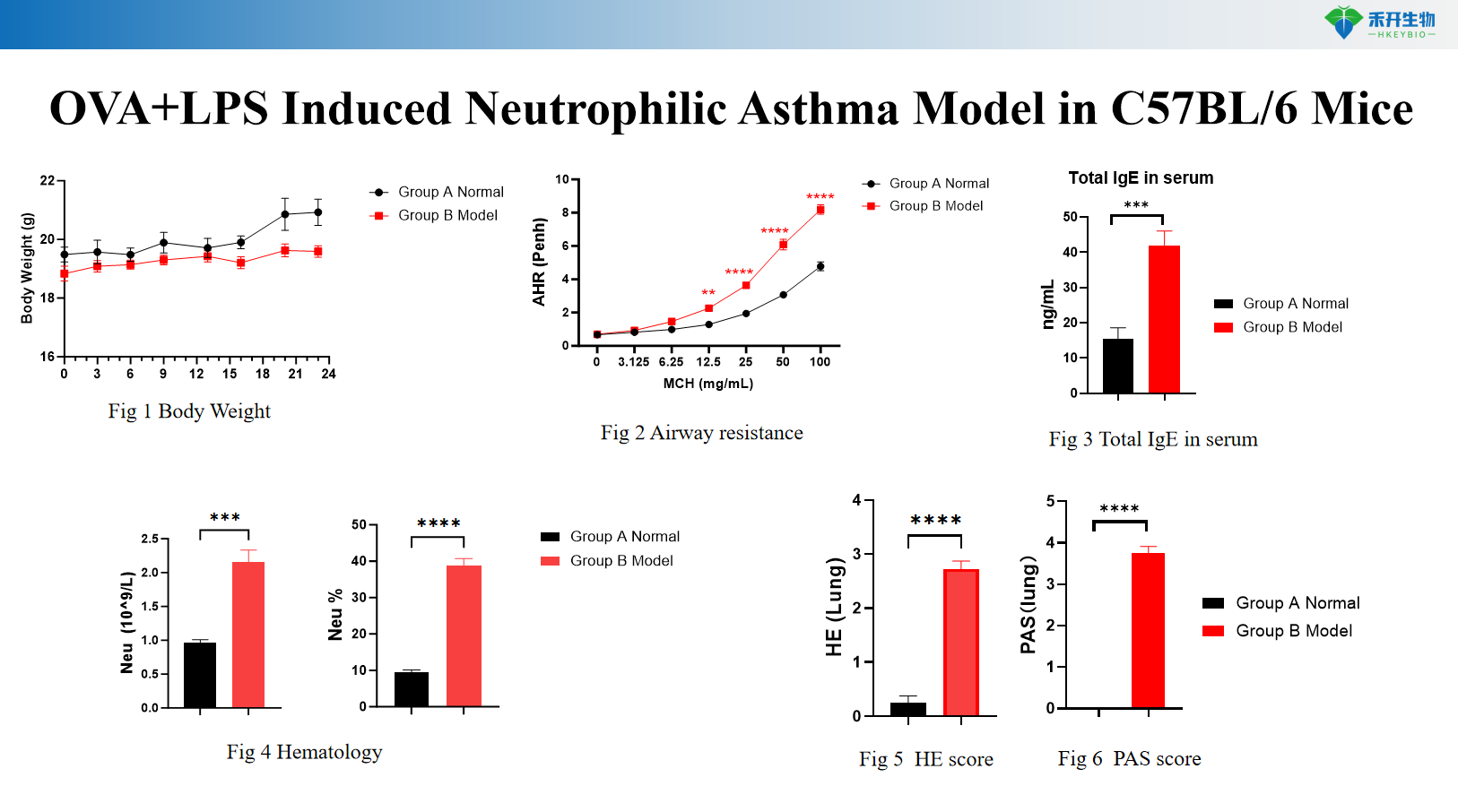
Model astmy indukowanej HDM u myszy C57BL/6
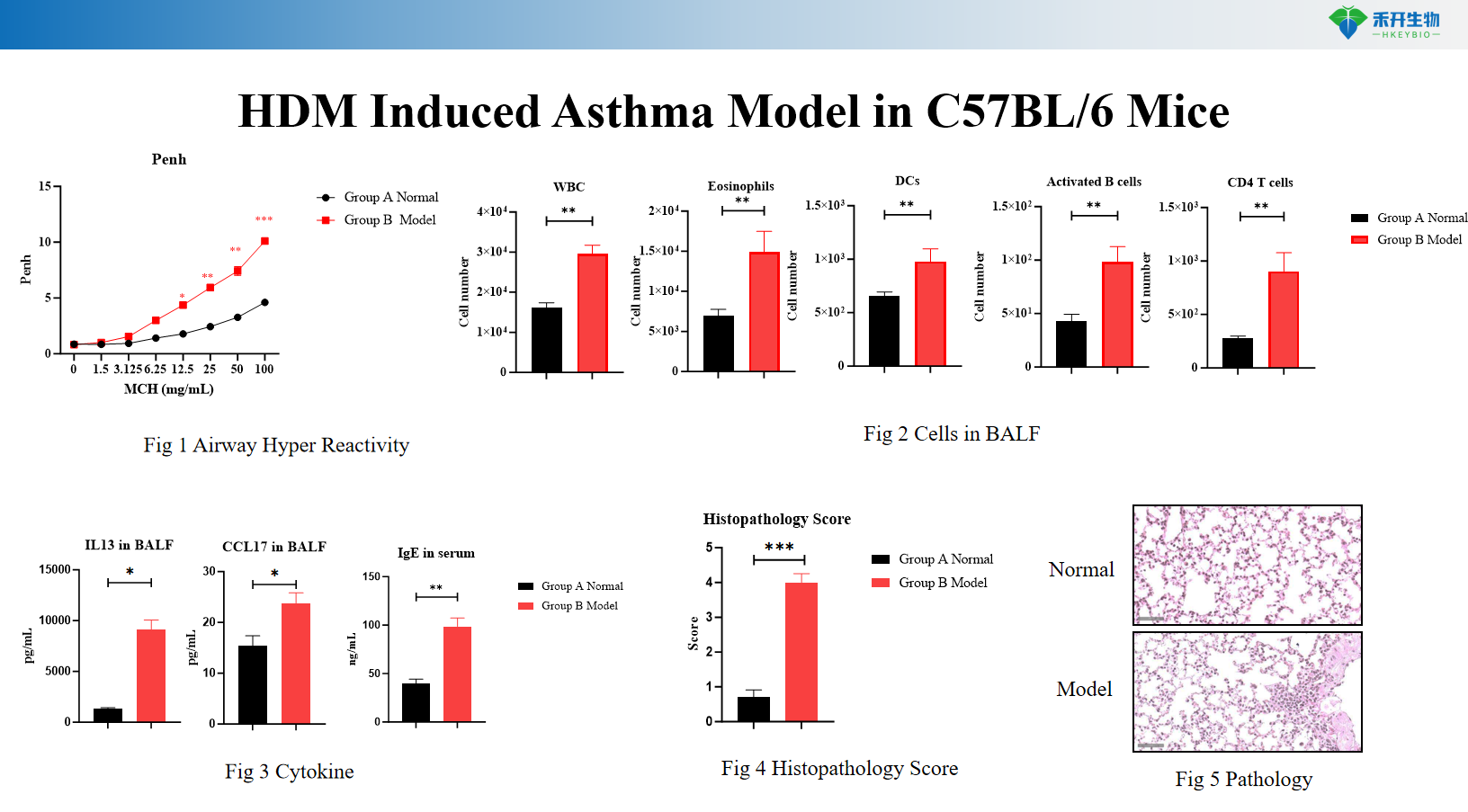
Model astmy indukowanej HDM u myszy IL4/IL4R
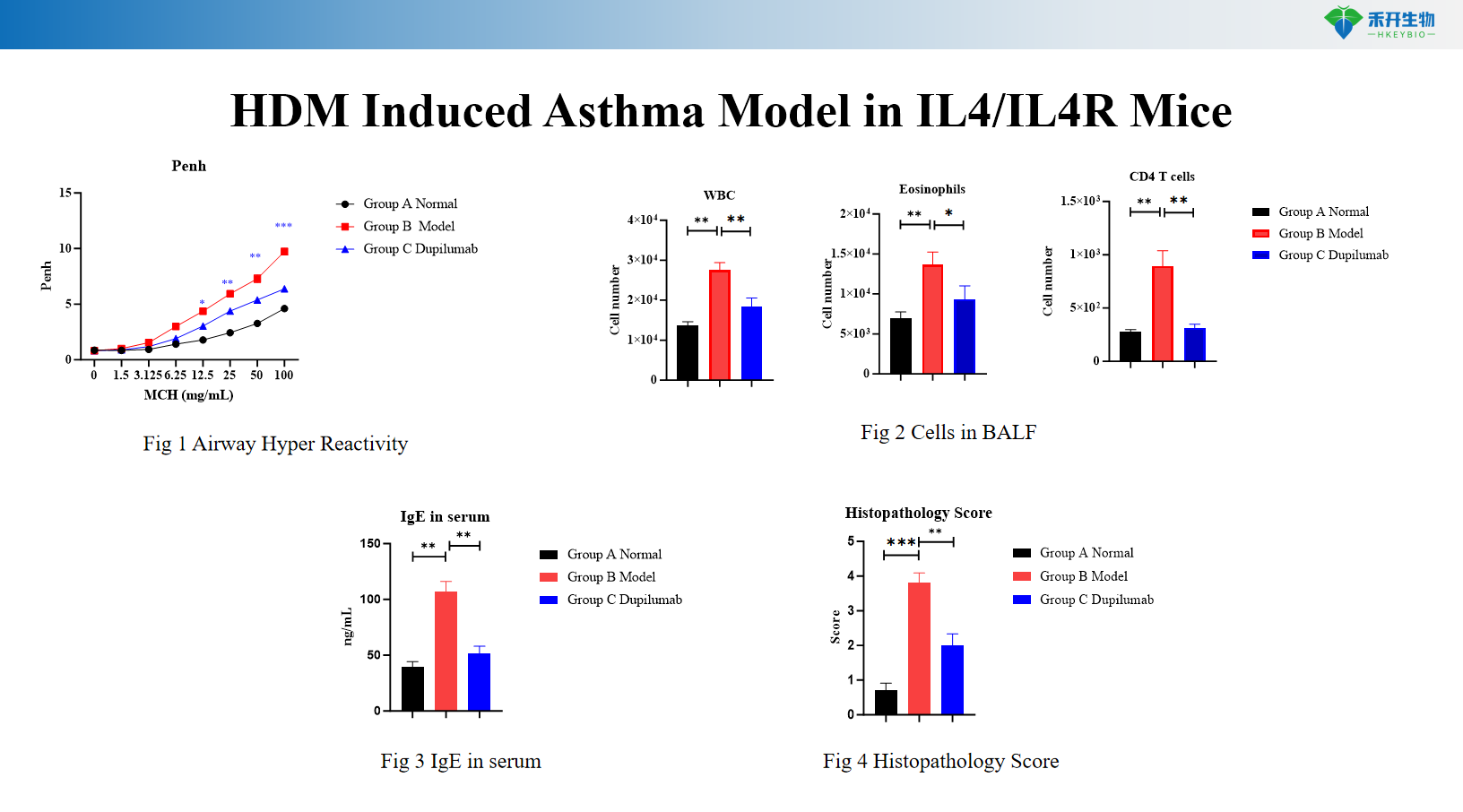
Model astmy indukowanej HDM+LPS u myszy C57BL/6
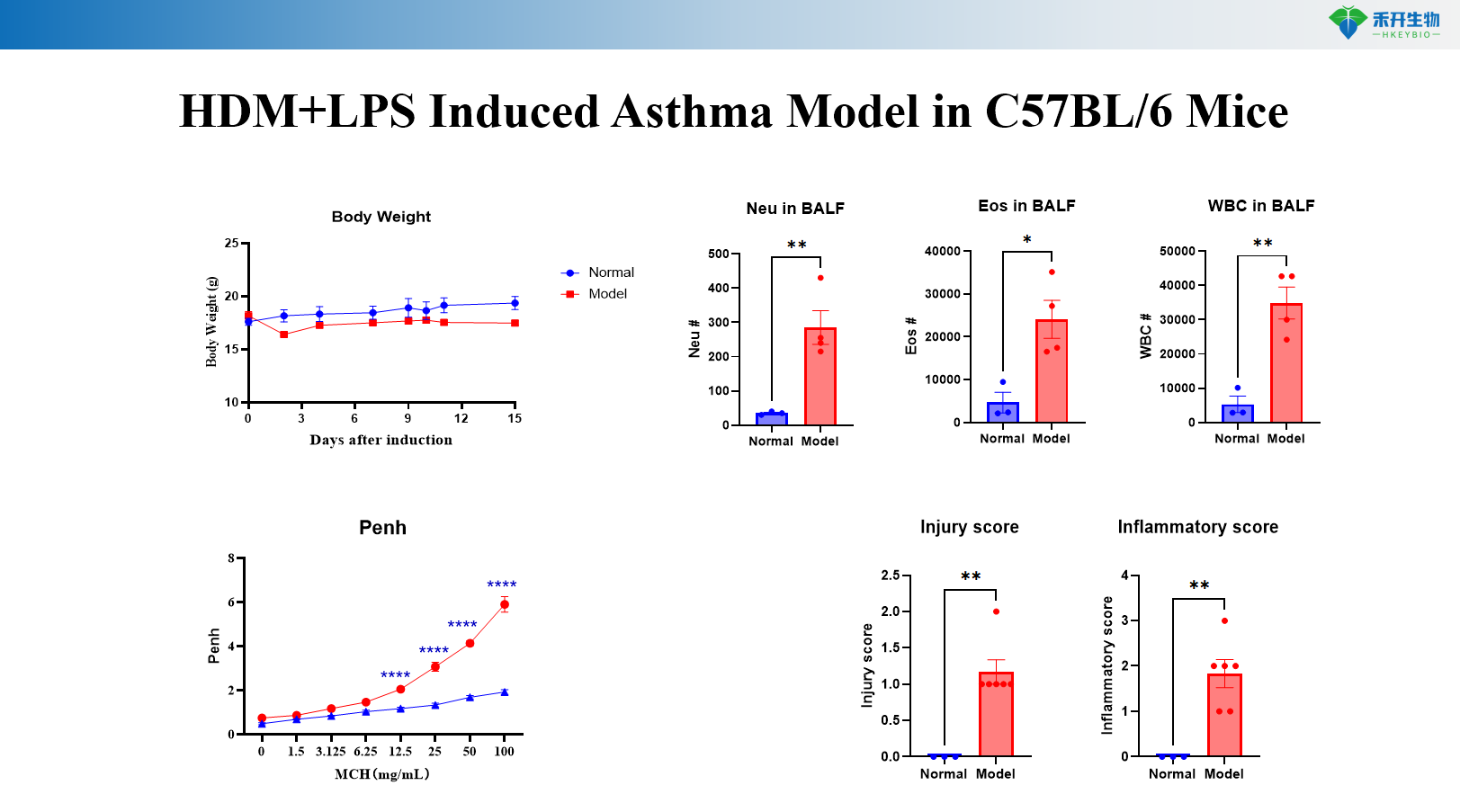
Model astmy indukowanej HDM+MC903 u myszy C57BL/6

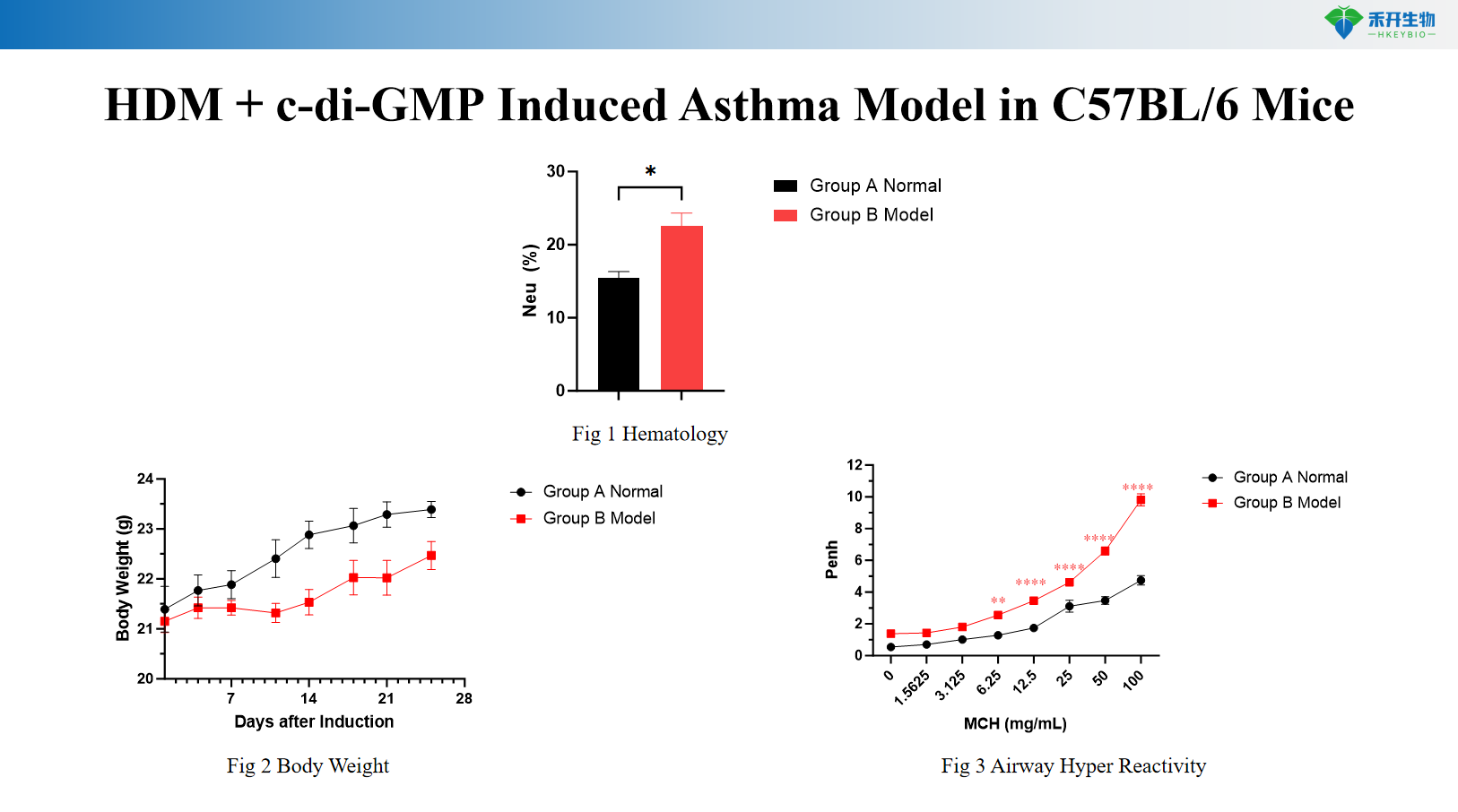
Model astmy indukowanej HDM + c-di-GMP u myszy C57BL/6
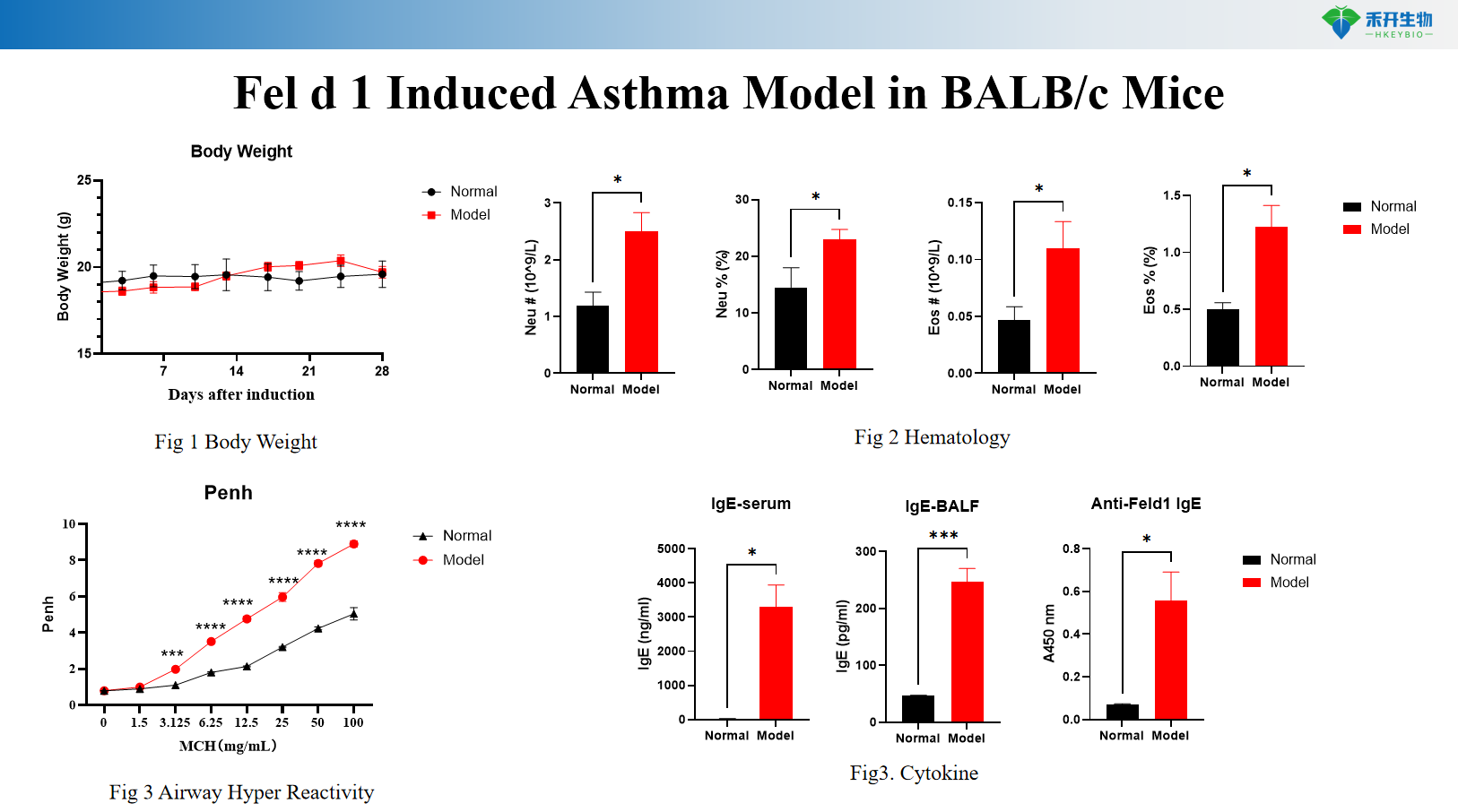
Model astmy indukowanej Fel d1 u myszy BALB/c
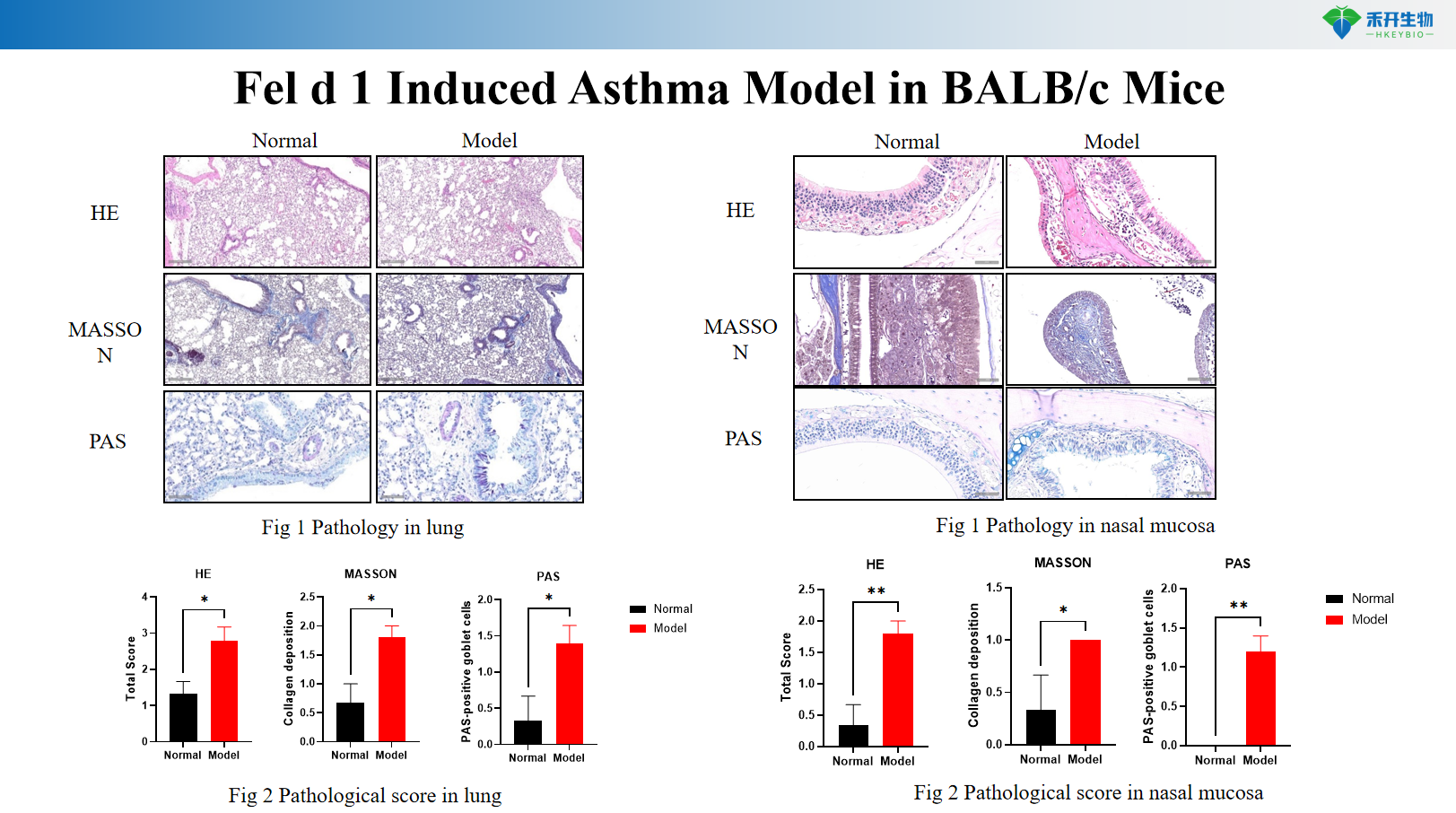
• Testowanie skuteczności leków biologicznych (anty-IL-4Rα, anty-IL-5, anty-IL-13, anty-TSLP, anty-IL-33)
• Ocena inhibitorów małocząsteczkowych (inhibitory JAK, inhibitory PDE4, antagoniści CRTH2)
• Walidacja celu dla Th2, Th17 i szlaków cytokin pochodzących z nabłonka
• Odkrycie biomarkerów (IgE, sygnatury cytokin, markery eozynofili/neutrofili)
• Badania farmakologiczne i toksykologiczne umożliwiające IND
Parametr |
Specyfikacja |
Gatunek/szczep |
C57BL/6, BALB/c, HIS humanizowany, transgeniczny IL4/IL4R |
Metoda indukcyjna |
OVA ± ałun ± MC903 ± LPS; HDM ± LPS ± MC903 ± c-di-GMP; Fel d 1 + ałun |
Czas trwania nauki |
3–8 tygodni (fazy uczulenia + prowokacji) |
Kluczowe punkty końcowe |
Masa ciała, AHR (inwazyjna/nieinwazyjna), cytologia BALF (eozynofile, neutrofile, makrofagi), całkowite IgE w surowicy i IgE swoiste dla alergenu, poziomy cytokin (IL-4, IL-5, IL-13, IL-17, IFN-γ), histopatologia płuc (HE, Masson, PAS) z punktacją, hematologia (opcjonalnie) |
| Pozytywna kontrola | Deksametazon lub przeciwciało anty-IL-4Rα dostępne jako związki referencyjne |
Pakiet danych |
Surowe dane, raporty analityczne, liczba komórek BALF, wyniki testu ELISA, preparaty histologiczne, dane dotyczące funkcji płuc, bioinformatyka (opcjonalnie) |
P: Jak wybrać odpowiedni model AD dla mojego kandydata na lek?
Odp.: W przypadku astmy eozynofilowej (Th2-high) zalecane są modele OVA lub HDM w BALB/c lub C57BL/6. W przypadku astmy neutrofilowej lub mieszanej astmy granulocytowej odpowiednie są modele OVA+LPS lub HDM+c-di-GMP w C57BL/6. Humanizowane myszy HIS idealnie nadają się do testowania leków biologicznych specyficznych dla człowieka. Myszy transgeniczne IL4/IL4R nadają się do badań szlaku Th2. Nasz zespół naukowy może pomóc w wyborze modelu w oparciu o konkretny cel.
P: Jaka jest różnica pomiędzy modelami indukowanymi OVA i HDM?
Odp.: OVA jest alergenem modelowym wymagającym adiuwanta do uczulenia, wywołującego silną odpowiedź Th2. HDM jest klinicznie istotnym alergenem ludzkim zawierającym proteazy, które aktywują zarówno odporność wrodzoną, jak i nabytą, bardziej naśladując patogenezę ludzkiej astmy alergicznej.
P: Czy te modele można wykorzystać do badań umożliwiających IND?
O: Tak. Badania można przeprowadzić zgodnie z zasadami GLP dotyczącymi zgłoszeń regulacyjnych (FDA, EMA).
P: Czy oferujecie dostosowane protokoły badań (np. różne harmonogramy uwrażliwiania/charakteryzowania, terapie skojarzone)?
O: Absolutnie. Nasz zespół naukowy dostosowuje protokoły indukcji, harmonogramy leczenia i analizy punktów końcowych do konkretnego kandydata na lek.
P: Jaki jest typowy harmonogram pilotażowego badania skuteczności?
Odp.: Większość modeli astmy, włączając uczulenie, prowokację, leczenie i analizę punktów końcowych, jest gotowa w ciągu 4–6 tygodni.
